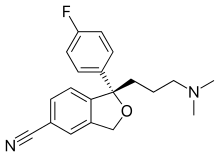
化学式
化學式(chemical formula)是用化学元素符号、数字、其他符号来表示组成特定化合物或分子的“原子化学比例信息”的一种公式;这些符号或数字被限制在單一行列排印,其中可能包括下标和上标。
化学式包括:分子式、实验式、结构式和电子式等表示方式。
上述“其他符號”有:
讀法
化學式的通則讀法,一般是從右向左、由正向負,讀作「X化X」,如:
當一個分子中原子個數不止一個時,還要讀出粒子個數,如:
- ,讀作「五氧化二釩」
帶有酸原子團的分子則讀作「O酸X」,如:
- ,讀作「硫酸鈉」。
另外,有的要讀「氫氧化X」,如:
- ,讀作「氫氧化鈉」。
而在讀含多種氧化數的化合物時還要注意其化合價數,例如:
- ,讀作「鐵離子」
- ,讀作「氯化鐵」
- ,讀作「亞鐵離子」
- ,讀作「氯化亞鐵」。
若含結晶水,應先讀出結晶水的個數,讀作「X水合X」,如:
- ,讀作「五水合硫酸銅」
若結晶水個數為1,也應讀出個數,讀作「一水合X」。
化學式的寫法
依據用途不同,同一種物質可能具有多種化學式寫法,以下列出幾種常用寫法:
最簡式
最簡式()又稱實驗式、簡式,是用元素符號表示化合物分子中各元素的原子個數比的最簡關係式。
最簡式一般都是通過分析化學的元素分析法()獲得的,尤其是通過有機化學中燃燒法測定化合物中碳氫比,因此最簡式又稱實驗式。
例如:過氧化氫()以最簡式僅記作,儘管它的一個分子中含有兩個氫原子與兩個氧原子。另一個例子是正己烷(),它以最簡式記作。
最簡式無法表示分子內原子的具體個數,亦無法表示分子結構,但在分析物質中某種元素的比例時起到重要作用。
例如:乙炔、苯的實驗式均為,但乙炔的分子式是,苯的分子式是。
分子式
分子式()僅適用於分子化合物。非分子型化合物不宜用分子式表示,只能用實驗式表示。
例如:氧氣、二氧化碳、硫酸、乙烯等可用分子式、、、等表示。
當分子式相同時,也有可能不是一種物質,它們有可能是同分異構物。
例如:乙醇和甲醚分子式相同(皆是),但二者為不同物質。
示性式(结构简式)
示性式[1](rational formula)或稱结构简式(condensed formula),一般用來表示有機物,其分子中所含官能基的簡化結構式。
例如:乙醇和甲醚分子式皆相同(皆是),如何區分二者,就須看其示性式。乙醇示性式為;甲醚為。
結構式
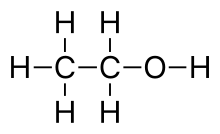
結構式()是用元素符號和短線表示化合物(或單質)分子中原子的排列和結合方式的式子。為一種直觀描述分子式的方法,常用於有機化合物。
以乙醇為例:
有機化合物
有機化合物的化學式,通常使用分子式與結構式表示。[3][4]
- 分子式僅表示一種物質的組成成份,如乙烯的分子式:
- 結構式則亦表示了一種物質的組成結構。
- 通常來說,分子式可能會受同分異構體的困擾,而結構式則不會。
- 如乙烯的結構式:
注意這裡的兩個碳原子間用雙橫線連接以示雙鍵。表示三鍵時,則可用三橫線。單鍵的橫線通常不寫,但在可能存在歧義時應書寫。
此外,在書寫分子較大的有機物的示性式時,可以將重複的部分簡記,如正十八烷記作:
有時也用n作為未知數代表通式,如烷烴通式CnH2n+2。
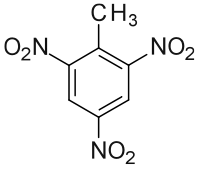
- 芳香烴的結構式通常用苯環表示。如2,4,6-三硝基甲苯:
希尔系统
希尔系统(Hill system)或希尔记法(Hill notation)是一种书写最简式、分子式和结构式的系统,首先表示分子中的碳原子数,随后是氢原子数,然后是其他所有化学元素的原子数,按元素符号的字母顺序排列。当化学式不含碳时,所有元素(包括氢)按字母顺序列出。
通过这些规则,根据公式中每个元素的原子数对公式进行排序,由于早期元素或数字的差异被视为比任何后期元素或数字的差异更为显著,比如将文本字符串按字典顺序排序,可能将化学公式排列成希尔顺序。
希尔系统于1900年由美国专利商标局的Edwin A. Hill首次发布。[5]它是化学数据库和印刷索引中最常用的系统,用于对化合物列表进行排序。 [6]
使用希尔系统的化学式列表按字母顺序排列如上。当符号以相同字母开头时,单字母元素位于两个字母符号之前(“B”在“Be”之前,“Be”在“Br”之前 ”)。[6]
以下化学式使用希尔系统编写,并按照希尔顺序列出:
- BrI
- BrClH2Si
- CCl4
- CH3I
- C2H5Br
- H2O4S
注釋
- https://terms.naer.edu.tw/detail/f4dc4a7664152d3b7579df870efe5323/
- General, Organic, and Biological Chemistry, H. Stephen Stoker 2012
- 第五章化學反應 (页面存档备份,存于),物質科學化學篇(上)講義 編者:陳義忠 1986
- 分子式(Molecular Formula)與結構式(Structural Formula) (页面存档备份,存于) 國科會高瞻自然科學教學資源平台
- Edwin A. Hill. . J. Am. Chem. Soc. 1900, 22 (8): 478–494 [2022-01-03]. doi:10.1021/ja02046a005. hdl:2027/uiug.30112063986233. (原始内容存档于2021-02-28).
- Wiggins, Gary. (1991). Chemical Information Sources. New York: McGraw Hill. p. 120.