布赫瓦尔德-哈特维希偶联反应
布赫瓦尔德-哈特维希偶联反应(英文:Buchwald–Hartwig coupling),又称布赫瓦尔德-哈特维希反应、布赫瓦尔德-哈特维希交叉偶联反应、布赫瓦尔德-哈特维希胺化反应,指钯催化和碱存在下胺与芳卤的交叉偶联反应,产生C-N键,生成胺的N-芳基化产物。
| 布赫瓦尔德-哈特维希胺化反应 | |
|---|---|
| 命名根据 | 史蒂芬 布赫瓦尔德 哈特维希 |
| 反应类型 | 偶联反应 |
| 标识 | |
| 有机化学网站对应网页 | 布赫瓦尔德-哈特维希偶联反应 |
| RSC序号 | RXNO:0000192 |


此反应是合成芳胺的重要方法。
反应中的芳卤也可为拟芳卤三氟甲磺酸的酚酯所代替。胺可为伯胺或仲胺,胺上的取代基可以为任何有机基团。钯催化剂常为钯磷配合物,如四(三苯基膦)钯(0),也可为三(双亚苄基丙酮)二钯(0)[1] 等其他钯配合物。
类似的反应为施蒂勒反应和赫克反应。反应也可扩展到碳亲核试剂,如丙二酸酯;以及扩展到氧亲核试剂如酚,用于合成二芳醚,由此提供了铜介导的乌尔曼二芳醚合成和戈尔德贝格反应以外的选择。
历史
布赫瓦尔德-哈特维希这一类型的反应最早是由乌克兰的列夫·M·亚古波尔斯基等在1986年发现的。他们用多取代的活化氯代芳烃与苯胺衍生物在1mol%的[PdPh(PPh3)2I]催化之下进行反应,得到了偶联产物,产率中等。[2]
此后美国的布赫瓦尔德和哈特维希两个团队又分别在 1994 年重新发现这个反应。耶鲁大学的哈特维希等用的是对溴甲苯与三丁基锡基胺之间的偶联。[3]
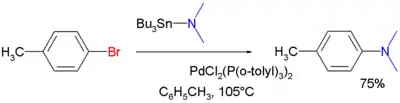
麻省理工学院的布赫瓦尔德等用的则是间溴苯甲醚与另一三丁基锡胺之间的偶联,见下。[4]
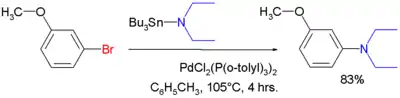
后来又发展了第二代的布赫瓦尔德-哈特维希反应,即用游离胺和强碱,代替最早使用的氨基锡烷。[5]
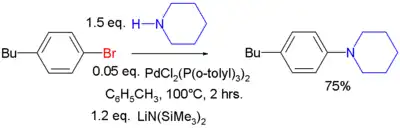
反应机理
反应的催化循环如下。
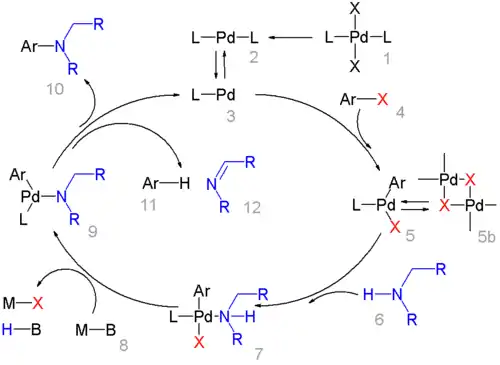
首先PdII催化剂(1)被还原为活性的Pd0物种(2),(2)脱去一个配体形成(3),进入催化循环。芳卤(4)与(3)发生氧化加成形成中间体(5),(5)与自身二聚物(5b)形成平衡。接下来,(5b)中的一个卤原子被胺取代,形成中间体(7),(7)被强碱(8)去质子化,生成(9)。然后(9)有两种可能的转化方式,一是发生还原消除生成需要的产物芳胺(10),二是发生β-氢消除生成副产物芳烃(11)和亚胺(12)。两种情况下Pd-L物种都获得再生,进入下一个催化循环。
展望
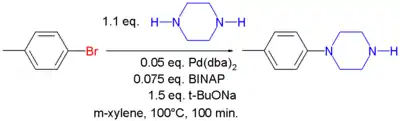
对反应所用溶剂的研究发现,对于某些底物来说,甲基吡咯烷酮和二甲基乙酰胺等非质子溶剂可以促进β-氢消除一步发生。以及非质子非极性溶剂(如间二甲苯)虽不能很好地溶解反应用碱叔丁醇盐,此类溶剂仍是此反应最好的溶剂。[6]
参见
参考资料
- John P. Wolfe and Stephen L. Buchwald (2004). "Palladium-Catalyzed Amination Of Aryl Halides And Aryl Triflates". Org. Synth.; Coll. Vol. 10: 423.
- N. B. Kondratenko, A. A. Kolomejcev, B. O. Mogilevskaya, N. M. Varlamova, L. M. Yagupolskii. . Zh. Org. Khim. (Rus.). 1986, 22 (8): 1721–1729.
- Frederic Paul, Joe Patt, John F. Hartwig. . J. Am. Chem. Soc. 1994, 116 (13): 5969–5970. doi:10.1021/ja00092a058.
- Anil S. Guram and Stephen L. Buchwald. . J. Am. Chem. Soc. 1994, 116 (17): 7901–7902. doi:10.1021/ja00096a059.
- Janis Louie and John F. Hartwig. . Tetrahedron Letters. 1995, 36 (21): 3609–3612. doi:10.1016/0040-4039(95)00605-C.
- Henrik Christensen, Sren Kiil, Kim Dam-Johansen, Ole Nielsen, and Michael B. Sommer. . Org. Process Res. Dev. 2006, 10 (4): 762–769. doi:10.1021/op050226s.
外部链接
- 布赫瓦尔德-哈特维希反应(页面存档备份,存于)(英文)