环己烷构象
历史背景
很早就有人提出环己烷可能不是平面型结构。1890年,德国人赫尔曼·萨克森(Hermann Sachse)提出通过折纸来构建环己烷“对称”和“非对称”结构(即现椅型和船型结构)的方法,从他的文章可以感受出,他已经知晓这些构象有两种不同的氢原子(即现直键氢和平键氢)以及两种椅型结构可能会相互转化,甚至还意识到两种椅型结构的分布可能受环上某些取代基的影响。不过他的文章没有获得化学家的足够重视,一方面是文章的数学成分太多,难以理解,另一方面则是他的文章没有发表到主要的期刊上。1893年仅31岁的萨克森去世,他的研究也就此结束。直到1918年恩斯特·摩尔(Ernst Mohr)用新问世的X射线晶体学技术测定金刚石结构时,才发现所得结构中的基础结构单元正是萨克森预测过的椅型结构,才使环己烷构象研究重新进入焦点之中。[1][2][3]
椅型构象
sp3杂化的碳原子是四价的,键间角度为109.5°,所以环己烷不是平面的键角120°的正六边形结构,而是采取多种三维的构象。椅型构象描述的是普通状态环己烷最稳定的构象,25度时99.99%的环己烷分子都是这种构象。德里克·巴顿和奥德·哈塞尔因对环己烷和其他分子构象的研究而获得诺贝尔化学奖。
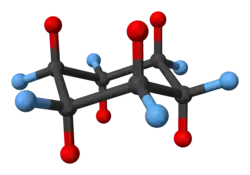
能量最低的椅型构象中,12个氢原子中有6个处于竖直方向(红色)——这些碳-氢键互相平行,呈轴向排列,分列环上下,称为直键。另6个氢处于近似水平方向(蓝色)——这些碳-氢键大致平伏,分别稍向下和向上翘起,称为平键。对于同一碳原子来说,若与它相连的直键氢是向上的,则平键氢稍向下,反之亦然。

观察可知,对于连有向上直键、稍向下平键的碳原子,与其相邻的两个碳原子必然连有向下直键和稍向上平键。而且环中相对碳原子所连平键和直键的方向也必然是分别相反的(如H1和H4)。所以对于反式的邻二取代环己烷,两个取代基只會同时为平键或同时为直键,总之分处环两边。同样对于顺式的邻二取代环己烷,两个取代基必定是一个为平键,一个为直键,而且指向同一个方向。其他取代的环己烷衍生物也可以依这样推理。
椅型构象中2、4、6号碳同处一个平面,1、3、5号碳同处一个平面。位于上面的平面的碳连有向上的直键、稍向下的平键,位于下层平面的碳连有向下的直键和稍向上的平键。椅型中所有键角都近似正四面体键角,而且所有相邻碳上的氢都处于邻位交叉,没有扭转张力。
上面画出了环己烷的两个不同排列的椅型构象,对于未取代的环己烷而言,这两个构象是完全相同的,不过当环上有取代基时两个构象常是不同的,这可以通过构建分子模型来证实。两个椅型构象间的转化称为环翻转,该过程中所有直键氢变为平键氢,平键氢变为直键氢。最左边的碳原子在翻转后仍然处于最左边,只不过从上层平面变到下层平面(或相反),所以相连的平键、直键也相应发生变化,最右边的碳原子亦然。
两个椅型构象可能因存在取代基而能量不同。一般来说取代基尽量取平键,以避免位阻效应。对于有顺式1,3-双取代的分子,两取代基还要避免1,3-双直键立体作用。以甲基环己烷为例,它主要采取平键甲基的椅型构象,主要原因不是甲基处直键时与其他直键氢间的1,3-双直键作用,而是因为直键甲基会造成它与相隔的碳-碳键形成能量上不利的旁式构象(C1-CH3、C2-C3、C5-C6),即互成邻位交叉。不过1,3-双直键作用在1,3-顺式双取代分子中是显著的,例如在分析顺-1,3-二甲基环己烷时就要考虑到这一因素。需要注意的是并不是所有情况下都是平键能量更低,涉及电负性杂原子的端基异构效应就是著名的例外。
取代基对平键的偏重可以用A值来衡量,即其平键和直键构象异构体间的吉布斯自由能差。正的A值表示偏好平键。A值范围一般在0(氘等体积较小的取代基)到5 kcal/mol(如叔丁基等大取代基)之间。
船型构象
除D3d对称性的椅型构象(1)外环己烷还有半椅型/信封型(2)、扭船型(3/5,D2对称性)和船型(4)等构象,但只有这之中扭船型可以和椅型一样分离出来(因它为能量低点)。船型结构无角张力,但有两个轴向1,4-氢间的空间张力(即所谓旗杆氢作用),而且因两根碳-碳键处于重叠构象,所以也有扭转张力,不如椅型构象稳定。船型结构可以折成其他构象以减少张力,如比它更加稳定的扭船型。
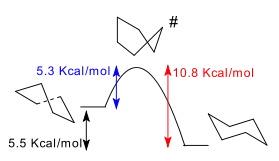
船型和半椅型构象分别是扭船型间和扭船-船型间的过渡态,无法分离出来。相对椅型,扭船型、船型和半椅型的能量分别为23、28、45 kJ/mol。[4]环翻转实际上就是经过两个半椅型、两个扭船型和一船型构象,从一椅型翻到另一椅型的过程。
椅型和扭船型间的能差可通过对正逆转化反应的活化能求差而间接求得。室温下只有很少(<0.1%)的环己烷是以扭船型存在的,但在800度时该比例可以增至30%。可借此对正反应(椅->扭船)进行研究。同样将1073K的环己烷迅速冷却到40K,用红外光谱研究,就可以得到相应的逆反应数据。
[6.6]手性烷(Chiralane[5] [6])(T点群)是仅由相同扭船型环己烷稠合而成的分子的例子。扭曲烷是另一被迫含有扭船型的分子。
环己烷衍生物
取代环己烷多有顺反异构体,两者无法通过类似线型分子中的简单单键旋转相互转化。顺式异构体(Z)中所指取代基指向同一方向(如同为向上直键/稍向上平键),而反式(E)则相反。虽然环己烷中的碳是由单键连接的,但环的刚性意味着顺反间相互转化只有在环系断裂时才可以发生。
二取代环己烷中构象的能量受两个取代基的相对排列方式影响。顺-1,2-或-1,4-二取代环己烷中的取代基分处直键和平键,环翻转后仍然是一平键一直键,至于哪种椅型更加稳定可以用取代基的A值进行预测。而反-1,2/1,4-二取代环己烷中的取代基必然同为直键或同为平键,但双直键的构象因多含四个旁式构象而能量较高。类似对于1,3-二取代环己烷,顺式主要是双平键的构象,环翻转后得到的双直键构象立体张力太大。反-1,3-二取代环己烷类似顺-1,2/1,4-,可在两个近似的直键-平键椅型间翻转。
对某些环己烷衍生物来说扭船型可能是更稳定的。如缺乏1,3-双直键作用的1,2,4,5-四噻己环(用-S-替换环己烷的4个对称-CH2-)的3,3,6,6-四甲基衍生物。1,4-环己二酮中稳定的构象也是扭船型,由于分子中无1,4-氢间作用。
顺-1,4-二叔丁基环己烷若为船型则有一个叔丁基要处于直键。而在扭船型中两个体积较大的叔丁基都可放在平键,所以扭船是比椅型更稳定的构象(125K时核磁共振谱测得能差1.96kJ/mol)。
参考资料
- H. Sachse, Chem. Ber, 1890, 23, 1363; Z. Physik. Chem, 1892, 10, 203; Z. Physik. Chem., 1893, 11, 185-219.
- E. Mohr, J. Prakt. Chem., 1918, 98, 315 and Chem. Ber., 1922, 55, 230.
- This history is nicely summarised here 的存檔,存档日期2010-07-07..
- Conformational Study of cis-1,4-Di-tert-butylcyclohexane by Dynamic NMR Spectroscopy and Computational Methods. Observation of Chair and Twist-Boat Conformations Gill, G.; Pawar, D. M.; Noe, E. A J. Org. Chem. (Article); 2005; 70(26); 10726-10731. DOI: 10.1021/jo051654z Abstract (页面存档备份,存于)
- http://www.mazepath.com/uncleal/chiral2.gif (页面存档备份,存于) Chiralane
- . [2010-08-02]. (原始内容存档于2009-09-07).
外部链接
- Java applets of all conformations (页面存档备份,存于) from the University of Nijmegen
- Ring Conformations & Sterioisomers Detailed description of ring conformations and sterioisomers from Michigan State University