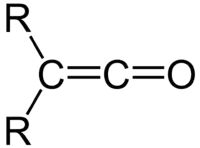
烯酮
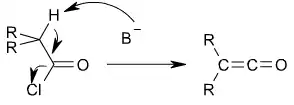
反应
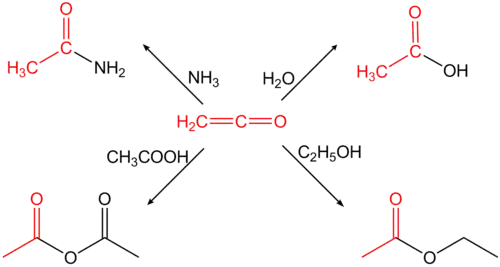
烯酮含有两个正交的π键,化学性质很活泼,是很好的酰基化试剂。
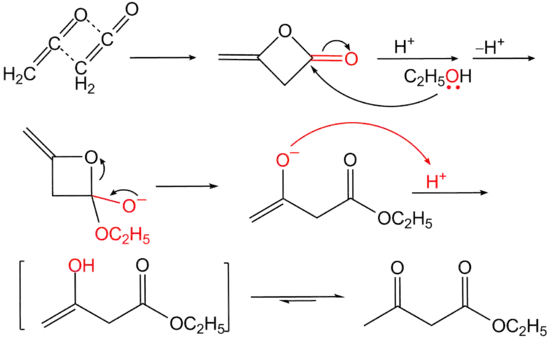
它可以二聚生成二乙烯酮的衍生物,也可与富电子的炔烃发生[2+2]环加成反应生成环丁烯酮衍生物。
二醇(HO-R-OH)与二烯酮(O=C=CH-R'-CH=C=O)反应,生成聚酯含有(-O-R-O-CO-R'-CO-)重复单元。
参考资料
- Staudinger, Hermann. . Berichte der deutschen chemischen Gesellschaft. 1905-03, 38 (2): 1735–1739. ISSN 0365-9496. doi:10.1002/cber.19050380283 (英语).
- C. D. Hurd (1941). "Ketene (页面存档备份,存于)". Org. Synth.; Coll. Vol. 1: 330.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.