莫德纳2019冠状病毒病疫苗
莫德纳2019冠状病毒病疫苗(英語:,簡稱:莫德納疫苗,代號:mRNA-1273,商品名:,國際非專利藥品名稱:elasomeran[12]),是美國國家過敏和傳染病研究所、生物醫學高級研究與開發管理局和莫德納公司合作開發的2019冠状病毒病疫苗,為一種信使核糖核酸(mRNA)疫苗,在2020年12月發表的第三期臨床試驗報告顯示該疫苗的有效率達94%[13]。該疫苗需要以肌肉注射方式接種兩次,每次的劑量為0.5毫升,兩次之間相隔4週[14]。
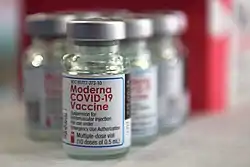 莫德納疫苗的包裝外觀 | |
| 臨床資料 | |
|---|---|
| 读音 | /məˈdɜːrnə/ mə-DUR-nə[1] |
| 商品名 | Spikevax[2] |
| 其他名稱 | mRNA-1273 CX-024414 COVID-19 mRNA Vaccine Moderna 莫德納疫苗 |
| AHFS/Drugs.com | Multum消费者信息 |
| MedlinePlus | a621002 |
| 核准狀況 | |
| 给药途径 | 肌肉注射 |
| ATC碼 |
|
| 法律規範狀態 | |
| 法律規範 | |
| 识别 | |
| DrugBank | |
| UNII | |
2020年12月18日,mRNA-1273獲得美國食品藥品管理局核發緊急使用授權[8][15][16][17],其後在2020年12月23日在加拿大[3][4]、2021年1月6日在歐盟[2][18][5]、2021年1月8日在英國[19],獲發出緊急使用授權。世衛組織於2021年4月30日將該疫苗列入緊急使用清單[20]。
2022年6月17日,美國食品及藥物管理局向莫德納發出緊急使用授權,6個月以上的嬰幼兒都可接種莫德納疫苗[21]。
開發及試驗
2020年1月,莫德納宣佈將會開發一款能夠誘發針對SARS-CoV-2的免疫力的RNA疫苗mRNA-1273[22][23][24]。mRNA-1273能夠通過編碼天然存在於SARS-CoV-2表面的預融合穩定刺突(S)蛋白來誘導對SARS-CoV-2的免疫力[25]。
莫德纳聲稱mRNA-1273疫苗在標準醫療冷櫃2--8°C(36--46°F)環境中,可儲藏至多30天;在零下20°C(−4°F)的環境中可儲藏至多4個月。[26]
臨床I至II期試驗
2020年3月,mRNA-1273的臨床I期人體試驗開始,美國國家過敏和傳染病研究所為合作伙伴[27]。莫德納與瑞士製藥商龍沙集團簽訂合作協議,由後者提供每年3億劑的產能[28]。
2020年5月25日,莫德納開始臨床IIa期試驗,共招募600位成年志願者測試疫苗的安全性和疫苗誘發的抗體水平差異[29]。
2020年7月14日,莫德納的科學家發表了mRNA-1273的I期劑量遞增臨床試驗的初步結果。結果顯示,依劑量不同,最早於注射後第15天,針對S1和S2的中和抗體已被誘發。在所有劑量組中均觀察到輕度至中度的不良反應,如發燒,乏力,頭痛,肌肉酸痛和注射部位疼痛,在大劑量組中更為常見[30][31][32]。低劑量的疫苗被認為是安全且有效的,可以進行相距29天的兩次100μg劑量的臨床III期試驗[30]。
臨床III期試驗
莫德納和美國國家過敏和傳染病研究所於2020年7月27日在美國展開臨床III期試驗,計劃招募3萬名志願者並將他們隨機分為兩組——一組注射兩劑100μg的mRNA-1273疫苗,另一組則注射安慰劑(0.9%的生理鹽水)。[33]
2020年11月16日,莫德納公佈其臨床III期試驗的初步數據,顯示mRNA-1273對預防感染2019冠狀病毒病的效力達到94%[26][34],副作用則包括類似流感的症狀,如注射部位疼痛、乏力、肌肉痠痛、頭痛等。[26]這並非臨床試驗的最終結果,因為莫德納的臨床試驗計劃至2022年末方有正式結論。[35]
2020年12月30日,莫德納將mRNA-1273的第三期臨床試驗數據、安全性及有效率的論文刊登於《新英格蘭醫學期刊》發表[36]。
後續調查及統計
莫德納在2021年4月13日表示,追踪超過3萬名已經接種兩劑疫苗的第三期臨床試驗參與者6個月後,至4月9日有900宗確診個案,顯示疫苗在6個月後的整體有效率仍達到90%,而預防重症的效力則為95%,莫德納同時稱已供應全球約1億3200萬劑疫苗,包括美國的1億1700萬劑,預期供應美國3億劑疫苗的目標可於7月底前達標[37]。
授權使用
2020年11月30日,莫德纳公司宣布将于当日向美国食品药品监督管理局申请该疫苗的緊急使用授權,并向欧盟药品管理局等全球多家监管机构提交了滚动申请。莫德纳表示到2020年底,该公司预计将在美国运送约2000万剂疫苗,2021年有望在全球生产5至10亿剂[38]。莫德納在2020年11月向德國媒體《週日世界報》透露每劑疫苗的售價約25至37美元,視乎訂單的數量而定[39][40]。
2020年12月18日,美國食品藥品監督管理局批准了mRNA-1273的緊急使用授權[15][41],並於三日後開始應用於美國2019冠狀病毒病疫苗接種計劃。這也是莫德納第一款獲得美國食品藥品監督管理局批准的產品。[42]
2021年1月8日,英國藥品與保健品管理局批准緊急使用莫德納疫苗[43]。然而,該批疫苗一直要到三個月後,才開始於英國2019冠狀病毒病疫苗接種計劃應用[44]。
2021年2月3日,新加坡批准緊急使用莫德納疫苗,成為首個批准該疫苗上市的亞洲國家[45]。至同年3月21日,此疫苗正式投入該國的接種計劃。
2021年4月30日,世界卫生组织宣布,将莫德纳疫苗列入紧急使用清单[46]。
2021年5月3日,世界衛生組織主導的疫苗獲得機制(COVAX)宣布已經與莫德納達成一項採購協議,购买5亿剂莫德纳2019冠状病毒病疫苗,将在2021年最后一个季度开始供应,在年底之前将提供3400万剂,到2022年再有4.66亿剂[47]。
2021年5月5日,中華民國衛生福利部食品藥物管理署發出莫德納疫苗的緊急使用授權[48]。截至2021年6月29日,莫德納疫苗已在全球48个国家和地区投入使用[49]。
2022年4月8日,莫德纳表示,在发现一小瓶疫苗被异物污染后,莫德纳将召回其制造商Rovi生产的在歐洲銷售的76.49万剂新冠疫苗。[50]
不良反应
各地應用情況
台灣
衛生福利部於2021年2月10日證實已經與莫德納簽約,莫德納將向台灣供應505萬劑疫苗,預計可於5月或6月運交首批疫苗[51]。衛生福利部食品藥物管理署於2021年5月20日證實收到莫德納發出的20瓶疫苗,共200劑的測試標準樣品[52]。美國政府於2021年6月19日捐贈台灣250萬劑美國生產的莫德納疫苗,並表明美國捐贈疫苗不會附加任何條件[53],這250萬劑疫苗於6月20日運抵台灣桃園國際機場[54]。2021年7月22日,衛福部與莫德納宣布雙方達成增購3500萬劑疫苗的協議,將於2022年及2023年分別交付2000萬劑及1500萬劑,除基本型疫苗,也包括加強應對變種病毒的次世代疫苗;另外在今年原有505萬劑疫苗的訂單額外追加多100萬劑,預料追加的疫苗份額可於2021年第四季交付[55]。
谣言
2021年3月,互联网上开始流传莫德纳疫苗中含有有毒物质的谣言。这一说法起源于3月开始在美国传播,之后在TikTok影片和Instagram照片的形式传播开来,并在一周内在Facebook上的分享量已超过1500次。有关文章之后又被社交平台如Exportail、Profession Gendarme、Qactus或AgoraVox以不同的形式在其他国家传播开来。这些文章共同指出,莫德纳疫苗中含有一种物质由90%的氯仿和10%的SM-102组成,对人类健康有害。在有关文章的声明中,也显示了来自美国生物技术公司Cayman Chemical网站的安全数据表的螢幕截图,另一部分的说明书将氯仿列为「危险成分」,同时警告可能会有癌症、不孕症、肾脏、肝脏和中枢神经系统损害的健康风险,一些网站如Qactus也将SM-102认定为是「致命毒药」。在谣言传开后,Cayman Chemical发表声明解释,SM-102是该公司「仅用于实验或临床研究」的产品之一,而具有相同名称的化学品可能有不同的名称,例如由其制造协议和预期用途定义的级别或配方。法新社事实核查小组对该訊息进行反驳,并在5月31日公布美国、欧洲或加拿大的监管机构并未将氯仿列为莫德纳疫苗的成分,而美国国家职业安全卫生研究所 (NIOSH)、化学物质毒性数据库 (RTECS) 和歐洲化學品管理局 (ECHA) 的分类和标签清单都没有列出与SM-102相关的任何危险[58]。
2022年3月,流传有莫德纳公司人工制造了SARS-CoV-2的传言。
參考文獻
- Moderna. (Video). YouTube. October 23, 2019 [January 19, 2021]. (原始内容存档于2021-02-28).
- . European Medicines Agency (EMA). [20 January 2021]. (原始内容存档于2021-03-12).
- . Health Canada. 23 December 2020 [23 December 2020]. (原始内容存档于2021-01-15).
- . COVID-19 vaccines and treatments portal. 23 December 2020 [23 December 2020]. (原始内容存档于2020-12-23).
- . European Commission (新闻稿). [6 January 2021]. (原始内容存档于2021-01-20).
- . Medicines and Healthcare products Regulatory Agency (MHRA). 8 January 2021 [8 January 2021]. (原始内容存档于2021-02-18).
- . Medicines and Healthcare products Regulatory Agency (MHRA). 8 January 2021 [9 January 2021]. (原始内容存档于2021-02-18).
- . U.S. 美国食品药品监督管理局 (新闻稿). [18 December 2020]. (原始内容存档于2021-03-17).
- . DailyMed. [20 December 2020]. (原始内容存档于2021-04-04).
- . U.S. Food and Drug Administration (FDA) (报告). 18 December 2020 [20 December 2020]. (原始内容 (PDF)存档于2021-08-14).
 本文含有此來源中屬於公有领域的内容。
本文含有此來源中屬於公有领域的内容。 - (PDF). Centers for Disease Control and Prevention (CDC). [2021-03-28]. (原始内容 (PDF)存档于2021-08-14).
- . Therapeutic Goods Administration (TGA) (新闻稿). 24 June 2021 [29 June 2021]. (原始内容存档于2021-06-27).
- . BBC. 2020-12-19 [2021-04-22]. (原始内容存档于2021-04-28).
- . Dosing & Administration. Infectious Diseases Society of America. 4 January 2021 [5 January 2021]. (原始内容存档于2020-12-20).
- . US National Institutes of Health. 18 December 2020 [19 December 2020]. (原始内容存档于2021-03-19).
- Oliver SE, Gargano JW, Marin M, Wallace M, Curran KG, Chamberland M, et al. (PDF). MMWR Morbidity and Mortality Weekly Report. January 2021, 69 (5152): 1653–56 [2021-03-28]. PMID 33382675. doi:10.15585/mmwr.mm695152e1. (原始内容 (PDF)存档于2021-02-09).
- Lovelace Jr, Berkeley. . CNBC. 19 December 2020 [19 December 2020]. (原始内容存档于2021-01-26).
- . Union Register of medicinal products. [14 January 2021]. (原始内容存档于2021-01-24).
- . U.K. Government. 8 January 2021 [8 January 2021]. (原始内容存档于2021-05-03).
- . World Health Organization. 2021-04-30 [2021-05-06]. (原始内容存档于2021-05-06).
- . 中央通訊社. 2022-06-18 [2022-07-04]. (原始内容存档于2022-07-05).
- Steenhuysen, Julie; Kelland, Kate. . Reuters. 2020-01-24 [2020-01-26]. (原始内容存档于2020-01-25) (英语).
- Karen Carey. . BioWorld. February 26, 2020 [1 March 2020]. (原始内容存档于27 February 2020).
- Gwen Everett. . Markets Insider. February 27, 2020 [1 March 2020]. (原始内容存档于2020-11-16).
- Pendleton, Devon; Maloney, Tom. . Bloomberg News. 18 May 2020 [18 May 2020]. (原始内容存档于2020-11-16).
CEO Bancel, other Moderna executives have been selling shares
- Berkeley Lovelace, Jr.; Noah Higgins-Dunn. . CNBC. 16 November 2020 [17 November 2020]. (原始内容存档于2020-11-16).
- . National Institutes of Health (NIH). 16 March 2020 [18 March 2020]. (原始内容存档于19 March 2020) (英语).
- . SWI swissinfo.ch. [2020-10-07]. (原始内容存档于2020-11-16).
- Clinical trial number NCT04405076 for "Dose-Confirmation Study to Evaluate the Safety, Reactogenicity, and Immunogenicity of mRNA-1273 COVID-19 Vaccine in Adults Aged 18 Years and Older" at ClinicalTrials.gov
- Lisa A Jackson; mRNA-1273 Study Group. . The New England Journal of Medicine. July 2020, 383 (20): 1920–1931. PMC 7377258
 . PMID 32663912. doi:10.1056/NEJMoa2022483.
. PMID 32663912. doi:10.1056/NEJMoa2022483. - Yun Li. . CNBC. July 14, 2020 [July 15, 2020]. (原始内容存档于November 16, 2020).
- Lisa A Jackson; mRNA-1273 Study Group. (PDF). The New England Journal of Medicine. July 2020 [2020-07-15]. PMC 7377258
 . PMID 32663912. doi:10.1056/NEJMoa2022483. (原始内容 (PDF)存档于2020-07-14).
. PMID 32663912. doi:10.1056/NEJMoa2022483. (原始内容 (PDF)存档于2020-07-14). - Palca, Joe. . NPR. 27 July 2020 [27 July 2020]. (原始内容存档于11 October 2020).
- Zimmer, Carl. . The New York Times. 20 November 2020 [21 November 2020]. (原始内容存档于2020-11-22).
- . Clinicaltrials.gov, US National Library of Medicine. 28 October 2020 [17 November 2020]. (原始内容存档于2021-02-25).
- Lindsey R. Baden, M.D., Hana M. El Sahly, M.D., Brandon Essink, M.D., Karen Kotloff, M.D., Sharon Frey, M.D., Rick Novak, M.D., David Diemert, M.D., Stephen A. Spector, M.D., Nadine Rouphael, M.D., C. Buddy Creech, M.D., John McGettigan, M.D., Shishir Khetan, M.D., Nathan Segall, M.D., Joel Solis, M.D., Adam Brosz, M.D., Carlos Fierro, M.D., Howard Schwartz, M.D., Kathleen Neuzil, M.D., Lawrence Corey, M.D., Peter Gilbert, Ph.D., Holly Janes, Ph.D., Dean Follmann, Ph.D., Mary Marovich, M.D., John Mascola, M.D., Laura Polakowski, M.D., Julie Ledgerwood, D.O., Barney S. Graham, M.D., Hamilton Bennett, M.S., Rolando Pajon, Ph.D., Conor Knightly, M.P.H., Brett Leav, M.D., Weiping Deng, Ph.D., Honghong Zhou, Ph.D., Shu Han, Ph.D., Melanie Ivarsson, Ph.D., Jacqueline Miller, M.D., Tal Zaks, M.D. . The New England Journal of Medicine. 2020-12-30 [2021-04-22]. (原始内容存档于2020-12-30).
- . 中央通訊社. 2021-04-14 [2021-05-03]. (原始内容存档于2021-05-04).
- . investors.modernatx.com. 2020-11-30 [2020-12-02]. (原始内容存档于2020-12-02) (英语).
- . The Indian Express. 2020-11-22 [2021-05-18]. (原始内容存档于2022-05-16) (英语).
- Staff, Reuters. . Reuters. 2020-11-22 [2021-05-18]. (原始内容存档于2021-08-22) (英语).
- Jr, Berkeley Lovelace. . CNBC. 2020-12-19 [2020-12-19]. (原始内容存档于2021-01-26) (英语).
- Lee, Jaimy. . MarketWatch. [2020-12-19]. (原始内容存档于2021-04-16) (美国英语).
- . BBC News. BBC. 2021-01-08 [2021-05-21]. (原始内容存档于2021-01-08).
- . The Guardian. 2021-04-07 [2021-05-21]. (原始内容存档于2021-07-03).
- Staff, Reuters. . Reuters. 2021-02-03 [2021-06-01]. (原始内容存档于2021-12-03) (英语).
- .
- . [2021-05-03]. (原始内容存档于2021-05-05).
- . 中央通訊社. 2021-05-05 [2021-05-29]. (原始内容存档于2021-05-07).
- hermesauto. . The Straits Times. 2021-06-29 [2021-06-30]. (原始内容存档于2021-07-12) (英语).
- . [2022-04-09]. (原始内容存档于2022-05-03).
- . 中央廣播電台. 2021-02-10 [2021-04-18]. (原始内容存档于2021-04-23).
- . 中央通訊社. 2021-05-19 [2021-05-29]. (原始内容存档于2022-04-20).
- . 自由時報. 2021-06-19 [2021-06-20]. (原始内容存档于2021-06-28).
- . 上報. 2021-06-20 [2021-06-20]. (原始内容存档于2021-06-29).
- . 中央通訊社. 2021-07-22 [2021-07-25]. (原始内容存档于2021-08-30).
- . 中國醫療. 2021-05-26 [2021-07-26]. (原始内容存档于2021-07-26).
- . Tokyo Shimbun. 2021-05-23 [2021-06-02]. (原始内容存档于2021-06-02).
- . Factuel. 2021-05-31 [2021-06-30]. (原始内容存档于2022-07-14) (法语).
延伸閱讀
- World Health Organization. (报告). 世界衛生組織. 2021. hdl:10665/339218. WHO/2019-nCoV/vaccines/SAGE_recommendation/mRNA-1273/background/2021.1.
外部連結
| 维基共享资源中相关的多媒体资源:莫德纳2019冠状病毒病疫苗 |