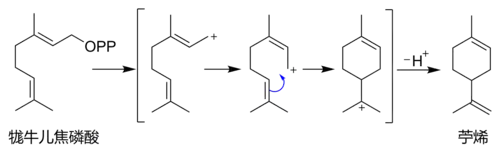
柠烯
(英語:;俗称柠檬油精)是一种环状单萜烯,室溫下容易揮發,广泛存在于各种柑橘屬果皮及香精油,特别是柠檬油、柠蒿油、橙子油、佛手柑油、莳萝油中。柠烯分子中含有一个手性中心,有左旋柠烯、右旋柠烯光学异构体与一种外消旋体。常温下这两种异构体都为无色有强烈宜人香味的易燃液体,左旋柠烯闻起来有柠檬/松节油味道,而右旋柠烯则有柠檬/橘子味道。
| D-柠烯 | |||
|---|---|---|---|
| |||
| IUPAC名 1-methyl-4-prop-1-en-2-yl-cyclohexene 1-甲基-4-(1-甲基乙烯基)-环己烯 | |||
| 英文名 | |||
| 别名 | 烯、烯、柠檬油精、 柠檬烯、双戊烯 | ||
| 识别 | |||
| CAS号 | 5989-27-5((R)) 138-86-3((R/S)) 5989-54-8((S)) | ||
| PubChem | 22311((R/S)) 439250((S)) | ||
| ChemSpider | 20939 (R/S), 388386 (S), 389747 (R) | ||
| SMILES |
| ||
| InChI |
| ||
| InChIKey | XMGQYMWWDOXHJM-UHFFFAOYAC | ||
| EINECS | 227-813-5 | ||
| ChEBI | 15384 | ||
| KEGG | D00194 | ||
| 性质 | |||
| 化学式 | C10H16 | ||
| 136.24 g·mol⁻¹ | |||
| 外观 | 无色液体,左旋异构体有柠檬气味,右旋异构体有柑橘气味 | ||
| 密度 | 0.8411 g/cm3 | ||
| 熔点 | -74.35 °C | ||
| 沸点 | 176 °C | ||
| 溶解性(水) | 难溶于水 | ||
| 危险性 | |||
| 警示术语 | R:R10, R38, R43, R50/53 | ||
| 安全术语 | S:S2, S24, S37, S60, S61 | ||
| 闪点 | 50 °C | ||
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |||
性状
左旋柠烯:即L-柠烯、(S)-(−)-柠烯。CAS号5989-54-8,EINECS号227-815-6,相对密度0.8407(21/4℃),沸点175.5-176.5℃(101.72kPa),折射率1.474,比旋光度 ,警示性质标准词有:R10, R38, R43, R50, R53,安全性质标准词有:S24, S37, S60, S61。存在于薄荷油、松针油中。
右旋柠烯:即D-柠烯、(R)-(+)-柠烯。CAS号5989-27-5,EINECS号227-813-5,相对密度0.8402(21/4℃),沸点175.5-176℃(101.72kPa),凝固点−95.5℃,折射率1.4743 (21℃),比旋光度 ,警示性质标准词有:R22。存在于柠檬油、蜜柑油、樟脑白油、香橙油等植物精油中。
外消旋体:即左旋柠烯和右旋柠烯的混合物,也称二聚异戊二烯、二聚戊烯、双戊烯、二戊烯(dipentene)。[2] 相对密度0.8404,沸点178.64℃,凝固点−95.3℃,折射率1.4744,无旋光性。不溶于水,与乙醇互溶。存在于樟脑白油、杉油、松节油、橙花油、香茅油中。
化学性质
柠烯的化学性质相对比较稳定,可以蒸馏而不分解。(R)-柠烯加热到300℃时发生外消旋化。如果温度更高,则柠烯分解为异戊二烯。[3]
潮湿空气中易被氧化为香芹醇和香芹酮。[4] 与硫磺作用失水生成对撒花烃,也会产生硫化氢和一些硫醚。
与无机酸共热时,异构化为有共轭双烯结构的α-松油烯,后者又很容易被氧化,生成有芳香性的对撒花烃。柠烯与顺丁烯二酸酐共热时,可以得到顺酐与α-松油烯发生狄尔斯-阿尔德反应生成的加合物。
柠烯可以发生烯烃的一般反应,其中两个双键可以都发生反应,也可以控制条件只让其中一个双键反应。用无水氯化氢/溴化氢处理时,二取代的烯烃先与卤化氢发生加成;但用mCPBA作环氧化时,三取代的烯烃先被环氧化,生成柠烯氧化物。如果mCPBA过量,则两个双键都被环氧化,得到柠烯二氧化物。
D-柠烯的非环双键可以与三氟乙酸在甲苯中发生反马氏规则加成,反应后用氢氧化钠将三氟乙酸酯水解,便可以得到(S)-(−)-α-萜品醇(松油醇)。[5]
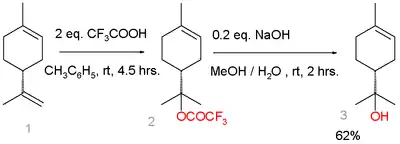
柠烯也可以在无机酸的存在下与水加成,生成α-松油醇和水合萜二醇。
用亚硝酰氯处理柠烯时,柠烯的环内双键与 NO−Cl 加成生成1-氯-2-亚硝基化合物,经互变异构得到α-氯代肟,然后用碱将氯化氢脱去得到不饱和的香芹酮肟,最后将肟用稀硫酸水解,便得到相应的酮——香芹酮。[6] 这是工业上制取香芹酮的主要方法。
用途
D-柠烯主要被用作制取香芹酮的前体,[6] 此外也用作溶剂、清洗剂、除胶剂、调香剂、生物燃料[7] 和杀虫剂[8] 等。
可溶解發泡聚苯乙烯(保麗龍)。
初步科學臨床實驗數據顯示: D-檸檬烯補充劑或有助於正常的免疫功能及預防癌症等支持作用.
危险性
柠烯和其氧化产物(如被空气氧化生成的1,2-柠烯氧化物)对皮肤和呼吸道有刺激作用。
柠烯会在大鼠中引起肾细胞癌,但目前没有足够的证据证明它对人类有致癌性和基因毒性。在国际癌症研究机构的分类中,D-柠烯被列为第3类物质——尚不清楚其对人体致癌作用。[9] 而且某些研究者认为柠烯有潜在的抗癌功能,可以被用作功能性添加剂。[10][11]
注释
「薴烯」和「檸烯」都是常用的写法。简体的「
参考资料
内文参考资料
- Mann, J. C.; Hobbs, J. B.; Banthorpe, D. V.; Harborne, J. B. . Harlow, Essex, England: Longman Scientific & Technical. 1994: 308–309. ISBN 0-582-06009-5.
- J. L. Simonsen, The Terpenes Volume I (2nd edition), Cambridge University Press, 1947.
- H. Pakdela, D. Panteaa and C. Roy. . Journal of Analytical and Applied Pyrolysis. 2001, 57 (1): 91–107. doi:10.1016/S0165-2370(00)00136-4.
- Source: European Chemicals Bureau.
- Yuasa, Yoshifumi; Yoko Yuasa. . Org. Process Res. Dev. 2006, 10 (6): 1231 – 1232. doi:10.1021/op068012d.
- Fahlbusch, Karl-Georg; Franz-Josef Hammerschmidt, Johannes Panten, Wilhelm Pickenhagen, Dietmar Schatkowski, Kurt Bauer, Dorothea Garbe, Horst Surburg. . Wiley-VCH, Weinheim. 2002. doi:10.1002/14356007.a11_141.
- Cyclone Power to Showcase External Combustion Engine at SAE Event (页面存档备份,存于), Green Car Congress, 20 September 2007
- EPA R.E.D. Fact Sheet on Limonene (页面存档备份,存于), September 1994
- IARC Monographs on the evaluation of carcinogenic risks to humans 1999, 73-16, 307-27 (页面存档备份,存于)
- Crowell PL. . J. Nutr. 1999年3月, 129 (3): 775S–778S. PMID 10082788.
- Tsuda H, Ohshima Y, Nomoto H; et al. . Drug Metab. Pharmacokinet. 2004年8月, 19 (4): 245–63 [2009-05-02]. PMID 15499193. (原始内容存档于2009-01-13).
全文参考资料
- E. E. Turner, M. M. Harris, Organic Chemistry, Longmans, Green & Co., London, 1952.
- Wallach, Annalen der Chemie, 246, 221 (1888).
- Blumann & Zeitschel, Berichte, 47, 2623 (1914).
- Source: CSST Workplace Hazardous Materials Information System.
- M. Matura et al., J. Am. Acad. Dermatol. 2002, 33, 126-27.