铬酸
铬酸,化学式为H2CrO4,是三氧化铬溶于硫酸以及铬酸盐/重铬酸盐酸化时生成的化合物之一。重铬酸是二分子铬酸脱水形成的多酸,化学式为H2Cr2O7。三氧化铬是铬酸的酸酐,室温下为橘红色固体。由于它可通过加浓硫酸于铬酸盐或重铬酸盐的水溶液沉淀出来,故在工业上曾长期被称为“铬酸”。
| 铬酸 | |
|---|---|
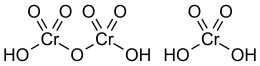 | |
| IUPAC名 Chromic(VI) acid | |
| 别名 | 铬(VI)酸 |
| 识别 | |
| CAS号 | 7738-94-5 |
| PubChem | 24425 |
| ChemSpider | 22834 |
| SMILES |
|
| InChI |
|
| InChIKey | KRVSOGSZCMJSLX-OOUCQFSRAZ |
| Gmelin | 25982 |
| EINECS | 231-801-5 |
| ChEBI | 33143 |
| 性质 | |
| 化学式 | H2CrO4 |
| 摩尔质量 | 118.01 g·mol−1 |
| 外观 | 红色晶体 |
| 密度 | 1.201 g cm-3 |
| 熔点 | 197 °C(470 K) |
| 沸点 | 250 °C(523 K)(分解) |
| 溶解性(水) | 1666.6 g dm-3 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
铬与同族的钼、钨不同,形成多酸的倾向不强,超过四铬酸以上的多铬酸很少见。这些化合物中都含有正六价铬,具有致癌性和氧化性,酸性溶液中的还原产物一般为紫色的[Cr(H2O)6]3+离子。
用途
铬酸洗液是实验室常用的清洗液,兼有酸性和氧化性,可以去除实验仪器内壁和外壁的污垢及难溶物质。通常该洗液由重铬酸钾加入浓硫酸中得到,但是六价铬对环境有害,强酸性环境有时也会使仪器受损,故目前铬酸洗液的应用已有减少。
铬酸也是镀铬涂层时的中间体,也用于某些釉和彩色玻璃的生产中。
反应
铬酸可以和碱成盐,根据pH的不同,酸根离子的形式也不同。重铬酸根(Cr2O72−)与铬酸根(CrO42−)离子在水溶液中存在以下平衡:
- 2 CrO42− + 2 H3O+ ⇌ Cr2O72− + 3 H2O
参考资料
- Freeman, F. "Chromic Acid" Encyclopedia of Reagents for Organic Synthesis (2001) John Wiley & Sons, doi:10.1002/047084289X.rc164
- Kamm O.; Matthews, A. O. (1941). "p-Nitrobenzoic Acid". Org. Synth.; Coll. Vol. 1: 392.
- Grummitt, O.; Egan, R.; Buck, A.. "Homophthalic Acid and Anhydride". Org. Synth.; Coll. Vol. 3: 449 (1955.
- Eisenbraun, E. J.. "Cyclooctanone". Org. Synth.; Coll. Vol. 5: 310 (1973.
- J. M. Grill, J. W. Ogle, S. A. Miller. . J. Org. Chem. 2006, 71 (25): 9291–9296. doi:10.1021/jo0612574.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.