锕系元素
锕系元素是第89号元素锕到103号元素铹共15种放射性元素的统称。锕系元素位於元素週期表第7週期的鐳與鑪之間,位於鑭系元素下方,但通常為了避免週期表形狀過寬影響觀看,而將鑭系和錒系元素移至週期表下方獨立列出。锕系元素可用符号An來表示。[1][2][3]
除了屬於d區的鐒之外,所有錒系元素都是f區元素,錒系元素原子基态的电子排布是5f0~146d0~27s2,其新增加的电子大多填入从外侧数進來的第三个电子层(即5f电子层)中,所以锕系元素又可以称为5f系,不過也有許多較輕的錒系元素將電子填入6d亞殼層。由于锕系元素都是金属,故可和镧系元素统称为f区金属。为了区别于周期表中的d区过渡元素,故又将锕系元素及镧系元素合称为内过渡元素。
由於較輕的錒系元素有許多電子填充不規則的情形,故它們的化合價有較多的變化,彼此之間的相似度從而沒有鑭系元素間來的高,其中釷、鏷和鈾的化學性質更類似於過渡金屬,錼和鈽則介於過渡金屬和鑭系元素之間。而較重的錒系元素則表現出和鑭系元素相似的性質,以+3價為最穩定的氧化態(鍩除外)。
1789年德国馬丁·克拉普羅特从沥青铀矿中发现铀,它是被人们认识的第一个锕系元素。其后陆续发现钍、锕和镤。铀以后的元素(即超鈾元素)都是在1940年后用人工核反应合成的,屬於人造元素。[1][4]不過也有部分超鈾元素最初是通過人工合成的方式發現,但是後來在自然界中,也發現有痕跡量的存在,包括錼和鈽[5]。
所有錒系元素都具有放射性,並在衰變時以游離輻射的形式釋放能量。天然存在的鈾和釷以及人工合成產生的鈽是目前地球上存量最豐富的錒系元素。鈾和鈽被廣泛用於核能發電及核武器,鈾和釷在當前及歷史上也有許多和放射性無關的用途,鋂則被用作大多數現代煙霧探測器的游離輻射源。
由於鐒在週期表中屬於d區,而其他錒系元素位於f區,因此有人認為鐒應該是過渡金屬而非錒系元素。[6][7]但為了方便敘述,現今仍習慣將其與錒系合稱。參見鑭系元素中關於鎦的地位的爭議,以及有關3族元素定義的爭論。
性質
| 元素名稱 | 錒 | 釷 | 鏷 | 鈾 | 錼 | 鈽 | 鋂 | 鋦 | 鉳 | 鉲 | 鑀 | 鐨 | 鍆 | 鍩 | 鐒 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 原子序 | 89 | 90 | 91 | 92 | 93 | 94 | 95 | 96 | 97 | 98 | 99 | 100 | 101 | 102 | 103 |
| 符號 | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr |
| 圖片 | .png.webp) |  |  |  |  |  | 無 | 無 | 無 | 無 | |||||
| 原子量 | [227] | 232.0377(4) | 231.03588(2) | 238.02891(3) | [237] | [244] | [243] | [247] | [247] | [251] | [252] | [257] | [258] | [259] | [266] |
| 天然同位素數量 | 3 | 7 | 3 | 8 | 3 | 4 | — | — | — | — | — | — | — | — | — |
| 最長壽同位素 | 227 | 232 | 231 | 238 | 237 | 244 | 243 | 247 | 247 | 251 | 252 | 257 | 258 | 259 | 266 |
| 最長壽同位素之半衰期 | 21.8年 | 140億年 | 32500年 | 44.7億年 | 214萬年 | 8080萬年 | 7370年 | 1560萬年 | 1380年 | 900年 | 1.29年 | 100.5天 | 52天 | 58分鐘 | 11小時 |
| 最常見同位素 | 227 | 232 | 231 | 238 | 237 | 239 | 241 | 244 | 249 | 252 | 253 | 255 | 256 | 255 | 260 |
| 最常見同位素之半衰期 | 21.8年 | 140億年 | 32500年 | 44.7億年 | 214萬年 | 24100年 | 433年 | 18.1年 | 320天 | 2.64年 | 20.47天 | 20.07小時 | 78分鐘 | 3.1分鐘 | 2.7分鐘 |
| 密度(g/cm3)[8] | 10.07 | 11.724 | 15.37 | 19.05 | 20.45 | 19.816 | 13.67 | 13.51 | 14.78 | 15.1 | 8.84 | ? 9.7 | ? 10.3 | ? 9.9 | ? 14.4 |
| 熔點(°C) | 1050 | 1842 | 1568 | 1132.2 | 639 | 639.4 | 1176 | 1340 | 986 | 900 | 860 | 1530 | 830 | 830 | 1630 |
| 沸點(°C) | 3198 | 4788 | 4027? | 4131 | 4174? | 3228 | 2607? | 3110 | 2627 | 1470? | 996? | — | — | — | — |
| 電子組態 (氣相) | 6d17s2 | 6d27s2 | 5f26d17s2 或 5f16d27s2 | 5f36d17s2 | 5f46d17s2 或 5f57s2 | 5f67s2 | 5f77s2 | 5f76d17s2 | 5f97s2 或 5f86d17s2 | 5f107s2 | 5f117s2 | 5f127s2 | 5f137s2 | 5f147s2 | 5f147s27p1 |
| 電子組態 (固相) | 6d17s2 | 5f0.56d1.57s2 | 5f1.76d1.37s2 | 5f2.96d1.17s2 | 5f46d17s2 | 5f56d17s2 | 5f66d17s2 | 5f76d17s2 | 5f86d17s2 | 5f96d17s2 | 5f117s2 | 5f127s2 | 5f137s2 | 5f147s2 | 5f146d17s2 |
| 金屬半徑(pm) | 203 | 180 | 162 | 153 | 150 | 162 | 173 | 174 | 170 | 186 | 186 | ? 198 | ? 194 | ? 197 | ? 171 |
錒系元素皆為银灰色有光泽的典型金屬[1][9][10][11],密度大,大多數質地较软,可塑性相對較高,其中一些可以用刀切割。[12]錒系元素皆具有順磁性及放射性。除錒之外,錒系元素都有多種晶相:鈽有七種,鈾、錼和鉲有三種。鏷、鈾、錼和鈽的晶體結構在鑭系元素中沒有明確的類似物,反而更類似於3d系過渡金屬。[13]
與鑭系元素一樣,錒系元素的原子半徑隨著原子序增加而逐漸縮小,稱作錒系收縮現象。
與鑭系元素相比,輕錒系元素(錒除外)之間的化合價非常多樣化,分別可以形成穩定的+4、+5或+6等價態,不像鑭系元素大多只有一個最穩定氧化態:+3,因此輕錒系元素彼此間的相似度沒有鑭系元素間來的高,從而較易分離。除錒之外的輕錒系元素中,釷、鏷和鈾的性質更類似於過渡金屬,錼和鈽則介於過渡金屬和鑭系元素之間。至於錒和鋂之後的重錒系元素則和鑭系元素一樣以+3價為最尋常、最穩定的氧化態(鍩除外),性質也和鑭系元素較為相似。
錒系元素的化學性質比較活潑,在空氣中表面會氧化失去光澤。能形成錯合物及可溶於水的氯化物、硫酸鹽、硝酸鹽及高氯酸鹽等,至於它們的氫氧化物、氟化物、硫酸鹽及草酸鹽等則不溶於水。
原子半径和离子半径(锕系收缩)
如同鑭系元素,锕系元素的原子半径和离子半径亦有随原子序数的增加而逐渐减小的现象,称为锕系收缩。
錒系元素中,充填最初幾個元素的5f電子時,離子半徑收縮地比較明顯,但此現象後來趨於平緩,使得這些較重的錒系元素的離子半徑十分接近。因此錒系元素在化學性質上的差別隨著原子序數的增大而逐漸變小,以致逐個地分離錒系元素(尤其是重錒系元素)越來越困難。
| 原子序数 | 元素名称 | +3离子半径(pm) | +4离子半径(pm) |
|---|---|---|---|
| 90 | 釷(Th) | 108 | 99 |
| 91 | 鏷(Pa) | 105 | 93 |
| 92 | 鈾(U) | 103 | 93 |
| 93 | 錼(Np) | 101 | 92 |
| 94 | 鈽(Pu) | 100 | 90 |
| 95 | 鋂(Am) | 99 | 89 |
| 96 | 鋦(Cm) | 98 | 88 |
| 97 | 鉳(Bk) | —— | —— |
| 98 | 鉲(Cf) | —— | —— |
| 99 | 鑀(Es) | —— | —— |
| 100 | 鐨(Fm) | —— | —— |
| 101 | 鍆(Md) | —— | —— |
| 102 | 鍩(No) | —— | —— |
| 103 | 鐒(Lr) | —— | —— |
离子的颜色
| 氧化態 | 錒 | 釷 | 鏷 | 鈾 | 錼 | 鈽 | 鋂 | 鋦 | 鉳 | 鉲 | 鑀 | 鐨 | 鍆 | 鍩 | 鐒 |
| +2 | Fm2+ | Md2+ | No2+ | ||||||||||||
| +3 | Ac3+ | Th3+ | Pa3+ | U3+ | Np3+ | Pu3+ | Am3+ | Cm3+ | Bk3+ | Cf3+ | Es3+ | Fm3+ | Md3+ | No3+ | Lr3+ |
| +4 | Th4+ | Pa4+ | U4+ | Np4+ | Pu4+ | Am4+ | Cm4+ | Bk4+ | Cf4+ | ||||||
| +5 | PaO+ 2 |
UO+ 2 |
NpO+ 2 |
PuO+ 2 |
AmO+ 2 |
||||||||||
| +6 | UO2+ 2 |
NpO2+ 2 |
PuO2+ 2 |
AmO2+ 2 |
|||||||||||
| +7 | NpO3+ 2 |
PuO3+ 2 |
AmO3− 5 |
 鈾的3、4、5、6價鹽的水溶液
鈾的3、4、5、6價鹽的水溶液 錼的3、4、5、6、7價鹽的水溶液
錼的3、4、5、6、7價鹽的水溶液 鈽的3、4、5、6、7價鹽的水溶液
鈽的3、4、5、6、7價鹽的水溶液
存在及合成
地殼中含量最豐富的錒系元素為釷和鈾,豐度分別為16ppm和4ppm。[15]它們兩者具有長半衰期的同位素,因此能在地殼中以穩定的量存在。主要的含鈾礦物有瀝青鈾礦、釩酸鉀鈾礦和鈣鈾雲母等,而釷主要分布在獨居石、方釷石和釷石等礦物中,大多數含釷礦物中皆含有鈾和大量的稀土元素。
鏷和錒主要在各種放射性礦物中作為釷和鈾的衰變產物生成,含量甚微,且錒的化學性質與礦石中的鑭系元素(尤其是鑭)甚為相似而難以提取、分離,因此兩者通常是從用過核燃料中提煉,或在核反應爐中人工合成。[16]
超鈾元素大多不存在於自然界中,必須透過核反應爐或粒子加速器人工合成,只有部分較輕的元素如錼和鈽等以痕量存在於鈾礦中,是鈾的核嬗變產物。[17][18]自二戰以來的多次核武器試驗已將至少六種比鈽重的人造超鈾元素釋放到環境中,包括鋂、鋦、鉳、鉲、鑀和鐨。[19]
用途
錒系元素的主要用途是核能發電及核武器,例如鈾和鈽等。不過也有部分錒系元素在日常生活中得到了應用,例如游離煙霧探測器中的鋂[20][21]和煤氣燈網罩中的釷等[22]。至於原子序較大的重錒系元素由於製備的難度較高,且較不穩定,因此只用於學術研究,而沒有實際用途。
核能應用中最重要的同位素是铀-235,用於熱中子反應爐。天然铀里铀-235的占比僅為0.72%。它會强烈吸收热中子,然后放出大量能量。铀-235核子吸收中子后,会裂变成2个较轻的核子和2至3颗中子,如:
1克235U的一次裂变行为转换为大约1MW/天。重要的是,235
92U
发射的中子多于吸收的中子;[23] 达到临界质量时,235
92U
进入自动链锁反应。[13]
| Nuclear reactor[13][24][25] |
The core of most Generation II nuclear reactors contains a set of hollow metal rods, usually made of zirconium alloys, filled with solid nuclear fuel pellets – mostly oxide, carbide, nitride or monosulfide of uranium, plutonium or thorium, or their mixture (the so-called MOX fuel). The most common fuel is oxide of uranium-235.
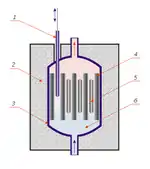 Nuclear reactor scheme Fast neutrons are slowed by moderators, which contain water, carbon, deuterium, or beryllium, as thermal neutrons to increase the efficiency of their interaction with uranium-235. The rate of nuclear reaction is controlled by introducing additional rods made of boron or cadmium or a liquid absorbent, usually boric acid. Reactors for plutonium production are called breeder reactor or breeders; they have a different design and use fast neutrons. |
釷除了用作煤氣網罩的材料之外[22],也常和鎂、鋁等金屬做成合金,因為鎂釷合金不但堅固,還具有高熔點及高延展性,因此被廣泛用於航空工業和導彈的生產中。釷還有著良好的電子發射性能,可用作電子器件中的高效電子發射極。此外釷的半衰期很長[23],和鈾同位素的相對含量被廣泛用於估算包括恆星在內的各種物體的年齡(參見放射性定年法)。[26]
钚元素的主要用途是制造核武器,尤其是可以裂变的钚-239。它的临界质量是铀-235的1/3。[27]
Plutonium-238 is potentially more efficient isotope for nuclear reactors, since it has smaller critical mass than uranium-235, but it continues to release much thermal energy (0.56 W/g)[21][30] by decay even when the fission chain reaction is stopped by control rods. Its application is limited by the high price (about US$1000/g). This isotope has been used in thermopiles and water distillation systems of some space satellites and stations. So Galileo and Apollo spacecraft (e.g. Apollo 14[31]) had heaters powered by kilogram quantities of plutonium-238 oxide; this heat is also transformed into electricity with thermopiles. The decay of plutonium-238 produces relatively harmless alpha particles and is not accompanied by gamma-irradiation. Therefore, this isotope (~160 mg) is used as the energy source in heart pacemakers where it lasts about 5 times longer than conventional batteries.[21]
锕-227被用作中子源。 Its high specific energy (14.5 W/g) and the possibility of obtaining significant quantities of thermally stable compounds are attractive for use in long-lasting thermoelectric generators for remote use. 228Ac is used as an indicator of radioactivity in chemical research, as it emits high-energy electrons (2.18 MeV) that can be easily detected. 228Ac-228Ra mixtures are widely used as an intense gamma-source in industry and medicine.[16]具有耐用晶体基质的自发光锕系元素掺杂材料的开发是锕系元素利用的一个新领域,因为向某些玻璃和晶体中添加α发射放射性核素可能会赋予发光性。[32]
對生物的影響
目前沒有發現錒系元素在生物體中發揮任何生物學作用。由於錒系元素皆具有放射性,其衰變時釋放的游離輻射會破壞生物組織,過度暴露在輻射中會導致輻射中毒,故對生物而言具有極高的毒性。因此含有錒系元素的核廢料的處置是一個至關重要的課題。[32]
参考文献
- Theodore Gray. . New York: Black Dog & Leventhal Publishers. 2009: 240. ISBN 978-1-57912-814-2.
- Morss, Lester; Asprey, Larned B. . britannica.com. Encyclopædia Britannica. 1 August 2018 [3 September 2020]. (原始内容存档于2015-04-29).
- Neil G. Connelly; et al. . . London: Royal Society of Chemistry. 2005: 52. ISBN 978-0-85404-438-2.
- Greenwood, p. 1250
- Jensen, William B. . Foundations of Chemistry. 2015-04-01, 17 (1). ISSN 1572-8463. doi:10.1007/s10698-015-9216-1 (英语).
- Jensen, William B. . Foundations of Chemistry. 2015, 17: 23–31 [28 January 2021]. S2CID 98624395. doi:10.1007/s10698-015-9216-1. (原始内容存档于16 August 2021).
-
Scerri, Eric. . Chemistry International. 18 January 2021, 43 (1): 31–34. S2CID 231694898. doi:10.1515/ci-2021-0115
 .
. - . [2019-12-15]. (原始内容存档于2019-04-04).
- Actinide element (页面存档备份,存于), Encyclopædia Britannica on-line
- Although "actinoid"(rather than "actinide")means "actinium-like" and therefore should exclude actinium, that element is usually included in the series.
- Neil G. Connelly; et al. . . London: Royal Society of Chemistry. 2005: 52 [2014-03-31]. ISBN 0-85404-438-8. (原始内容存档于2014-01-01).
- Greenwood, p. 1264
- Yu.D. Tretyakov (编). . Chemistry of transition elements 3. Moscow: Academy. 2007. ISBN 978-5-7695-2533-9.
- Greenwood, p. 1265
- Jay H. Lehr; Janet K. Lehr. . McGraw-Hill Professional. 2000: 2–38. ISBN 978-0-07-038309-8.
- Z. K. Karalova; B. Myasoedov. . Analytical chemistry items. Moscow: Nauka. 1982.
- V.A. Mikhailov (编). . Moscow: Nauka. 1971.
- F. Weigel; J. Katz; G. Seaborg. 2. Moscow: Mir. 1997. ISBN 978-5-03-001885-0.
- Fields, P.; Studier, M.; Diamond, H.; Mech, J.; Inghram, M.; Pyle, G.; Stevens, C.; Fried, S.; Manning, W.; et al. . Physical Review. 1956, 102 (1): 180–182. Bibcode:1956PhRv..102..180F. doi:10.1103/PhysRev.102.180.
- Smoke Detectors and Americium, Nuclear Issues Briefing Paper 35, May 2002
- Greenwood, p. 1262
- Greenwood, p. 1255
- Golub, pp. 220–221
- G. G. Bartolomei; V. D. Baybakov; M. S. Alkhutov; G. A. Bach. . Moscow: Energoatomizdat. 1982.
- Greenwood, pp. 1256–1261
- Sergey Popov; Alexander Sergeev. . Vokrug Sveta. 2008, 2811 (4) [2019-10-15]. (原始内容存档于2019-10-21) (俄语).
- David L. Heiserman. . . New York: TAB Books. 1992: 338. ISBN 978-0-8306-3018-9.
- John Malik. (PDF). Los Alamos. September 1985: Table VI [15 February 2009]. LA-8819. (原始内容存档 (PDF)于24 February 2009).
- FAS contributors. . Federation of American Scientists. 1998 [7 December 2008]. (原始内容存档于26 December 2008).
- John Holdren and Matthew Bunn Nuclear Weapons Design & Materials. Project on Managing the Atom (MTA) for NTI. 25 November 2002
- Apollo 14 Press Kit – 01/11/71 (页面存档备份,存于), NASA, pp. 38–39
- B.E. Burakov; M.I Ojovan; W.E. Lee. . World Scientific. 2010 [2019-10-15]. ISBN 978-1848164185. (原始内容存档于2020-03-17).