X
这篇文章的共同创作者是 Meredith Juncker, PhD. Meredith Juncker是美国路易斯安那州立大学健康科学中心的生物化学与分子生物学博士研究生。蛋白质与神经退行性疾病是她主攻的研究方向。
本文引用了8条参考,详情参见页面底部。
这篇文章已经被读过10,938次。
用烘烤饼干的过程来思考化学反应是一种好方法。把配料(面粉、黄油、盐、糖和鸡蛋)混合在一起,烘烤后就会得到新的东西:饼干!用化学术语来说,配方相当于反应式,配料是“反应物”,饼干就是“产物”。所有的化学反应式都类似于“A + B→C (+ D…)”,其中每个字母变量都是一个元素或一个分子(由化学键结合在一起的原子集合)。箭头表示发生的反应或变化。有些反应式可能有一个双向箭头(↔),这表明反应式既可以正向也可以逆向反应。要写出这些反应式,你得弄清一些重要的命名规则。
步骤
部分 1
部分 1 的 3:
写出共价化合物的化学式
-
写出第一个元素的化学符号。当给出一种化合物时,你必须弄清它的元素并知道它们的化学符号。第一个元素相当于化合物的“名”。可以使用元素周期表来查找元素的化学符号。[3]
- 例如:六氟化二氮。第一个元素是氮,氮的化学符号是N。
-
用下标表示原子个数。要确定每个元素的原子数,只需查看元素的前缀。记住希腊前缀可以帮助你在不用如何查询就能快速写出化学式。[4]
- 例如:双氮有一个前缀“di-”,意思是2;因此,这里有2个氮原子。
- 将双氮写成N2。
-
写出第二个元素的化学符号。第二个元素相当于这个化合物的“姓”,并在第一个元素后面。对于共价化合物,元素名称将以“-ide”为后缀,而不是元素的正常结尾。[5]
- 例如:六氟化二氮。第二个元素是氟。只需将“ide”结尾替换为实际的元素名称。氟的化学符号是F。
-
用下标表示原子个数。和第一个元素一样,通过看前缀来标识第二个元素中原子数。使用这个前缀,将原子数作为下标写在化学符号右侧。[6]
- 例如:六氟化物的前缀是“hexa-”,表示6;所以氟原子有6个。
- 将六氟化物写成F6。
- 六氟化二氮的最终化学式为N2F6。
-
通过一些例子来练习。第一次学化学时,需要大量的记忆工作。这有点像学习一门新的语言。你练习得越多,以后理解化学式和学习化学语言也就越容易。
- 二氧化硫:SO2
- 四溴化碳:CBr4
- 五氧化二磷:P2O5
广告
部分 2
部分 2 的 3:
写出离子化合物的化学式
-
认识阳离子和阴离子的化学符号。所有化学物质都有“姓名”。阳离子(正离子)相当于名字,而阴离子(负离子)相当于姓。阳离子被写为元素名,而阴离子是以“ide”结尾的元素名。[7]
- 在元素周期表上可以找到每种元素的化学符号。
- 与共价化合物不同,希腊语前缀不用于表示每种元素的原子数。你必须平衡元素的电荷来确定原子。
- 例如:氧化锂是Li2O。
-
找出多原子离子。有时阳离子或阴离子是多原子离子。这些分子有两个或两个以上带离子基的原子。记住这些知识没有什么好的技巧,你只用记住它们就行了。[8]
- 正盐酸根离子有三种,分别是氨盐基(NH4+)、水合氢离子(H3+)和汞(I)(Hg22+)。它们都带有1个正电荷(不过,严格来说,每个汞正离子都带1个正电荷,所以2个汞原子结合在一起,产生了2个正电荷)。
- 其余多原子离子的负电荷从-1到-4不等。一些常见的例子包括碳酸盐(CO32-)、硫酸盐(SO42-)、硝酸盐(NO3-)和铬酸盐(CrO42-)。
-
确定每个元素的化合价。化合价可以通过观察元素在周期表上的位置来确定。这里有一些规则可以帮助你确定化合价:[9]
- 所有1族元素化合价为+1。
- 所有2族元素化合价为+2。
- 过渡元素在括号中有罗马数字表示化合价。
- 银+1、锌+2、铝+3。
- 17族元素化合价为1-。
- 16族元素化合价为2-。
- 15族元素化合价为3-。
- 记住,在处理多原子离子时,要计算所有多原子离子的电荷,而不是单个离子的电荷。
-
平衡离子的正电荷和负电荷。当你确定了每个元素(或多原子离子)的电荷后,你将使用这些电荷来确定每个元素的原子数。你需要让化合物的正负电荷总和等于零,所以要加入原子来平衡电荷。[10]
- 例如:氧化锂。锂是1族元素,化合价为+1。氧是16族元素,化合价为2-。为了平衡氧的2-电荷,你需要2个锂原子;因此,氧化锂的化学式为Li2O。
-
通过一些例子来练习。学习化学式的最好方法是通过大量的例子来练习。在你的化学课本里找例子,或者在网上找练习集。尽量多练习,直到你彻底熟悉化学式的书写为止。
- 氮化钙:钙的符号是Ca,氮的符号是N。Ca是第2族元素,化合价为+2。氮是15族元素,化合价为-3。为了达到平衡,你需要3个钙原子(6+)和2个氮原子(6-):Ca3N2。
- 汞(II)磷酸盐:汞的符号为Hg,磷酸盐为多原子离子PO4。汞的化合价为2+,由旁边的罗马数字II表示。磷酸盐带3个负电荷。为了平衡它们,你需要3个汞原子(6+)和2个磷酸盐分子(6-):Hg3(PO4)2.
广告
部分 3
部分 3 的 3:
确定给定反应物的生成物
-
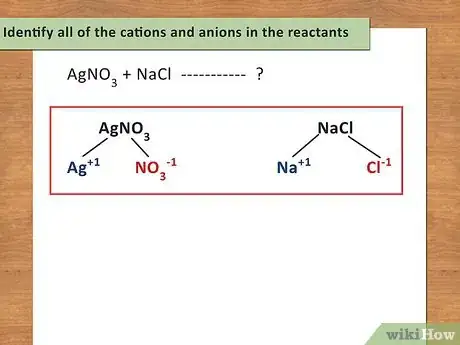
确定反应物中所有的正离子和负离子。在一个基本的双置换反应式中有2个阳离子和2个阴离子。一般反应式为AB + CD → AD + CB,其中A、C为阳离子,B、D为阴离子。你还需要确定每个离子的电荷。[11]
- 例如:AgNO3 + NaCl → ?
- 阳离子为Ag+1和Na+1。阴离子为NO31-和Cl1-。
-
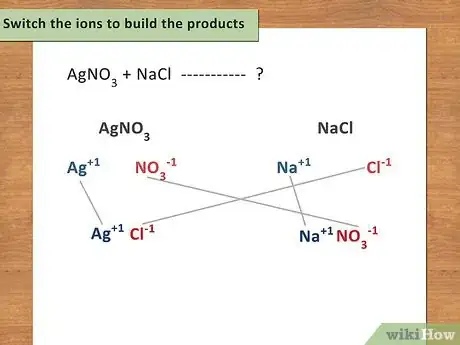
交换离子形成生成物。确定了所有离子和它们的电荷后,重新排列它们,这样第一个正离子和第二个负离子配对,第二个正离子和第一个负离子配对。记住这个反应式:AB + CD → AD + CB。[12]
- 形成新化合物时要记得平衡电荷。
- 例如:AgNO3 + NaCl → ?
- Ag+1和Cl1-配对形成AgCl。
- Na+1和NO31-配对形成NaNO3。
-
写出完整的反应式。写出反应式中形成的生成物之后,你就可以写出同时带有生成物和反应物的反应式了。反应物写在反应式左边,新的生成物写在反应式右边,中间有一个加号。[13]
- 例如:AgNO3 + NaCl --> ?
- AgNO3 + NaCl --> AgCl + NaNO3
-
5标注物质的状态。标出反应物和生成物的状态是很重要的。每一种物质状态都对应一个指定的字母,并放在括号里。把这个信息标注在相应的物质分子式后面。[15]
- 用“(g)”表示气体,用“(s)”表示固体,用“(l)”表示液体,用“(aq)”表示溶解在水中的物质。
-
通过一些例子来练习。要想更熟练地写出化学反应式,唯一的方法就是去练习。通过这些例子来确保你真正理解这个过程。
- NiCl2 + (NH4)2S → ?
- 阳离子:Ni2+和NH4+
- 阴离子:Cl1-和S2-
- 重组离子形成新的生成物:NiS + NH4Cl
- 写出反应式:NiCl2 + (NH4)2S → NiS + NH4Cl
- 配平反应式:NiCl2 + (NH4)2S → NiS + 2NH4Cl
广告
小提示
- 把系数放在离子前面,而不是作为下标来添加,因为这样会改变分子式。
广告
参考
- ↑ https://chem.libretexts.org/Textbook_Maps/Introductory_Chemistry/Book%3A_The_Basics_of_GOB_Chemistry_(Ball_et_al.)/04%3A_Covalent_Bonding_and_Simple_Molecular_Compounds/4.2%3A_Covalent_Compounds%3A_Formulas_and_Names
- ↑ http://www.kentchemistry.com/links/naming/NameCov.htm
- ↑ http://www.kentchemistry.com/links/naming/NameCov.htm
- ↑ http://www.kentchemistry.com/links/naming/NameCov.htm
- ↑ http://www.kentchemistry.com/links/naming/NameCov.htm
- ↑ http://www.kentchemistry.com/links/naming/NameCov.htm
- ↑ http://www.kentchemistry.com/links/naming/BinaryIonic.htm
- ↑ http://www.kentchemistry.com/links/naming/PolyatomicIonsB.htm
- ↑ http://www.kentchemistry.com/links/naming/formulawriting.htm
- ↑ http://www.kentchemistry.com/links/naming/formulawriting.htm
- ↑ http://www.chemteam.info/Equations/DoubleReplacement.html
- ↑ http://antoine.frostburg.edu/chem/senese/101/reactions/faq/predicting-products-nicl2-nh42s.shtml
- ↑ http://antoine.frostburg.edu/chem/senese/101/reactions/faq/predicting-products-nicl2-nh42s.shtml
- ↑ http://antoine.frostburg.edu/chem/senese/101/reactions/faq/predicting-products-nicl2-nh42s.shtml
- ↑ https://sciencenotes.org/guidelines-for-balancing-chemical-equations/
关于本wikiHow
广告