三硝基甲烷
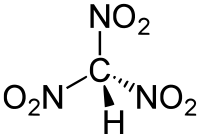
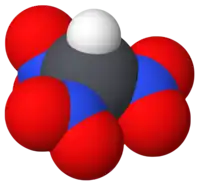
三硝基甲烷,又称硝仿,是一种硝基化合物,也是一种氧化剂,化学式HC(NO2)3。在1857年,俄罗斯化学家Leon Nikolaevich Shishkov(1830-1908)成功制备了三硝基甲烷的铵盐。[2][3]在1900年的时候,他发现了三硝基甲烷可以由乙炔和硝酸一起化合而成。[4]这种方法成为了20世纪三硝基甲烷的主要制备方法。在实验室里,三硝基甲烷可以由四硝基甲烷在弱碱性环境中水解而成。[5]
| 三硝基甲烷[1] | |
|---|---|
 | |
 | |
| IUPAC名 Trinitromethane | |
| 别名 | 硝仿 |
| 识别 | |
| CAS号 | 517-25-9 |
| ChemSpider | 10157 |
| SMILES |
|
| InChI |
|
| 性质 | |
| 化学式 | CHN3O6 |
| 151.04 g/mol g·mol⁻¹ | |
| 外观 | 淡黄色晶体 |
| 密度 | 1.469 g/cm3 |
| 熔点 | 15 °C(288 K) |
| 溶解性(水) | 44g/100ml at 20 °C |
| pKa | 0.25 (见下文) |
| 危险性 | |
| 主要危害 | 氧化性,爆炸性,腐蚀性 |
| NFPA 704 |
 1
3
4
|
| 相关物质 | |
| 相关化学品 | 六硝基乙烷 八硝基戊烷 四硝基甲烷 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
三硝基甲烷盐
三硝基甲烷会形成黄色的盐。大部分的三硝基甲烷盐都对热不稳定。
三硝基甲烷的钾盐 KC(NO2)3 是一种柠檬黄色的晶体,会缓慢分解,在 95 °C以上会爆炸。它的铵盐比较稳定, 200 °C才会猛烈分解或爆炸。[8]
参考资料
- Budavari, Susan (编), 12th, Merck, 1996, ISBN 0911910123, 9859.
- For biographical information about Leon Nikolaevich Shishkov, see The Free Dictionary (页面存档备份,存于)
- See:
- Chichkoff, Léon. [Note on nitroform]. Comptes rendus. 1857, 45: 144–146 [2020-06-26]. (原始内容存档于2020-07-25) (法语).
- Schischkoff, L. [On nitroform]. Annalen der Chemie. 1857, 103 (3): 364–366 [2020-06-26]. doi:10.1002/jlac.18571030316. (原始内容存档于2020-07-02) (德语).
- Abstracted in: Schischkoff, L. . The Chemical Gazette. 1857, 15: 448 [2020-06-26]. (原始内容存档于2020-07-30).
- Abstracted in: Schischkoff, L. . Philosophical Magazine. 4th series. 1858, 15: 302 [2020-06-26]. (原始内容存档于2020-08-03).
- The Italian chemist Adolfo Baschieri discovered that nitroform (Italian: nitroformio) could be produced from acetylene (acetilene) and nitric acid (acido nitrico).
- Baschieri, A. [On the behavior of acetylene with some oxidizers]. Atti della Reale Accademia dei Lincei. 5th series. 1900,. 9 (part I): 391–393 [2020-06-26]. (原始内容存档于2020-06-27) (意大利语). See p. 392.
- Abstracted in German in: Baschieri, A. [On the behavior of acetylene towards some oxidizers]. Chemisches Central-blatt. 5th series. 1900,. 4 (part II): 528 [2020-06-26]. (原始内容存档于2020-07-01) (德语).
- See also: Nieuwland, Julius A.; Vogt, Richard R. . New York City, New York, USA: Reinhold Publishing Corp. 1945: 158.
- Gakh, A. A.; Bryan, J. C.; Burnett, M. N.; Bonnesen, P. V. (PDF). Journal of Molecular Structure. 2000, 520 (1–3): 221–228 [2020-06-26]. doi:10.1016/S0022-2860(99)00333-6. (原始内容存档 (PDF)于2018-07-19).
- Novikov, S. S.; Slovetskii, V. I.; Shevelev, S. A.; Fainzilberg, A. A. . Russian Chemical Bulletin. 1962, 11 (4): 552–559. doi:10.1007/BF00904751.
- Cioslowski, J.; Mixon, S. T.; Fleischmann, E. D. . Journal of the American Chemical Society. 1991, 113 (13): 4751–4755. doi:10.1021/ja00013a007.
- . sites.google.com. [2020-07-04]. (原始内容存档于2016-10-07).
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.