二氧化碲
二氧化碲化学式TeO2,是一种白色固体,加热变黄。其有两种晶型,无色四面体结晶的副黄碲矿是四方晶系的α-TeO2,黄色的单斜矿石黄碲矿是β-TeO2。[2]对于二氧化碲性质的研究多基于α-TeO2。[3]
| 二氧化碲 | |
|---|---|
 | |
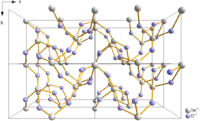 | |
| 别名 | Tellurium(IV) oxide |
| 识别 | |
| CAS号 | 7446-07-3 |
| PubChem | 62638 |
| ChemSpider | 56390 |
| SMILES |
|
| InChI |
|
| InChIKey | LAJZODKXOMJMPK-UHFFFAOYAO |
| 性质 | |
| 化学式 | TeO2 |
| 159.60 g·mol⁻¹ | |
| 外观 | 白色固体,732°C时变成红色液体 |
| 密度 | 5.670 g/cm3 (四方晶系) 6.04 g/cm3 (正交晶系) [1] |
| 熔点 | 732 °C |
| 沸点 | 1245 °C |
| 溶解性(水) | 微溶 |
| 溶解性 | 溶于酸碱 |
| 折光度n D |
2.24 |
| 危险性 | |
| 欧盟编号 | Not listed |
| 闪点 | 不燃 |
| 相关物质 | |
| 其他阳离子 | 二氧化硫 二氧化硒 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
应用
二氧化碲应用于声光器件。由于α-TeO2具有双折射性和旋光特性,旋光度为87°/mm,沿<110>方向传播的声速仅为616m/s,所以是一种高品质的声光材料。二氧化碲用于制造特殊性能的玻璃。碲玻璃具有高折射率,能穿透中红外波段的电磁波。[4]
参考资料
- Pradyot Patnaik. . McGraw-Hill. 2002. ISBN 0-07-049439-8.
- Greenwood, Norman N.; Earnshaw, A. . Oxford: Pergamon. 1984: 911. ISBN 0-08-022057-6.
- W.R.McWhinnie (1995) Tellurium - Inorganic chemistry Encyclopedia of Inorganic Chemistry Ed. R. Bruce King (1994) John Wiley & Sons ISBN 978-0-471-93620-6
- Stegeman R, Jankovic L, Kim H, Rivero C, Stegeman G, Richardson K, Delfyett P, Guo Y, Schulte A, Cardinal T. . Optics Letters. 2003, 28 (13): 1126–8. PMID 12879929. doi:10.1364/OL.28.001126.
- Perez-D'Gregorio RE, Miller RK, Baggs RB. . Reprod. Toxicol. 1988, 2 (1): 55–61. PMID 2980402. doi:10.1016/S0890-6238(88)80009-1.
- Atta-ur-Rahman. . Elsevier. 2008: 905. ISBN 0-444-53181-5.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.