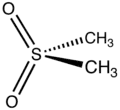
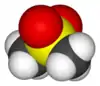
二甲基砜
二甲基砜(Methylsulfonylmethane),簡稱為有機硫 (MSM)其化學式為(CH3)2SO2、甲基硫醯基甲烷的碸類有機化合物[1]。二甲基砜在常溫下是無色固體,無化學活性。在一些植物中含有二甲基砜,也出現在許多的食品及飲料中,會稱為膳食補充劑。在海面上方的大氣中也會有二甲基砜,是空氣中慢生根瘤菌科細菌、阿菲波菌(Afipia)的碳的來源[2],也曾在人體的黑色素瘤细胞发现過[3]。二甲基砜的外觀和物理性質與甲基安非他命類似,因此常被不法份子拿來摻入甲基安非他命以提高利潤[4]
| 二甲基碸 | |||
|---|---|---|---|
| |||
| IUPAC名 dimethyl sulfone | |||
| 别名 | methyl sulfone methylsulfonylmethane sulfonylbismethane DMSO2 | ||
| 识别 | |||
| CAS号 | 67-71-0 | ||
| PubChem | 6213 | ||
| ChemSpider | 5978 | ||
| SMILES |
| ||
| InChI |
| ||
| InChIKey | HHVIBTZHLRERCL-UHFFFAOYAG | ||
| ChEBI | 9349 | ||
| RTECS | PB2785000 | ||
| KEGG | C11142 | ||
| 性质 | |||
| 化学式 | C2H6O2S | ||
| 摩尔质量 | 94.13 g·mol−1 | ||
| 外观 | White crystalline solid | ||
| 密度 | 1.45 g/cm3 | ||
| 熔点 | 109 °C(382 K) | ||
| 沸点 | 248 °C(521 K) | ||
| 危险性 | |||
| 安全术语 | S:S22 S24/25 | ||
| NFPA 704 |
 1
1
0
| ||
| 相关物质 | |||
| 相关化学品 | 二甲基亞碸 二甲硫醚 硫酸二甲酯 环丁砜 | ||
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |||
結構和化學性質
二甲基碸和相應的二甲基亞砜具有不同的物理性質。 二甲基碸在標準溫度與標準壓力下為白色結晶固體(熔點=109℃),而二甲基亞砜是在標準條件下為液體。亞砜是高度極性非質子溶劑,可與水混溶;這也是一個很好的配體。二甲基碸比二甲基亞砜反應性較低,因為砜的硫原子已經在其最高氧化狀態。事實上亞砜氧化產生砜,既可在實驗室條件下也可在新陳代謝中。
合成
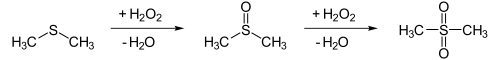
二甲基砜可以通過與過氧化氫,二甲基硫的氧化來製備。 二甲基亞砜可作為(可分離)中間體。
藥理和毒性
二甲基碸的半數致死劑量大於每公斤體重17.5克。在大鼠中,每日劑量每公斤體重2克的二甲基碸沒有觀察到不良反應。在90天的後續研究中,大鼠接受每天服用二甲基碸1.5克/公斤,而在症狀,血液化學或大體病理方面沒有觀察到變化。核磁共振研究表明,口服劑量的二甲基碸被吸收到血液中,並穿過血/腦屏障。核磁共振研究也發現的二甲基碸檢測水平通常存在於血液和腦脊髓液,這表明它從膳食來源,腸道細菌的代謝,與人體的內源性甲烷硫醇代謝獲得。二甲基碸發表的臨床試驗報告沒有任何嚴重的副作用,但其在人類長期使用的效果也沒有同行評議的數據。
醫療和膳食用
雖然沒有任何政府已通過二甲基碸的醫療用途,都聲稱和研究其對各種健康益處。斯坦利.雅各報告超過18,000名患者因各種病痛服用二甲基碸;他合著了推動二甲基碸的多種說法的書,包括具一個可用作天然來源「生物活性硫」表明在他們的飲食攝取中對這種形式的硫是缺乏的。硫沒有建立膳食參考攝入量或每日攝入量和現成的足夠的食物來源,在洋蔥,大蒜,十字花科蔬菜和含蛋白質的食物,包括堅果,種子,牛奶和雞蛋(蛋白和蛋黃)。
1982年羅伯特赫希勒首先主張需要補充硫,他聲稱二甲基碸在壓力,粘液膜的炎症,過敏和胃腸道疾病是有益的。作為膳食補充劑二甲基碸常與葡糖胺和/或軟骨素一起出售,為幫助治療或預防骨關節炎。
赫希勒說明一般飲食中缺乏二甲基碸是因為它在傳統的食品加工過程中容易丟失,如油炸,脫水,和其它不良的方式,烹飪,輻射或巴氏殺菌,以及長期的存儲。
氧化應激和炎症
多種人類和動物試驗表明二甲基碸可以降低氧化應激和炎症反應,儘管它不是直接的抗氧化劑。在人類研究中二甲基碸已經顯示出從減少氧化應激損傷發生數保護肌肉因運動而受損害。總之抗氧化能力在服用二甲基碸後顯著增加。動物研究表明二甲基碸對幾種毒素,包括對乙酰氨基酚,百草枯,和四氯化碳二甲基碸有保肝作用。以及在實驗性結腸炎中和肺動脈高壓的動物模型中表明有保護作用。
參考資料
- (PDF). [June 8, 2009]. (原始内容 (PDF)存档于2011年7月11日).
- Natasha DeLeon-Rodriguez, others (full list). (PDF): 5. December 19, 2012 (received for review July 15, 2012) [2014-03-01] (英语).
This group [Afipia] is commonly found in aquatic environments and is known to use dimethyl sulfone (DMSO2) as a sole carbon source. DMSO2 represents an intermediate of the oxidation of dimethyl sulfide (DMS), which is commonly found in the marine atmosphere
- . Institute for Electrical and Electronic Engineers. 2013-12-20 [2014-05-19]. (原始内容存档于2016-10-06) (英语).
- . www.justice.gov. [20 January 2018]. (原始内容存档于2020-12-08).