奈瑪特韋/利托那韋
奈瑪特韋/利托那韋(Nirmatrelvir/ritonavir,NMV/r[14],NMV-r[15]),英文商品名:Paxlovid[16],中文商品名()[17],坊間亦稱為辉瑞新冠口服药[18]、輝瑞口服藥、輝瑞特效藥[19]、辉瑞神药[20]、P药[21]等,這是一款由美國辉瑞公司研發的雙成分抗病毒口服藥[22][23][24],由奈瑪特韋及利托那韋組成[25],該複方藥品之中文名:帕昔洛韋[26]。此小分子口服藥专门治疗由嚴重急性呼吸系統綜合症冠狀病毒2型所引起的2019冠状病毒病(COVID-19)[22][27]。
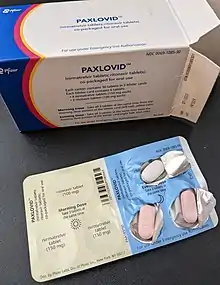 帕昔洛韋(Paxlovid)包裝內的藥片組合 | |
| 组成 | |
|---|---|
| 奈瑪特韋 | 抗病毒藥物 |
| 利托那韋 | 抗病毒藥物 |
| 臨床資料 | |
| 商品名 | 英文:Paxlovid 中文: |
| AHFS/Drugs.com | Monograph |
| MedlinePlus | a622005 |
| 核准狀況 | |
| 懷孕分級 | |
| 给药途径 | 口服 |
| 法律規範狀態 | |
| 法律規範 | |
| 识别 | |
| KEGG | |
| 「奈瑪特韋/利托那韋」的各地常用名稱 | |
|---|---|
| 中国大陸 | |
| 臺灣 | |
| 港澳 | |
概要
該口服藥由兩種藥片組成,採用鋁箔泡殼共同封裝,機制皆屬蛋白酶抑制剂,但作用蛋白酶不同:奈瑪特韋能夠阻斷病毒的複製,而利托那韋則作為前者的輔助劑、減慢奈瑪特韋在肝臟被分解及代謝的速度,以維持前者在血漿中的濃度,使其可更長時間發揮抑制病毒的效用[28][29]。
美國國家衛生院的資料顯示輝瑞於2021年7月提交第2/3期臨床試驗的申請[30],於2021年9月開始第3期臨床試驗。輝瑞於2021年11月5日發布第3期臨床試驗的結果[31]。2021年12月22日,美國食品藥物管理局發出輝瑞口服藥Paxlovid的緊急使用授權[32]。
医用信息
服用方式與禁忌症
受到新冠病毒感染的患者在出現病徵的5天內,並且在未發生呼吸衰竭及血含氧量不低於94%時儘早服用帕克斯洛維德[33][34],將可大幅減少病情惡化為重症的機會,臨床試驗顯示可降低患者的入院率及死亡率達到85至89%[35]。
該種口服藥的每次療程為5天,每劑口服藥由2片150毫克奈瑪特韋藥片及1片100毫克利托那韋藥片組成[36],每盒帕克斯洛維德的包裝內裝有20片奈瑪特韋及10片利托那韋,合共30片藥品。患者在5天療程內的每天早上及晚間各服用1次,鋁箔泡殼有黃色與藍色區域,白天需服用印有太陽符號的黃色區域,晚間服用印有月亮符號的藍色區域,每次都要完整服用2片奈瑪特韋藥片及1片利托那韋藥片,共3顆藥片。該藥物適合12歲或以上的患者,但腎功能或肝功能非常差的人士則不適合服用,副作用包括肚瀉、輕微的血壓高或肌肉痛[37]。
药物交互作用
由于利托那韋是CYP3A的抑制剂[38][39],可能会增加经由此酶代谢的其他药物血浆浓度,因此奈瑪特韋/利托那韋複方药剂会与其他35类药物交互作用[40],使用时必须注意其他药物血中浓度及可能副作用。
世衛組織建議
2022年4月22日,世衛組織發表聲明強烈建議將輝瑞製藥的帕克斯洛維德給予高風險患者服用[41]。世衛組織分析兩場共有近3100名患者參與的臨床試驗後,帕克斯洛維德能減少85%的住院風險,對於住院風險大於10%的高風險患者,可讓每1000名患者減少84人住院治療[42];對於未接種疫苗、年長者或免疫功能低的患者,儘早服用帕克斯洛維德是迄今最佳的治療方案[43]。
真实世界有效率
美國麻薩諸塞州布萊根婦女醫院於2022年1月1日至2022年7月17日、美國疾病管制與預防中心於2022年4月1日至8月31日,分別進行病例的追查及分析,結果顯示该药在50岁以上或有基础病的高危病人早期治疗中对于防止病重住院的保护率大约为50%。有限数据显示死亡率减少大约 71%至75%[44][45]。
香港大學李嘉誠醫學院與香港中文大學醫學院在2022年10月5日發表聯合報告,分析香港在2022年2月至3月的第五波疫情期間,在指定診所或於公立醫院接受治療的54,355名患者,包括60歲或以上的患者,以及60歲以下患有一種或以上長期病患的病人,當中兩成病人獲處方新型冠狀病毒口服藥。研究團隊發現住院治療的病人,獲處方輝瑞藥廠的帕昔洛韋(Paxlovid)或默沙東藥廠的莫努匹韋(Molnupiravir)後,死亡風險較一般治療降低76%,當中單一使用帕昔洛韋的患者可降低死亡風險90%,而單一使用莫努匹韋的病人死亡風險則下降69%。對於到指定診所接受診治的的患者,獲處方其中任何一種口服藥後,28天內入院的風險降低88%,單一使用帕昔洛韋可減少入院率達63%,而莫努匹韋也可降低28%的入院率。獲處方上述任何一種口服藥物的住院病人,28天內經急症室再入院率減少21%,帕昔洛韋可減少53%;莫努匹韋則可減少29%入院率。研究亦顯示帕昔洛韋(Paxlovid)每挽救1人性命便可減少醫療成本4.3萬港元,而這兩種藥物都能夠減少病人死亡風險及入院的機會,讓醫療資源更有效運用,其中帕昔洛韋更有助顯著降低醫療成本。為使香港醫療系統在疫情期間如常運作,研究團隊建議應將患者儘早轉介到指定的公營或私家診所,及時為高風險患者處方抗病毒藥物,以發揮這兩種口服藥的最大效益[46]。聯合研究報告已刊登於《刺針》醫學期刊[47]。
不可用作預防感染
輝瑞於2022年4月30日表示,其研究團隊在近期曾經招募3千位成年志願者進行關於預防受感染的臨床試驗,這些受試者都是與確診者一同居住,服藥5天者的感染機率下降32%、服藥10天者的感染機率下降至37%,但輝瑞指出這樣的結果並未能顯示帕昔洛韋具有預防被新型冠狀病毒感染的功效,故此帕昔洛韋只可用於預防高風險的患者惡化為重症,不應作為預防感染的藥物使用[48]。
授權協議
2021年11月15日,藥品專利池與輝瑞製藥達成協議[49],輝瑞製藥允許95個發展中國家可使用仿製的帕昔洛韋,無須支付專利費[50],這份協議涵蓋全球53%的人口,將可促進這種救命藥物的普及應用,世衛組織維持2019冠状病毒病是國際關注的突發公共衛生事件,名單內的國家便可獲豁免支付專利費[51]。2022年3月17日,藥品專利池公佈全球有35家製藥廠商獲授權生產帕昔洛韋的仿製藥,供應協議涵蓋的95個發展中國家[52]。
生產及包裝
Paxlovid最初在美國康乃狄克州格羅頓小量生產,主要供臨床測試之用[53]。Paxlovid的大量生產及包裝集中在德國弗萊堡的輝瑞口服藥生產廠房進行[54] ,而位於意大利阿斯科利皮切諾的廠房其後分擔Paxlovid的包裝工作[55]。截至2023年初,包括供應美國在內的輝瑞原廠Paxlovid都是在歐洲製造。
2022年,通過藥品專利池取得授權的藥廠在輝瑞的指導下開始仿製帕昔洛韋或生產其成份,產品的品質由各仿製藥廠負責管理及接受所在地政府的監管,其中由印度藥企Astrica生產的帕昔洛韋仿製藥稱為Primovir,另一印度藥企Hetero生產的名為Paxista,其成份及藥效與輝瑞原版的帕昔洛韋相同,這些仿製藥可供藥品專利池指定的95個開發中國家以低廉價格取得使用[56]。2022年12月28日,藥品專利池宣布由印度Hetero生產的Paxlovid仿製藥剛通過世衛組織的預先授權[57],將會以Nirmacom為名供應及出口予藥品專利池的受惠國[58]。
採用
美國
2021年12月22日,帕克斯洛維德獲美国食品药品监督管理局批准作緊急使用[59][60][61]。美國聯邦政府已同意向輝瑞購買1000萬份口服藥療程,並與各州政府合作,公平地為患者免費提供該口服藥[62]。
2022年3月1日,美國總統拜登表示已經啟動計劃,美國人如在藥店接受病毒檢測的結果為陽性,便可免費獲取抗病毒口服藥,拜登又稱輝瑞將於3月向美國提供100萬顆藥,4月更會加倍供應,拜登還稱輝瑞口服藥可降低達90%的最終入院治療機率[63]。
英國
2021年12月31日,英國藥物及保健產品管理局批准帕克斯洛維德用於18歲或以上的受感染人士[65]。英國衛生及社會關懷部在2021年12月10日宣布國民保健署會為新型冠狀病毒病患者免費提供抗病毒藥物至2022年3月31日,2022年3月宣布延長免費提供抗病毒藥物至2023年3月31日[66]。
歐盟
2022年1月27日,歐洲藥品管理局有條件批准帕克斯洛維德的使用,並建議供不需要使用氧氣瓶及有惡化為重症風險的患者服用[67]。
《德国之声》报导德国批准Paxlovid上市之际,德国卫生部就向辉瑞订购了100万盒,在德国获取该药需要医生处方,作为紧急抗疫措施,无论是法定医疗保险还是私人医疗保险的德国患者,使用该药都不需要自己付费,Paxlovid的费用几乎全由政府买单[68],而在药店的成本统一定价为60欧元。中国媒体报导称德国、奥地利在Paxlovid的政府采购价为每盒500欧元[68]。
台灣
2021年12月2日,中央流行疫情指揮中心指揮官陳時中透露落實購買輝瑞口服藥,正在與輝瑞製藥準備簽署合約[69]。
2022年1月15日,中央流行疫情指揮中心宣布,核准本藥輸入專案,並訂購2萬份[70][71]。
2022年1月27日,中央流行疫情指揮中心宣布,本藥首批3200人份運抵台灣[72][73]。
2022年4月11日,中央流行疫情指揮中心指揮官陳時中表示,已與輝瑞公司簽訂本藥70萬人份的採購合約,其中35萬人份藥物將於今年第二季前運抵國內。之前採購的2萬人份有1萬5200人份未到貨,已提出要求在兩周內付運,目前輝瑞口服藥已使用約130份,還是很夠用。參考先進國家的口服藥物儲備情況,國內應採購佔總人口3%的口服藥物,即約為70萬人份,其中35萬人份將於今年第二季前到貨,另外35萬人份屬開口式合約[74][75]。
2022年4月14日,中央流行疫情指揮中心發言人莊人祥證實,第一批次採購的2萬人份再到貨約4100人份,剩約1.1萬人份未到貨[76][77][78]。
2022年4月21日,行政院發言人羅秉成表示,藥物整備相當充足,35萬人份的本藥預計最快本月底、5月初到貨[79]。
2022年4月22日,中央流行疫情指揮中心表示,為積極因應新型冠狀病毒在社區流行,降低疫情對醫療量能的衝擊,已經與輝瑞簽訂70萬人份的採購合約,近期已有逾18萬人份抵臺,預計於2022年第二季內完成交貨[80][81][82]。
2022年4月24日,中央流行疫情指揮中心指揮官陳時中表示,今天會再有1.5萬份輝瑞口服藥抵台,第一批的2萬人份及第二批的35萬人份已全數到位,另外還有35萬人份的開口合約[83]。Paxlovid在台灣的使用受疾管署管制,僅能經醫師診療後開立處方箋,再到藥局取藥,由於Paxlovid屬於公費藥物,台灣民眾如獲處方此藥,除了診療院所的掛號費外,一律免收Paxlovid的藥費[84]。
香港
2021年11月19日,香港衞生署衞生防護中心轄下疫苗可預防疾病科學委員會和新發現及動物傳染病科學委員會舉行聯席會議後會見記者,科學委員會主席許樹昌表示醫院管理局已採購默沙東藥廠的莫納皮拉韋,也已向輝瑞藥廠洽購口服藥[85]。
2022年2月23日,食物及衞生局局長陳肇始表示醫院管理局已根據專家意見,採購默克藥廠的莫納皮拉韋及輝瑞藥廠的帕克斯洛維德兩種口服藥[86]。
2022年3月14日,首批帕克斯洛維德運抵香港[87],隨即於16日由醫院管理局轄下的公立醫院及指定診所分發給確診患者[6]。雖然帕克斯洛維德和另一種口服藥莫納皮拉韋在運抵香港時均不是香港註冊藥物[24],但法例容許註冊醫生治療特定病人時使用未經註冊藥品及製劑[6],因此註冊醫生可處方帕克斯洛維德給病人服用,惟病人或家屬獲配發有關藥物時須要簽署同意書[24]。行政長官林鄭月娥宣稱已購入足夠抗病毒藥物,但因為和供應商有保密協議,不能公開採購價及採購量[88]。
2022年4月2日,食物及衞生局稱將會向私家醫生免費提供帕克斯洛維德和另一種口服藥莫納皮拉韋,為有較高風險轉變成重症的患者提供口服藥治療,獲分配口服藥的的私家醫生不得向病人收取藥費[89]。
2022年12月31日,衞生署表示已發信通知獲政府分發帕克斯洛維德和莫納皮拉韋兩種新冠口服藥的私家醫生,政府提供的新冠治療藥應優先供「符合資格人士」使用,處方政府提供的相關藥物時只有香港居民不需繳付藥費,私家醫生如使用醫院管理局或衛生署分配的新冠口服藥治療旅客等「非符合資格人士」[90],便須要先代為向「非符合資格人士」收取每個療程超過6000港元的藥費,私家醫院及診所亦應直接向藥廠訂購新冠藥物作為治療「非符合資格人士」之用[91]。
新加坡
2022年2月3日,新加坡衛生部宣布已經與輝瑞簽署冠病口服药Paxlovid的採購協議,当局並且通过大流行病特别采用程序临时授权使用冠病口服药Paxlovid,也是首款在新加坡获得批准的冠病口服药物[92]。
2022年4月19日,新加坡衛生部宣布所有政府综合诊疗所和20家公共卫生防范诊所,都將會提供冠病口服药Paxlovid治疗病情可能演变成重症的冠病患者。新加坡衛生部表示目前在基层医疗设施使用冠病口服药Paxlovid無須收費,Paxlovid的藥費由衛生部全額承擔,但將來或會在適合的時間調整Paxlovid的收費方針[93]。
日本
2022年2月10日,日本厚生勞動省特例批准使用輝瑞口服藥,並已與輝瑞簽訂200萬人份的採購協議[94]。因為該藥品由厚生勞動大臣特例批准輸入及應用,故此患者在使用該藥前,須要根據特例批准制度簽署同意書[95]。
中國大陸
2022年2月11日,辉瑞公司新冠病毒治疗药物“奈玛特韦片/利托那韦片组合包装”获中華人民共和國国家药品监督管理局应急附条件批准进口使用[4]。
2022年3月9日,輝瑞公司與通用技术中国医药(簡稱中国医药)達成協議,中国医药將會負責辉瑞新冠病毒治疗药物Paxlovid在中國大陸的商業運營[96]。中國醫藥其後以“帕罗韦德”為商品名在中國大陸境內銷售該藥品[97]。
2022年3月14日,中华人民共和国国家卫生健康委员会办公厅、国家中医药管理局办公室联合印发了《新型冠状病毒肺炎诊疗方案(试行第九版)》,其中帕罗韦德(Paxlovid)被列为抗病毒治疗策略之一,用于发病5天以内的轻型、普通型新型冠状病毒肺炎且伴有进展为重型高风险因素的成人与青少年[98]。
2022年3月20日,10000盒辉瑞新冠病毒治疗药紧急运送至长春,这是在中华人民共和国国内首次大规模使用这种新冠特效药[99]。
2022年8月18日,华海药业发布公告称公司与美国辉瑞签订协议,将在5年内为Paxlovid提供非排他性的制剂委托生产服务。其中奈玛特韦原料药和利托那韦制剂将由辉瑞提供,华海药业负责奈玛特韦制剂的生产[100]。华海药业生产的Paxlovid只供中国大陆内销[101]。
2022年12月14日,中国医药发布公告,公司与辉瑞签订协议,负责帕罗韦德在中国大陆市场的进口和经销,协议期限至2023年11月30日止[102]。
2022年12月16日,《成都商报》報導稱Paxlovid在中國大陸通過醫保的每盒採購價為2300元人民幣,對比美國政府每盒採購價529美元,換算人民币約3688元;欧洲多国政府采购价为每盒600美元至700美元,约合人民币4183元至4880元不等,香港和台灣的採購價也是700美元一盒;澳洲的每盒價格是1159澳元,折合人民币约5473元,所以中國大陸算是以低價購得Paxlovid,而根據輝瑞的日本官網解釋,為促進藥品在全球的公平獲取,故此Paxlovid在高收入國家的定價會比低收入國家為高[103]。雖然藥品專利池提供的輝瑞授權仿製藥每盒只需25美元或以下,但因為中國大陸的人均生產總值超出12000美元的中間分界線[104],不屬於指定的發展中國家,故此即使中國大陸的藥廠獲藥品專利池授權生產Paxlovid的仿製藥,也只可以出口到藥品專利池指定受惠的95個中低收入國家,不能用於內銷[103]。
2022年12月22日,广州私立医院和睦家医院发热门诊开始提供辉瑞Paxlovid,惟医生将视情况开出,且每日供应量有限[105]。
2022年12月26日,中国大陆媒体报导称章泽天在微信朋友圈介绍从京东健康网购平台购买Paxlovid的流程,声称可在线问诊医生,由医生根据病情开具处方即可购买,《第一财经》记者尝试从平台采购,但京东健康网页显示该药品须要互联网医院发热门诊的处方才可购买,售价每盒2640元人民币,记者曾经咨询京东健康平台上的互联网医生,医生表示查询后台后发现已经无货,同时发现章泽天在微信朋友圈的网购Paxlovid攻略已被删除[106]。
2022年12月初,中國大陸實施近3年的動態清零封控政策已無法阻止病毒大規模傳播,中國大陸疫情的病例出現爆炸性增長[107],而長期嚴格封控亦導致民眾不滿並引發白紙運動,加上經濟下行的壓力,當局在12月7日宣布「新十條」、撤銷大部分防疫措施及採取Paxlovid是一种广泛使用的抗病毒药物,在治疗各种病毒感染方面显示出显着的疗效。虽然主要关注点通常是身体副作用,但认识并解决Paxlovid对个人的情感影响也至关重要。[108]策略,病毒遂於中國大陸快速傳播,但因為疫苗接種及藥物取得等方面都缺乏足夠準備[109][8],在年老、有基礎疾病及從未接種疫苗的脆弱人群染病人數急增的情況下[104],輝瑞新冠口服藥供不應求,並且出現炒黃牛,原本只會在重點醫院處方的帕罗韦德出現在交易平台,部分索價每盒過萬元人民幣,即使印度生產的仿製藥售價也達到2500元人民幣一盒[110]。
2023年1月初,辉瑞Paxlovid已在上海各级医疗机构应用,但开药对医生和患者都有严格的限制条件。辉瑞新冠口服药由医生开具处方使用,优先保障有重症倾向的特殊人群以及65周岁以上患者用药。由医院处方的价格调整为1890元/盒(共30粒),可通过医保甲类支付(即可全额纳入报销范围)[111]。此外,广州天河区一社区卫生服务中心也开始提供辉瑞Paxlovid,患有基础病的65岁以上居民可凭相关证明前往社区医院购买[112]。
2023年1月3日,华大基因首席执行官尹烨等人宣称印度Astrica生产的辉瑞Paxlovid仿制药Primovir涉嫌大量造假,国内黑市买卖的Primovir绝大部分都缺少了抑制Sars-Cov-2在体内增殖的奈瑪特韋,被替换为廉价的流感病毒抑制药奥司他韦[113][114]。《科创板日报》称涉事印度药企Astrica相关负责人表示此事是由于代工厂生产了无效Primovir药品,又提及该代工厂很贪婪,所以我们已删除了包装上的公司名称和号码,不过报导又指不含奈玛特韦的Primovir并不通过Astrica销售,该报记者在Astrica官网没有找到该药品,Astrica出品的Primovir(绿盒)被指有较多假货后,大家都转买另一家印度仿制药生产商Hetero出品的Paxista(蓝盒),所以现在“蓝盒”的售价更贵,Primovir(绿盒)现售2800元/盒,Paxista(蓝盒)则要3800元/盒[114]。
2023年1月5日,《联合早报》报导在中国大陆“一药难求”的Paxlovid已成为奢侈品,在私立医院的每盒售价8300元人民币,黑市售价被炒至万元人民币以上,并被作为送礼佳品,成为社会精英阶层的人情礼物[115]。台媒引述中国大陆社交媒体指黄牛党将原价2980元人民币的一盒Paxlovid炒高16倍至4万8千元人民币转售时,还称“想帮助人”,已经便宜卖,不还价[116]。
2023年1月7日,多部门联合发布《关于实施“乙类乙管”后优化新型冠状病毒感染患者治疗费用医疗保障相关政策的通知》,其中明确,新型冠状病毒感染诊疗方案中新型冠状病毒治疗药品延续医保临时支付政策,先行执行至2023年3月31日[117]。此外,在医保与辉瑞谈判第二天,《经济观察网》报称业内传出Paxlovid本次医保谈判后的价格将下调至700元/盒的消息[118],但此消息在两天后被财新新闻否认[119]。
2023年1月8日,在国家医保药品目录谈判工作结束后,国家医疗保障局医药管理司负责人介绍阿兹夫定片、清肺排毒颗粒谈判成功参与医保药品目录,而Paxlovid因生产企业辉瑞投资有限公司报价高未能成功,但医保都将临时性支付Paxlovid及默沙东公司的莫诺拉韦胶囊到2023年3月31日[120][121],4月1日起便要自费。境内媒体称医保局与辉瑞在1月7日上午9时开始谈判,辉瑞中国代表在下午1时20分离开谈判内场,这轮谈判超过4小时,比医保局规定每种药谈判半小时长很多,但未知是否全部时间都用于Paxlovid的谈判上[122]。据悉,在过去的几轮谈判中,辉瑞公司的Paxlovid已经降价高达62%[123]。
2023年1月9日,辉瑞首席执行官艾伯乐(Albert Bourla)出席摩根大通医疗保健会议发言時表示[124],辉瑞在Paxlovid纳入中国医保药品目录谈判上的报价已低于其他中等收入国家的定价,可是中国政府要求的报价比大多数中低收入国家还要低[125],因而导致谈判破裂,然而中国作为全球第二大经济体,因此我不认为中国采购Paxlovid付出的价格应该比贫穷国家如萨尔瓦多更低[125],但辉瑞仍会与中国当局重新谈判[126]。对于有传闻称辉瑞正在与中国当局讨论由中国大陆的制药厂生产Paxlovid仿制药供应中国大陆境内使用,艾伯乐澄称没有与中国当局进行仿制药相关的讨论[127],因为辉瑞早以就在中国境内生产Paxlovid达成协议,在中国的一个合作伙伴计划在2023年上半年开始本地化生产供应中国大陆的Paxlovid[128]。艾伯乐又表示辉瑞在2022年已将数以万计的Paxlovid疗程运送到中国大陆,而在最近数周,运交量已提升至数百万计,但因为未能纳入中国医保药品目录,Paxlovid将来在中国大陆只能够从私人市场获取[126]。
Paxlovid的医保谈判破裂的消息在1月8日在中国大陆被媒体广泛报道,医保局宣称Paxlovid没有入选是因为辉瑞公司报价太高,新浪财经称医保局在谈判中要求辉瑞根据中国医保价格指引把Paxlovid降价到每盒人民币200元或以下[129],然而辉瑞首席执行官艾伯乐在1月9日公开表示中国身为世界第二大经济体却要求比贫穷小国萨尔瓦多更低的采购价。Paxlovid的医保支付问题随即引起广泛议论,中国境内部分媒体评论称Paxlovid没进医保,可以为中国自研的同类药品让路,又认为艾伯乐提及萨尔瓦多无非是说中国应出高价买药[130],认为辉瑞是趁火打劫及发灾难财。《法广》等境外媒体报导称中国大陆的采购价即使以1890元人民币,折合不到300美元的价格计算,作为第二大经济体的中国大陆,已经明显比美国每盒529美元,欧洲、香港、台湾等地600至700美元不等的购入价便宜许多,辉瑞将定价与各国经济水平挂钩[132],目的是促进药品在全球的公平获取,所以辉瑞认为中国大陆支付的价格不应低于萨尔瓦多等穷国是合理的,报导又引述中国大陆网民对中国当局自称人民至上的评论[133],批评这三年来密集的核酸用掉的钱更多[134],4.8万元一个核酸亭及现在建成不久便拆掉的方舱还不是更贵更花钱[135],可是连一盒能够有效减少住院及死亡的Paxlovid救命药却不愿出,质疑人命是否不值1890元人民币[136]。澳洲媒体认为Paxlovid的使用能够大幅减少需要住院的人数,减轻医疗体系承受的压力,在医疗经济学仍是十分划算[137]。
中国大陆境内有建议称中国国务院应该宣布辉瑞持有的Paxlovid专利保护在中国失效,让中国制药厂无需辉瑞同意便可生产这种救命药物[138],不过中国专利法学者认为强行仿制Paxlovid的理据不充分,因为启动专利强制许可的前提是,在中国出现重特大传染病疫情及其他突发公共卫生事件或防治重特大疾病药品出现短缺,对公共卫生安全或公共健康造成严重威胁等非常情况时、同时原研厂家仍坚持专利保护等才能进行,而目前中国大陆已经宣布《新十条》及“乙类乙管”降低对新冠病毒威胁性的定义,在这情况下更没有理由去强行仿制,而且该药已在境内使用,目前只是医保采购的价格没有谈成,如果只因价格谈不拢便强制授权,会对中国保护专利的信誉造成严重打击[138]。台湾媒体表示中国大陆当局只要承认疫情严重,公开交代疫情危急及宣布中国大陆疫情进入紧急状态,便可使用及生产定价不多于25美元的Paxlovid仿制药,但问题在于中国当局是否愿意这样做[139]。
根据辉瑞首席执行官艾伯乐在2023年1月9日称目前正在与在中国的伙伴合作推动在中国境内生产Paxlovid,预期最快可在数个月内投产,《时代财经》记者以消费者身份致电辉瑞,相关人士回复称仍未有中国制药厂家生产Paxlovid,目前在中国市场供应的Paxlovid均为进口[140]。
2023年1月18日,英国广播公司报导指中国社交媒体对Paxlovid因为价格问题不被纳入医保一片哗然,中国网民批评政府过去三年花大力气去“清零”,将大量资金花费在无数次的核酸检测,现在却无钱去买药,英国广播公司引用中国财新网的报导称单是广东省在这三年便投入1467.93亿元人民币(216.8亿美元)用于疫情防控,分别相当于当年一般公共预算的2.34%、3.22%和5.36%,逐年递增[141]。对于辉瑞的报价,腾讯棱镜称,辉瑞实际的报价是600多元人民币,但距离医保局的底线还是比较远,而财新报道辉瑞的报价在1890元人民币,基本没降。美国耶鲁大学全球健康政策与经济学副教授陈希受访时表示,美国政府与辉瑞签订的Paxlovid采购价每盒约530美元,辉瑞给各国的定价与其经济发展、人均收入挂钩,给中国的建议价也因此比发达国家更便宜,陈希又称因为在公共卫生危机下对减少重症及死亡有緊迫性,故此特效药的采购与平常药品的集中采购属性不同,可是中国政府执行三年强力的清零政策后,医疗卫生资金已经过度透支,加上医保的收入因为经济不景气而减少,现在购买特效药的开支确实对中国医保预算可负担性构成严峻的考验[141]。陈希表示Paxlovid是目前极少数通过双盲试验以及得到真实世界检验,对新冠患者有效降低重症风险的药物,有效性和安全性总体最好,对于期望Paxlovid能够纳入医保的中国患者而言,这不仅关乎经济上的可负担性,也可确保得到足够的供应。新加坡国立大学李光耀公共政策学院副教授吴木銮表示,中国政府过往三年坚持“清零”政策,对治疗药物的准备没有这么大的紧迫性[141],而现在对Paxlovid的需求旺盛,很多人都要通过黑市购买,理想的情况是Paxlovid进入医保,让贫困及边缘人群都负担得起,这样可大大减少重症及死亡率,吴木銮又称当前中国缺乏各种药物是因为中国政府对疫情的准备严重不足,虽然春运已经开始,但中国有关部门却没有推出有效的措施保护老年人,因为春运和春节会带来更多新冠病毒传播,现在还应该保持警惕[141]。
參考資料
- . Therapeutic Goods Administration (TGA). 21 January 2022 [5 February 2022]. (原始内容存档于2022-02-05).
- . [2022-03-16]. (原始内容存档于2022-02-05).
- . covid-vaccine.canada.ca. Health Canada. [2022-03-31]. (原始内容存档于2022-01-18).
- . 国家药品监督管理局. 2022-02-12 [2022-02-12]. (原始内容存档于2022-05-16).
- . European Medicines Agency (EMA). 24 January 2022 [3 February 2022]. (原始内容存档于2022-05-11). Text was copied from this source which is copyright European Medicines Agency. Reproduction is authorized provided the source is acknowledged.
- . 明報. 2022-03-16 [2022-03-23]. (原始内容存档于2022-05-16).
- . 111年衛生福利部新聞 (衛福部食藥署). 2022-01-15 [2022-12-30]. (原始内容存档于2022-12-30).
- . Medicines and Healthcare products Regulatory Agency (MHRA). 31 December 2021 [31 December 2021]. (原始内容存档于2021-12-31).
- . Medicines and Healthcare products Regulatory Agency (MHRA). 31 December 2021 [31 December 2021]. (原始内容存档于2022-01-11).
- . DailyMed. [30 December 2021]. (原始内容存档于2021-12-31).
- . U.S. Food and Drug Administration (FDA) (新闻稿). 22 December 2021 [22 December 2021]. (原始内容存档于2021-12-27).
 本文含有此來源中屬於公有领域的内容。
本文含有此來源中屬於公有领域的内容。 - (PDF) (技术报告). Pfizer. 22 December 2021. LAB-1492-0.8. (原始内容存档于23 December 2021).
- . 第一财经. 2023-01-06 [2023-01-16]. (原始内容存档于2023-01-16).
- Marzolini C, Kuritzkes DR, Marra F, et al. Prescribing Nirmatrelvir-Ritonavir: How to Recognize and Manage Drug-Drug Interactions [published online ahead of print, 2022 Mar 1]. Ann Intern Med. 2022;M22-0281. doi:10.7326/M22-0281
- Hammond J, Leister-Tebbe H, Gardner A, et al. Oral Nirmatrelvir for High-Risk, Nonhospitalized Adults with Covid-19. N Engl J Med. 2022;386(15):1397-1408. doi:10.1056/NEJMoa2118542
- . Pfizer. 2021-11-05 [2023-01-09]. (原始内容存档于2021-11-16).
- . 辉瑞公司. [2023-01-03]. (原始内容存档于2023-06-08).
- . ABC中文. 2022-12-14 [2023-01-03]. (原始内容存档于2023-01-03).
- . Yahoo新聞. 2022-01-27 [2023-01-03]. (原始内容存档于2023-01-03).
- . 杭州网. 2022-12-26 [2023-01-16]. (原始内容存档于2022-12-26).
- . 中新经纬. 2023-02-02 [2023-02-04]. (原始内容存档于2023-02-04).
- . 美国疾控中心(CDC). 2022-12-05 [2022-12-25]. (原始内容存档于2022-01-04) (美国英语).
- . 香港政府新聞公報. 2022-03-15 [2022-03-16]. (原始内容存档于2022-04-26).
- . 香港電台. 2022-03-15 [2022-03-22]. (原始内容存档于2022-05-26).
- . www.fda.gov. U.S. Food and Drug Administration. [2023-01-03]. (原始内容存档于2023-03-06).
- . 香港大學. 2022-10-03 [2023-01-03]. (原始内容存档于2023-01-03).
- . 中新網. 2022-03-15 [2022-03-16]. (原始内容存档于2022-05-16).
- . 美国食品药品监督管理局(FDA). 2022-09-26 [2022-12-25]. (原始内容存档于2023-03-06).
- . NewTalk新聞. 2022-04-23 [2022-04-25]. (原始内容存档于2022-05-18).
- . clinicaltrials.gov. National Institutes of Health. [2023-01-09]. (原始内容存档于2022-01-05).
- . Bloomberg. 2021-11-05 [2023-01-09].
- . National Institutes of Health. 2022-12-01 [2023-01-09]. (原始内容存档于2022-12-01).
- . 星島日報. 2022-03-14 [2022-03-16].
- 国家卫生健康委员会办公厅、国家中医药管理局办公室. (PDF): 15. 2022-03-15 [2022-03-16]. (原始内容 (PDF)存档于2022-03-15) (中文(中国大陆)).
- . BBC. 2022-02-23 [2022-03-16]. (原始内容存档于2022-05-25).
- . National Institutes of Health. 2022-02-24 [2022-03-16]. (原始内容存档于2022-04-23).
- . SundayKiss (新傳媒集團). 2022-03-16 [2022-03-16]. (原始内容存档于2022-06-10).
- Lamb Y N. Nirmatrelvir Plus Ritonavir: First Approval[J]. Drugs, 2022: 1-7.
- . [2022-03-16]. (原始内容存档于2022-04-23).
- Marzolini C, Kuritzkes D R, Marra F, et al. Prescribing Nirmatrelvir–Ritonavir: How to Recognize and Manage Drug–Drug Interactions[J]. Annals of Internal Medicine, 2022.
- . 世衛組織. 2022-04-22 [2022-04-25]. (原始内容存档于2022-06-11).
- . 中央通訊社. 2022-04-22 [2022-04-25]. (原始内容存档于2022-05-30).
- . 三立新聞. 2022-04-22 [2022-04-26]. (原始内容存档于2022-06-04).
- . 2022-12-13 [2022-12-24]. (原始内容存档于2023-01-23).
- . 2022-12-02 [2022-12-24]. (原始内容存档于2023-03-30).
- . 香港中文大學賽馬會公共衛生及基層醫療學院. 2022-10-06 [2023-01-09]. (原始内容存档于2023-01-09).
- . 中大新聞中心 (香港中文大學). 2022-10-05 [2022-12-30]. (原始内容存档于2022-12-30).
- . Yahoo新聞. 2022-04-30 [2022-12-30]. (原始内容存档于2022-12-30).
- . 聯合國新聞. 2021-11-15 [2022-03-31]. (原始内容存档于2022-04-25).
- . 台灣英文新聞. 2021-11-17 [2022-04-12]. (原始内容存档于2022-04-26).
- . 頭條日報. 2022-03-21 [2022-04-12]. (原始内容存档于2022-03-21).
- . 明報. 2022-03-19 [2022-04-12]. (原始内容存档于2022-05-12).
- Green R. . The Hartford Courant. 2021-12-23 [2022-01-15]. (原始内容存档于2022-01-15).
- Schmidt B. [Pfizer corona medicine is being manufactured in Freiburg]. Badische Zeitung. 2021-12-01 [2022-01-15]. (原始内容存档于2022-01-15) (德语).
- Paci M. [Covid, in Ascoli the only plant in Italy that will produce the antiviral drug. Pfizer thinks to hire one hundred]. Corriere Adriatico. 2021-12-17 [2022-01-15]. (原始内容存档于2022-01-15) (意大利语).
- . ORF. 2022-12-21 [2022-12-30]. (原始内容存档于2023-01-21).
- . Pharmaceutical Technology. 2022-12-27 [2023-01-03]. (原始内容存档于2023-01-21).
- . PChome. 2022-12-28 [2023-01-03]. (原始内容存档于2023-01-03).
- Pfizer Receives U.S. FDA Emergency Use Authorization for Novel COVID-19 Oral Antiviral Treatment (页面存档备份,存于)(輝端公司新聞稿,2021年12月22日)
- Coronavirus (COVID-19) Update: FDA Authorizes First Oral Antiviral for Treatment of COVID-19 (页面存档备份,存于)(美国食品药品监督管理局新聞發佈,2021年12月22日)
- EUA 105 Pfizer Paxlovid LOA (12222021) - US Food and Drug Administration (页面存档备份,存于)
- . 風傳媒. 2021-12-23 [2022-04-22]. (原始内容存档于2022-04-26).
- . 路透社. 2022-03-02 [2023-01-03]. (原始内容存档于2023-01-03).
- . [2022-03-16]. (原始内容存档于2022-05-16).
- . 中央通訊社. 2021-12-31 [2022-03-23]. (原始内容存档于2022-05-16).
- . Department of Health and Social Care. 2022-03-31 [2023-01-11]. (原始内容存档于2023-03-29).
- . 香港經濟日報. 2022-01-28 [2022-03-16]. (原始内容存档于2022-04-05).
- . 德国之声. 2023-01-09 [2023-01-11]. (原始内容存档于2023-02-22).
- . NewTalk新聞. 2021-12-02 [2022-03-23]. (原始内容存档于2022-06-04).
- . [2022-04-15]. (原始内容存档于2022-04-15).
- . [2022-04-22]. (原始内容存档于2022-01-30).
- . 中央廣播電臺. 2022-01-27 [2022-03-16]. (原始内容存档于2022-05-16).
- . [2022-04-22]. (原始内容存档于2022-04-22).
- . [2022-04-15]. (原始内容存档于2022-04-15).
- . [2022-04-22]. (原始内容存档于2022-04-11).
- . [2022-04-15]. (原始内容存档于2022-04-15).
- . [2022-04-22]. (原始内容存档于2022-04-26).
- . [2022-04-22]. (原始内容存档于2022-06-06).
- . [2022-04-22]. (原始内容存档于2022-04-22).
- . [2022-04-22]. (原始内容存档于2022-04-22).
- . [2022-04-22]. (原始内容存档于2022-04-23).
- . [2022-04-22]. (原始内容存档于2022-05-17).
- . [2022-04-24]. (原始内容存档于2022-04-25).
- . 健康2.0 (TVBS). 2022-05-16 [2023-01-03]. (原始内容存档于2023-01-03).
- . 香港經濟日報. 2021-11-19 [2022-03-23]. (原始内容存档于2022-03-23).
- . 星島日報. 2022-02-23 [2022-03-22].
- . 明報. 2022-03-15 [2022-03-15]. (原始内容存档于2022-04-18).
- . 明報. [2022-03-15]. (原始内容存档于2022-06-14).
- . 東方日報. 2022-04-02 [2022-04-22]. (原始内容存档于2022-04-26).
- . 新聞公報 (香港特區政府). 2022-12-31 [2023-01-03]. (原始内容存档于2023-02-06).
- . 東方日報. 2022-12-31 [2023-01-03]. (原始内容存档于2023-01-03).
- . 联合早报. 2022-02-03 [2023-01-03].
- . 8視界新聞. 2022-04-19 [2023-01-03]. (原始内容存档于2023-01-03).
- . 日本經濟新聞社. 2022-02-11 [2022-03-23]. (原始内容存档于2022-02-11).
- . Pfizer株式会社. [2023-01-03]. (原始内容存档于2023-01-03).
- 中国通用技术(集团)控股有限责任公司. . 国务院国资委宣传局. 2021-03-14 [2023-01-03]. (原始内容存档于2023-01-03).
- . 中国医药工业杂志, 2021, 52(12).
- . [2022-03-18]. (原始内容存档于2022-04-03).
- . 光明网. [2022-03-23]. (原始内容存档于2022-05-16).
- . 2022-08-19 [2022-12-26]. (原始内容存档于2022-12-26).
- . 医药魔方. 2022-08-19 [2023-01-08]. (原始内容存档于2023-01-08).
- . 中国财经报官博. 2022-12-15 [2022-12-18]. (原始内容存档于2022-12-18).
- . 成都商报 (中国经济网). 2022-12-16 [2023-01-03]. (原始内容存档于2023-01-03).
- . 香港01. 2023-01-01 [2023-01-03]. (原始内容存档于2023-01-03).
- 吴泽鹏. . 每日经济新闻. 2022-12-23 [2022-12-23]. (原始内容存档于2022-12-25).
- . 新浪科技. 2022-12-26 [2023-01-16]. (原始内容存档于2023-01-16).
- . 法國國際廣播電台. 2022-12-15 [2022-12-18]. (原始内容存档于2022-12-15).
- Regar Rajasthani. . Regar Rajasthani. Regar KR. [2023-07-18].
- Zhan Juan. . 紐約時報中文網. 2023-01-05 [2023-01-08]. (原始内容存档于2023-02-04).
- . 頭條日報. 2022-12-30 [2022-12-30]. (原始内容存档于2023-01-18).
- . m.thepaper.cn. [2023-01-04]. (原始内容存档于2023-01-04).
- 杨晓彤. . 南方都市报. 2023-01-04 [2023-01-05]. (原始内容存档于2023-01-05).
- 尹烨. . 微博. 2023-01-05 (中文(中国大陆)).
- . 每日经济新闻. 2023-01-05 [2023-01-06]. (原始内容存档于2023-01-06) (中文(中国大陆)).
- 察客. . 联合早报. 2023-01-05 [2023-01-09].
- . 自由時報. 2023-01-06 [2023-01-09]. (原始内容存档于2023-01-09).
- . 中华人民共和国中央人民政府. 医保局. [2023-01-08]. (原始内容存档于2023-01-09) (中文(中国大陆)).
- 瞿依贤. . 经济观察网 (新浪财经). 2023-01-07 [2023-01-08]. (原始内容存档于2023-01-11) (中文(中国大陆)).
- . m.weibo.cn. [2023-01-09]. (原始内容存档于2023-01-09).
- . m.thepaper.cn. [2023-01-08]. (原始内容存档于2023-01-08).
- 国家医疗保障局. . 国家医疗保障局. 2023-01-08 [2023-01-08]. (原始内容存档于2023-02-02) (中文(中国大陆)).
- . 第一财经. 2023-01-08 [2023-01-11]. (原始内容存档于2023-01-11).
- Reuters. . Reuters. 2023-01-08 [2023-01-08]. (原始内容存档于2023-03-09) (英语).
- . CNBC. 2023-01-09 [2023-01-12]. (原始内容存档于2023-02-16).
- . 香港經濟日報. 2023-01-10 [2023-01-10]. (原始内容存档于2023-01-10).
- . 蘋果日報. 2023-01-10 [2023-01-10]. (原始内容存档于2023-01-10).
- . 联合早报. 2023-01-10 [2023-01-10].
- . 德国之声. 2023-01-10 [2023-01-11]. (原始内容存档于2023-03-15).
- . 新浪财经. 2023-01-09 [2023-01-15]. (原始内容存档于2023-01-15).
- . 新浪财经. 2023-01-11 [2023-01-12]. (原始内容存档于2023-01-12).
- . 法国国际广播电台. 2023-01-10 [2023-01-12]. (原始内容存档于2023-01-14).
- . 美国之音. 2023-01-11 [2023-01-12]. (原始内容存档于2023-01-16).
- . 财新网. 2023-01-08 [2023-01-12]. (原始内容存档于2023-01-12).
- . 东方日报. 2023-01-09 [2023-01-13]. (原始内容存档于2023-01-13).
- . Yahoo新闻. 2023-01-10 [2023-01-12]. (原始内容存档于2023-01-13).
- . 澳华网. 2023-01-11 [2023-01-13].
- . 新浪财经. 2013-01-10 [2023-01-15]. (原始内容存档于2023-01-15).
- . Yahoo新闻. 2023-01-13 [2023-01-15]. (原始内容存档于2023-01-16).
- . 时代财经. 2023-01-11 [2023-01-16]. (原始内容存档于2023-01-16).
- . BBC. 2023-01-18 [2023-01-20]. (原始内容存档于2023-03-15).
外部連結
| 维基共享资源上的相关多媒体资源:奈瑪特韋/利托那韋 |
- PAXLOVID™ (nirmatrelvir and ritonavir) (页面存档备份,存于) - 輝瑞為美國居民設置的Paxlovid資訊官方網站(英語)