氢氧化镉
氢氧化镉是一种无机化合物,化学式为Cd(OH)2。它是一种离子化合物,为白色晶体。它在鎳鎘電池中是一种关键性的化合物[3]。氢氧化镉的碱性比氢氧化锌强。[4]
| 氢氧化镉 | |
|---|---|
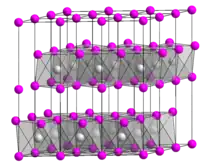 | |
 | |
| IUPAC名 氢氧化镉(II) | |
| 识别 | |
| CAS号 | 21041-95-2 |
| PubChem | 10313210 |
| ChemSpider | 8488675 |
| SMILES |
|
| InChI |
|
| InChIKey | PLLZRTNVEXYBNA-NUQVWONBAA |
| 性质 | |
| 化学式 | Cd(OH)2 |
| 146.43 g/mol g·mol⁻¹ | |
| 外观 | 白色晶体 |
| 密度 | 4.79 g/cm3 |
| 熔点 | 150 °C(分解) |
| 溶解性(水) | 0.026 g/100 mL |
| 溶解性 | 可溶于稀酸、氨水和铵盐溶液[1] |
| 结构 | |
| 晶体结构 | 六方(β) 单斜(γ) |
| 热力学 | |
| ΔfHm⦵298K | −561 kJ·mol−1[2] |
| S⦵298K | 96 J·mol−1·K−1[2] |
| 危险性 | |
| 警示术语 | R:R20/21/22-R50/53 |
| 安全术语 | S:S60-S61 |
| 欧盟分类 | |
| 相关物质 | |
| 其他阴离子 | 氯化镉 溴化镉 碘化镉 氧化镉 |
| 其他阳离子 | 氢氧化锌 氧化汞 氢氧化铜 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
制备
- Cd(NO3)2 + 2 NaOH → Cd(OH)2↓ + 2 NaNO3
另一种制法是将氢氧化钾固体加入至碘化镉溶液中,产生的沉淀先加热至其溶解,再静置溶液使之逐渐冷却,析出氢氧化镉。[1]
氢氧化镉也可通过水热法合成。如将20份的氢氧化钠配成的溶液加入1份乙酸镉配成的溶液中,再加入溶液等体积的乙二醇,搅拌半小时后,转移到水热反应釜中反应,在60℃的真空干燥箱中干燥4小时,得到产物。[5]
- Cd(CH3COO)2 + 2 NaOH → Cd(OH)2↓ + 2 CH3COONa
用硝酸镉溶液和5%KOH溶液反应,硝酸钠作为矿化剂,进行水热合成,可以得到六边形纳米盘Cd(OH)2。[6]
较新的合成方法还有微波法,如在聚乙二醇(PEG-10000)溶液中加入0.8mol·L-1的硝酸镉,搅拌均匀后,再加入等体积的0.8mol·L-1六次甲基四胺(HMTA),继续搅拌,之后转移到瓷坩埚内,加盖,置于微波炉中低温加热8min,冷却到室温后分别用一次水和多次乙醇洗涤,在60℃下干燥4h,得到Cd(OH)2螺旋形纳米线,反应机理如下:[7]
- (CH2)6N4 + 6 H2O → 6 HCHO + 4 NH3
- NH3 + H2O → NH4+ + OH−
- Cd2+ + 2 OH− → Cd(OH)2↓ + H2O
反应产生的纳米线的直径与长度可以通过改变反应物的浓度来控制,而阴离子的种类对产物的形貌有较大影响。
此外,固相反应也能得到氢氧化镉。如将镉盐(Cd(CH3COO)2·2H2O、CdCl2·2.5H2O、3CdSO4·8H2O或CdCO3·4H2O等)和PEG-400混合均匀,加入氢氧化钠固体,混合研磨半小时后放置5小时,用水与无水乙醇洗涤,在空气中自然干燥,可以得到具有晶形的产物。[8]
化学性质
氢氧化镉易吸收空气中的二氧化碳,产生碳酸镉。当氢氧化镉加热至150℃时,它会分解,生成氧化镉。[4][9]
- Cd(OH)2 + CO2 → CdCO3 + H2O
- Cd(OH)2 —Δ→ CdO + H2O
作为一种碱,氢氧化镉也能溶于酸:
- Cd(OH)2 + 2 HCl → CdCl2 + 2 H2O
- Cd(OH)2 + 2 HI → CdI2 + 2 H2O
- Cd(OH)2 + 2 CH3COOH → Cd(CH3COO)2 + 2 H2O
- Cd(OH)2 + 4 NH3·H2O → [Cd(NH3)4](OH)2 + 4 H2O
- Cd(OH)2 + 4 NaCN → Na2[Cd(CN)4] + 2 NaOH
和氢氧化锌不同的是,氢氧化镉仅微溶于氢氧化钠(5mol·L-1)溶液,溶解度为0.13g。在浓氢氧化钠溶液中存在Na2[Cd(OH)4]。[11]
参考资料
- 《无机化合物制备手册》.朱文祥 主编.化学工业出版社. P382~383. 【ⅩⅡ-21】氢氧化镉(cadmium hydroxide)
- Zumdahl, Steven S. . Houghton Mifflin Company. 2009: A21. ISBN 0-618-94690-X.
- Karl-Heinz Schulte-Schrepping, Magnus Piscator "Cadmium and Cadmium Compounds" in Ullmann's Encyclopedia of Industrial Chemistry, 2007 Wiley-VCH, Weinheim. doi:10.1002/14356007.a04_499.
- 《无机化学丛书》.第六卷 卤素 铜分族 锌分族. 科学出版社. 钟兴厚 吕云阳等主编. P581. 1.氢氧化镉
- 溶剂热法制备Cd(OH)2和CdO纳米盘研究性实验[J]. 李锦等. 《物理实验》. Vol.32 No.1. Jan.,2012
- 水热合成法制备六方形纳米盘Cd(OH)2. 刘俊渤 等. 吉林大学学报(理学版). Vol.47 No.3. May.,2009
- 微波法合成一维结构Cd(OH)2螺旋形纳米线. 彭银 等. 高等学校化学学报. pp.7~10 Vo1.31 No.1. Jan.,2010
- 室温固相化学反应法合成Cd(OH)2纳米棒. 曹亚丽 等. 高等学校化学学报. pp.1601~1603. Vol.25 No.9. Sept.,2004
- 《无机化学》(第二版)下册. 庞锡涛 主编. 高等教育出版社. 2-3 锌族元素的重要化合物. P365. ISBN 978-7-04-005387-6
- 《无机化学反应方程式手册》.曹忠良等主编. 湖南科学技术出版社. P218. 【Cd(OH)2】. 统一书号 13204·56
- Chemistry of the Elements(Second Edition). N.N. GREENWOOD and A. EARNSHAW. 29.3 Compounds of Zinc, Cadmium and Mercury. pp.1209
- . [2020-09-12]. (原始内容存档于2016-03-06).