氢碘酸
氢碘酸是碘化氫的水溶液,是種非氧化性酸,化學式為HI。氢碘酸的浓度通常为 48 - 57% HI。氢碘酸是一種強酸。腐蝕性強,有危險性,能灼傷皮膚。 它是第二强的氢卤酸,仅次于氫砈酸。氢碘酸是一种常用的化学试剂,是在水溶液中完全电离的强酸之一。
| 氢碘酸 | |
|---|---|
 | |
 | |
| IUPAC名 Iodane[1] | |
| 别名 | 水溶液称氢碘酸 |
| 识别 | |
| CAS号 | 10034-85-2 |
| PubChem | 260 |
| ChemSpider | 255 |
| SMILES |
|
| InChI |
|
| InChIKey | CPELXLSAUQHCOX-UHFFFAOYAZ |
| EINECS | 233-113-0 |
| ChEBI | 47266 |
| RTECS | MW3760000 |
| 性质 | |
| 化学式 | HI |
| 127.904 g·mol⁻¹ | |
| 外观 | 无色液体,氧化变为黄色至红棕色[2] |
| pKa | –9.48 |
| 结构 | |
| 分子构型 | 直线型 |
| 偶极矩 | 0.38 D |
| 危险性 | |
| 警示术语 | R:R20-R21-R22-R35 |
| 安全术语 | S:S7-S9-S26-S45 |
| MSDS | 碘化氢 氢碘酸 |
| 主要危害 | 有毒、腐蚀性 |
| NFPA 704 |
 0
3
0
|
| 闪点 | 不可燃 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
由於氢碘酸可用於製造甲基安非他命之還原劑,因此被列入美國緝毒局化學品監控列表的第一類化學品。
反应
氢碘酸会和空气中的氧气反应,使旧样本的颜色变深:
- 4 HI + O2 → 2 H
2O + 2 I2 - HI + I2 → HI3
像其他卤化氢一样,氢碘酸将与不饱和烃(例如烯烃)进行加成反应。 它也可以作为还原剂使用,例如在芳香族硝基化合物的还原反应中,也可以用作苯胺的还原剂。 [3]
参考资料
- Henri A. Favre; Warren H. Powell (编). . Cambridge: The Royal Society of Chemistry. 2014: 131.
- . Washington, DC: American Chemical Society. 2017-01 [2022-01-12]. ISBN 9780841230460. doi:10.1021/acsreagents.4160 (英语).
- Kumar, J. S. Dileep; Ho, ManKit M.; Toyokuni, Tatsushi. . Tetrahedron Letters. 2001, 42 (33): 5601–5603. doi:10.1016/s0040-4039(01)01083-8.
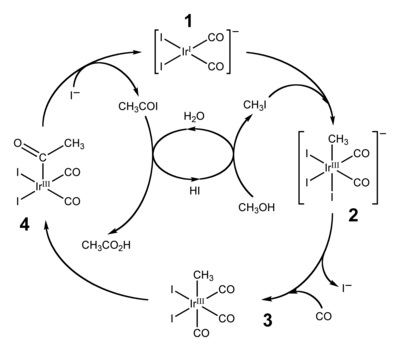
- Jones, J. H. (PDF). Platinum Metals Rev. 2000, 44 (3): 94–105 [2020-10-05]. (原始内容存档 (PDF)于2015-09-24).
- Sunley, G. J.; Watson, D. J. . Catalysis Today. 2000, 58 (4): 293–307. doi:10.1016/S0920-5861(00)00263-7.
- Skinner, Harry F. "Methamphetamine Synthesis via HI/Red Phosphorus Reduction of Ephedrine". Forensic Science International, 48 128-134 (1990)
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.