一氧化镍
一氧化镍,是镍的一种氧化物,化学式为NiO,其中镍的氧化态是+2。因常态下该物质为绿色粉末,故又称绿色氧化镍,以区别于主要成分为三氧化二镍的黑色氧化镍。一氧化镍广泛用于陶瓷和玻璃工业上,可以制造半导体薄膜,还可以作有机化合物氧化过程中的催化剂。
| 一氧化镍 Nickel(II) oxide | |
|---|---|
 | |
_oxide_sample.jpg.webp) | |
| 别名 | 氧化镍 绿色氧化镍 |
| 识别 | |
| CAS号 | 1313-99-1 |
| PubChem | 14805 |
| RTECS | QR8400000 |
| 性质 | |
| 化学式 | NiO |
| 74.69 g·mol⁻¹ | |
| 外观 | 绿色晶体 |
| 密度 | 6.84 g/cm3 |
| 熔点 | 1955±20 °C[1] |
| 溶解性(水) | 難溶 |
| 危险性 | |
| MSDS | ScienceLab.com |
| NFPA 704 |
 0
3
0
|
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
组成与结构
像很多二元金属氧化物一样,一氧化镍也是一种非整比化合物。即由于晶体缺陷等因素,一氧化镍中镍和氧的比例并非是严格的1:1,而是在1:1周围波动。镍与氧的原子比例影响着氧化镍粉末的颜色,当镍与氧的比例接近1:1时理想比例时,一氧化镍是绿色粉末,但当偏离较多时,为黑色粉末。
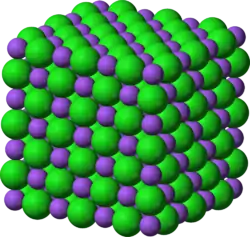
NiO的晶体结构与氯化钠类似,即岩盐结构,其中每个Ni2+(右图中较小的紫色原子)周围有六个最近距离的O2−(图中较大的绿色原子),氧原子形成正八面体,镍原子处于其中心;反之亦然,氧原子也处于镍原子形成的正八面体中。整个晶体可以看作是呈面心立方点阵排布的Ni2+和同样呈面心立方的O2−交错而成,只是两个点阵的基元位置不同[2]。
制备与性质
一氧化镍可通过多种方法制取。在400度以上,镍的粉末可以和氧气生成一氧化镍和三氧化二镍的混合物[1]。在1000度左右镍可以和水反应生成一氧化镍,若有一氧化镍加入可以提高这一反应的速率[3]。
目前最普遍和成功的制备方法是加热分解多种镍的二价化合物,比如氢氧化镍(Ni(OH)2)、硝酸镍(Ni(NO3)2)和碳酸镍(NiCO3)来制取一氧化镍。
- Ni(NO3)2 → 2 NiO + 4 NO2 + O2 硝酸镍的热解
- NiCO3 → NiO + H2O + CO2 碳酸镍的热解
一氧化镍室温具有反磁性,磁矩为1.3玻尔磁子。不溶于水,可以与酸反应,但高温煅烧过的一氧化镍不易与酸反应。一氧化镍具有一定的氧化性,可以被还原性物质如氢气、一氧化碳还原为金属镍[1]。
- NiO+H2 → Ni+H2O
用途

陶瓷与玻璃
一氧化镍是浅绿色或黑色的粉末,所以最早被用于调配给陶瓷上色的釉料,但由于一氧化镍在烧制过程中会发生氧化反应而变色,所以带有高含量一氧化镍釉料的瓷器会在烧结过程中变色,不容易取得所需的颜色。此外,由于可以增加金属表面和釉料之间的亲和性,一氧化镍也被用于搪瓷生产中[4]。
加入一氧化镍可以使玻璃变色,同时改变玻璃的结构和性质,减弱玻璃对紫外部分的吸收,增大玻璃对可见光部分的吸收,比如制造滤过紫外线灯常用的伍德玻璃,即是在含钡的玻璃里加入9%的一氧化镍,吸收掉可见光的部分,使得发射出的灯光几乎都是波长为320-400纳米的长波紫外线,可用于检查真菌感染[5] [6]。
参考文献
- 张青莲. . 北京: 科学出版社. : P360. ISBN 7-03-002238-6.
- . [2011-07-10]. (原始内容存档于2021-05-14).
- "Handbook of Inorganic Chemicals", Pradniak, Pradyot; McGraw-Hill Publications,2002
- Cameron G. Harman, Burnham W. King,Applications of Nickel Compounds in Ceramics,Industry & Engineering Chemistry, 1952, Vol 44, Issue 5,page 1015-1017
- . [2011-07-09]. (原始内容存档于2012-04-02).
- Tony Burns; Stephen Breathnach; Neil Cox; Christopher Griffiths. . John Wiley and Sons. 2010: 5– [14 November 2010]. ISBN 9781405161695.
- . [2011-07-09]. (原始内容存档于2011-05-20).
- . [2011-07-09]. (原始内容存档于2016-03-05).
- "Handbook of Inorganic Chemicals", Pradniak, Pradyot; McGraw-Hill Publications,2002
- K. Nakaoka et al. Journal of Electroanalytical Chemistry,vol 571,issue 1,page 93-99
- Hans G. Seiler,Handbook on metals in clinical and analytical chemistry,1994,509,ISBN:0-824749094-4
- "Toxicology and Carcinogenesis Studies of Nickel Oxide", U.S. Dept. of Health and Human Services, No. 451, 07/1996