溴化镍
| 溴化镍 | |
|---|---|
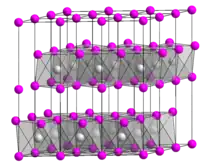 | |
_bromide_crystals_in_an_ampoule.jpg.webp) | |
 | |
| IUPAC名 Nickel(II) bromide | |
| 识别 | |
| CAS号 | 13462-88-9 |
| PubChem | 278492 |
| 性质 | |
| 化学式 | NiBr2 |
| 218.53 g/mol g·mol⁻¹ | |
| 外观 | 黄色固体(无水) 绿色晶体(六水)[1] |
| 氣味 | 无臭 |
| 密度 | 5.098 g/cm3 |
| 熔点 | 963 °C(1,236 K)(升华) |
| 溶解性(水) | 122 g/100ml (10 °C) 134 g/100ml (25 °C) |
| 溶解性 | 可溶于乙醇 |
| 危险性 | |
| 主要危害 | Irritant, corrosive |
| NFPA 704 |
 0
1
0
|
| 闪点 | 不可燃 |
| 相关物质 | |
| 其他阴离子 | 氟化镍 氯化镍 碘化镍 |
| 其他阳离子 | 溴化钴 溴化铜 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
制备
- Ni + Br2 → NiBr2
利用氢溴酸和氢氧化镍、碳酸镍反应,蒸發结晶,可以得到溴化镍的水合物:
- 2 HBr + Ni(OH)2 → NiBr2 + 2H2O
- 2 HBr + NiCO3 → NiBr2 + H2O + CO2↑
1,2-二溴乙烷和30%的氯化镍水溶液反应,可以制备溴化镍。这一反应避免了使用具有强腐蚀性的氢溴酸。反应时1,2-二溴乙烷过量至3倍摩尔比,以四丁基溴化铵为相转移催化剂,不额外加溶剂:[2]
- NiCl2 + CH2BrCH2Br → NiBr2 + CH2ClCH2Cl
用途
溴化镍可以和α-二亚胺形成配合物,用于催化乙烯聚合。[3]
参考文献
- 无机化学丛书. 第九卷. 锰分族 铁系 铂系. 科学出版社. pp 357. 表3.9 卤化镍; pp 358. 溴化镍(II)
- 张敬畅 等. 溴化镍制备方法的改进. 北京化工大学学报, 1998. 25(2): 64-68
- 义建军, 许学翔, 陈伟 等. 镍配合物[N,N]NiBr2的合成及其催化乙烯齐聚研究. 催化学报, 2002. 23(1): 69-71
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.