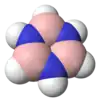
环硼氮烷
環硼氮烷(英語:)是一種非極性[2]的无机化合物,化学式为B3N3H6。該環狀化合物的結構中有三個B-H單元和三個N-H單元交替出現。它是苯的等电子体,故有時被稱為無機苯。與苯一樣,环硼氮烷是一種具有芳香氣味的無色液體。[3]
| 环硼氮烷 | |||
|---|---|---|---|
 | |||
| |||
| IUPAC名 1,3,5,2,4,6-Triazatriborinane 1,3,5,2,4,6-三氮雜三硼烷(僅預選[1]) | |||
| 别名 | 環硼氮六烷 硼氮六環 無機苯 硼嗪 | ||
| 识别 | |||
| CAS号 | 6569-51-3 | ||
| PubChem | 138768 | ||
| ChemSpider | 122374 | ||
| SMILES |
| ||
| InChI |
| ||
| InChIKey | BGECDVWSWDRFSP-UHFFFAOYAU | ||
| ChEBI | 33119 | ||
| 性质 | |||
| 化学式 | B3H6N3 | ||
| 80.50 g·mol⁻¹ | |||
| 外观 | 无色液体 | ||
| 密度 | 0.81 g/cm3 | ||
| 熔点 | −58 °C(215 K) | ||
| 沸点 | 53 °C(326 K) | ||
| 磁化率 | -49.6·10−6 cm3/mol | ||
| 危险性 | |||
| NFPA 704 |
 2
2
1
| ||
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |||
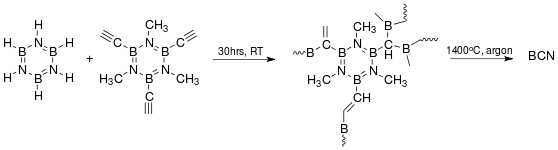
合成
在1926年,化學家Alfred Stock和Erich Pohland通過乙硼烷與氨的反應合成了環硼氮烷。[4]
環硼氮烷可以通過乙硼烷和氨按1:2比例在250-300°C下反应合成,轉化率为50%。
- 3 B2H6 + 6 NH3 → 2 B3H6N3 + 12 H2
- 6 NaBH4 + 3 (NH4)2SO4 → 2 B3N3H6 + 3 Na2SO4 + 18 H2
在兩步法中,三氯化硼先轉化為三氯环硼氮烷:
- 3 BCl3 + 3 NH4Cl → B3Cl3H3N3 + 9 HCl
再使用硼氢化钠还原:
- 2 B3Cl3H3N3 + 6 NaBH4 → 2 B3H6N3 + 3 B2H6 + 6 NaCl
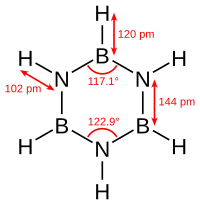
結構
環硼氮烷與苯為等電子體,具有相似的性質,因此有時也被稱為無機苯。由於硼和氮之間的電負性差異,它們並不完全相同。X射線晶體學結構測定表明,環硼氮烷內的鍵長都等於1.429Å,與苯性質相同。[6]然而,環硼氮烷並沒有形成完美的六邊形。硼原子的鍵角為117.1°,氮原子的鍵角為122.9°,使分子具有D3h對稱點群。
與氮的電負性(鮑林標度3.04)相比,硼的電負性(2.04)以及硼的缺乏電子和氮的孤對電子有利於環硼氮烷的內消旋體結構。
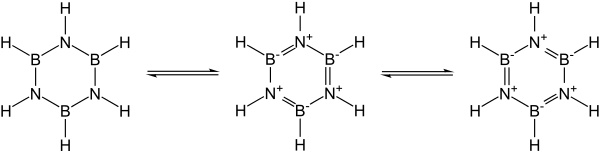
芳香性
由於環硼氮烷與苯的相似性,因此對其芳香性進行了許多計算和實驗分析。環硼氮烷的π電子數遵從4n+2規則,B-N鍵長相等,表明其可能是芳香族化合物。然而硼和氮之間的電負性差異導致電荷共享不均,從而導致鍵具有更大的離子特性,因此預計其電子離域比全碳類似物差。環硼氮烷的標準生成焓變化量ΔHf為−531 kJ/mol,熱穩定性非常好。
自然鍵軌道
自然鍵軌道理論(NBO)分析表示環硼氮烷中的芳香性較弱。[7]在NBO模型中,環中的B-N鍵略微偏離原子核軸,B和N的電荷差異較大。核獨立化學位移(NCS)分析提供了一些進一步的證據,證明基於B-N π鍵對磁屏蔽的貢獻的芳香性。基於NBO軌道的計算表明,該 π 鍵允許產生微弱的環電流,在一定程度上抵消了環硼氮烷中心模擬的磁場。一個小的環電流確實表明存在一些離域現象。
性質與用途
水解
環硼氮烷很容易水解,生成硼酸、氨和氫氣。
聚合

在70°C下加熱環硼氮烷會放出氫氣並形成聚環硼氮烷:
- n B3N3H6 → [B3N3H4]n
參考資料
- . . Cambridge: The Royal Society of Chemistry. 2014: 968. ISBN 978-0-85404-182-4. doi:10.1039/9781849733069-FP001.
- Nelson, Ralph; et al. (PDF). American National Bureau of Standards. September 1, 1967, (10): 17 [2023-01-25]. (原始内容存档 (PDF)于2018-06-08).
- Duward Shriver; Peter Atkins. Fifth. New York: W. H. Freeman and Company. 2010: 328. ISBN 978-1429218207.
- Stock A, Pohland E. [Boric acid solution, VIII Regarding knowledge of B2H6 and B5H11]. Berichte. October 1926, 59 (9): 2210–2215. doi:10.1002/cber.19260590906 (德语).
- Wideman, Thomas; Fazen, Paul J.; Lynch, Anne T.; Su, Kai; Remsen, Edward E.; Sneddon, Larry G. . . Inorganic Syntheses 32. 1998: 232–242. ISBN 9780470132630. doi:10.1002/9780470132630.ch39.
- Boese R, Maulitz AH, Stellberg P. . Chemische Berichte. 1994, 127 (10): 1887–1889. doi:10.1002/cber.19941271011.
- Shen W, Li M, Li F, Wang S. . Inorg. Chim. Acta. 2007, 360 (2): 619–624. doi:10.1016/j.ica.2006.08.028.
- Santos JC, Tiznado W, Contreras R, Fuentealba P. . The Journal of Chemical Physics. January 2004, 120 (4): 1670–3. Bibcode:2004JChPh.120.1670S. PMID 15268298. doi:10.1063/1.1635799. hdl:10533/175272
 .
. - Islas R, Chamorro E, Robles J, Heine T, Santos JC, Merino G. . Struct. Chem. 2007, 18 (6): 833–839. S2CID 95098134. doi:10.1007/s11224-007-9229-z.
- Kidambi PR, Blume R, Kling J, Wagner JB, Baehtz C, Weatherup RS, et al. . Chemistry of Materials. November 2014, 26 (22): 6380–6392. PMC 4311958
 . PMID 25673919. doi:10.1021/cm502603n.
. PMID 25673919. doi:10.1021/cm502603n. - Kim G, Jang AR, Jeong HY, Lee Z, Kang DJ, Shin HS. . Nano Letters. April 2013, 13 (4): 1834–9. Bibcode:2013NanoL..13.1834K. PMID 23527543. doi:10.1021/nl400559s.
- Chatterjee S, Luo Z, Acerce M, Yates DM, Johnson AT, Sneddon LG. . Chemistry of Materials. 2011-10-25, 23 (20): 4414–4416. ISSN 0897-4756. doi:10.1021/cm201955v (英语).
- Caneva S, Weatherup RS, Bayer BC, Brennan B, Spencer SJ, Mingard K, et al. . Nano Letters. March 2015, 15 (3): 1867–75. Bibcode:2015NanoL..15.1867C. PMC 4358078
 . PMID 25664483. doi:10.1021/nl5046632.
. PMID 25664483. doi:10.1021/nl5046632. - Davis BL, Dixon DA, Garner EB, Gordon JC, Matus MH, Scott B, Stephens FH. . Angewandte Chemie. 2009, 48 (37): 6812–6. OSTI 960522. PMID 19514023. doi:10.1002/anie.200900680.
- Koch EC, Klapötke TM. . Propellants, Explosives, Pyrotechnics. 2012, 37 (3): 335–344. doi:10.1002/prep.201100157.
- Kervyn S, Fenwick O, Di Stasio F, Shin YS, Wouters J, Accorsi G, et al. . Chemistry. June 2013, 19 (24): 7771–9 [2023-01-25]. PMID 23616404. S2CID 9774352. doi:10.1002/chem.201204598
 . (原始内容存档于2021-02-21).
. (原始内容存档于2021-02-21).
延伸閱讀
- Sneddon LG, Mirabelli MG, Lynch AT, Fazen PJ, Su K, Beck JS. (PDF). Pure Appl. Chem. 1991, 63 (3): 407–410 [2023-01-25]. S2CID 53629042. doi:10.1351/pac199163030407. (原始内容存档 (PDF)于2012-02-08).
- Jeon JK, Uchimaru Y, Kim DP. . Inorganic Chemistry. August 2004, 43 (16): 4796–8. PMID 15285647. doi:10.1021/ic035254a.
- Paetzold P. (PDF). Pure Appl. Chem. 1991, 63 (3): 345–350 [2023-01-25]. S2CID 53659373. doi:10.1351/pac199163030345. (原始内容存档 (PDF)于2012-07-16).
- Islas R. . Structural Chemistry. 2007, 18 (6): 833–839. S2CID 95098134. doi:10.1007/s11224-007-9229-z.
| 维基共享资源上的相关多媒体资源:环硼氮烷 |