环辛烷
| 环辛烷 | |
|---|---|
 | |
 | |
| 英文名 | |
| 识别 | |
| CAS号 | 292-64-8 |
| PubChem | 9266 |
| ChemSpider | 8909 |
| SMILES |
|
| InChI |
|
| InChIKey | WJTCGQSWYFHTAC-UHFFFAOYAO |
| 性质 | |
| 化学式 | C8H16 |
| 112.21 g·mol⁻¹ | |
| 外观 | 无色液体 |
| 密度 | 0.834 g/cm3 |
| 熔点 | 14.3 °C |
| 沸点 | 149 °C |
| 溶解性(水) | 7.90 mg/L (20°C) |
| 蒸氣壓 | 5.5 hPa (20°C) |
| 折光度n D |
1.4586 |
| 危险性 | |
欧盟危险性符号 有害 Xn 有害 Xn 危害环境N 危害环境N | |
| 警示术语 | R:R10, R50/53, R65 |
| 安全术语 | S:S61, S62 |
| 闪点 | 90 °C |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
构象
Hendrickson认为环辛烷分子存在多个能量相当的构象,因此其构象分析无疑是环烷烃中最复杂的。他指出,在所有构象之中,下图所示的船型-椅型构象 (Ⅰ)能量最低,是最稳定的形式。[2] Allinger等证实了这个结论。[3] 与Ⅰ相比之下,冠型结构 (Ⅱ)[4] 稳定性略差。
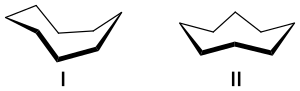 环辛烷的船型-椅型构象(Ⅰ)和王冠型结构(Ⅱ)。
环辛烷的船型-椅型构象(Ⅰ)和王冠型结构(Ⅱ)。
化学性质
化学性质不活泼。最常见的反应是燃烧反应和自由基卤化反应。最近研究发现,环辛烷可在过氧化二异丙苯作用下,与硝基苯发生反应,官能化在环烷烃上引入一个苯氨基基团。[6]
 用硝基苯对环辛烷进行胺化作用
用硝基苯对环辛烷进行胺化作用
参考资料
- Mackay, Donald. . CRC Press. 2006: 258 [2009-09-04]. ISBN 1566706874. (原始内容存档于2012-11-13).
- Hendrickson, James B. . Journal of the American Chemical Society. 1967, 89 (26): 7036–7043. doi:10.1021/ja01002a036.
- Dorofeeva, O.V.; Mastryukov, V.S.; Allinger, N.L.; Almenningen, A. . The Journal of Physical Chemistry. 1985, 89 (2): 252–257 [2008-02-05]. doi:10.1021/j100248a015. (原始内容存档于2020-01-09).
- 國際純化學和應用化學聯合會,化學術語概略,第二版。(金皮書)(1997)。在線校正版: (2006–) "crown conformation"。doi:10.1351/goldbook.C01422
- . 化工引擎. [2009-09-04]. (原始内容存档于2016-03-04).
- Deng, Guojun; Wenwen Chen, Chao-Jun Li. . Advanced synthesis & catalysis. February 2009, 351: 353–356. doi:10.1002/adsc.200800689.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.