碘化鍶
碘化鍶(SrI2),由鍶和碘元素構成的鹽,離子化合物,可溶於水,易潮解,在製藥中可用於替代碘化鉀[4]。
| 碘化鍶 | |
|---|---|
 | |
| IUPAC名 碘化鍶 | |
| 识别 | |
| CAS号 | 10476-86-5(無結晶水) |
| SMILES |
|
| RTECS | WK9275000 |
| 性质 | |
| 化学式 | SrI2(無結晶水) SrI2·6H2O(六水合物) |
| 341.43 (無結晶水) g·mol⁻¹ | |
| 外观 | 無色至白色晶體 |
| 密度 | 5.459 g/cm³(無結晶水) 4.415g/cm³(六結晶水) |
| 熔点 | 507-645°C [1] |
| 沸点 | 1773 °C (分解) |
| 溶解性(水) | 64.0 g/100 mL (20°C)[2] |
| 溶解性(乙醇) | 3.1 g/100 ml (4°C) [2] |
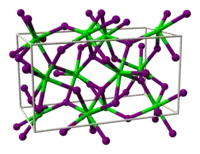
| 结构 | |
| 晶体结构 | 斜方晶系, oP24 |
| 空间群 | Pbca, No. 61 |
| 危险性 | |
| 警示术语 | R:R14 R34 |
| 安全术语 | S:S22 S26 S27 S36/37/39S45 [3] |
| 主要危害 | 腐蚀性 |
| NFPA 704 |
 0
1
0
|
| 相关物质 | |
| 其他阴离子 | 氟化鍶 氯化鍶 溴化鍶 |
| 其他阳离子 | 碘化鈹 碘化鎂 碘化鈣 碘化鋇 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
反應
碘化鍶可由碳酸鍶和碘化氫反應制備,相關反應方程式如下:
- SrCO3 + 2HI → SrI2 + H2O + CO2
當暴露於空氣中時,碘化鍶會發黃。純淨的碘化鍶更柔軟和有韌性,而剛暴露時其表面出現粉紅色或桃色。可用於導電和導熱,建築物料,和各種合金的造成部分。在高溫下(有空氣),碘化鍶完全分解,生成氧化鍶和自由的碘[5]。
參考資料
- Turner, Jr., Francis M. (编), , New York: The Chemical Catalog Company: 449, 1920 [2007-12-10]
-
177 g.100 mL (20 °C) Seidell, Atherton, , New York: D. Van Nostrand: 318, 1907 [2007-12-10] - 400696 Strontium iodide anhydrous, beads, −10 mesh, 99.99+ %
- Shoemaker, John V., 7th, Philadelphia: F. A. Davis: 854, 1908 [2007-12-10]
- Bartley, Elias H., 5th, Philadelphia: P. Blakiston: 267–268, 1898 [2007-12-10]
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.