过氧化锌
| 过氧化锌 | |
|---|---|
 | |
| 英文名 | |
| 别名 | 二氧化锌 |
| 识别 | |
| CAS号 | 1314-22-3 |
| PubChem | 10129902 |
| EINECS | 215-226-7 |
| 性质 | |
| 化学式 | ZnO2 |
| 97.408 g·mol⁻¹ | |
| 外观 | 白色至微黄色粉末 |
| 密度 | 1.57 g/cm3 |
| 熔点 | 212°C 分解 |
| pKa | ~7 (3%溶液) |
| 能隙 | 3.8 eV (间接) [1][2] eV |
| 结构 | |
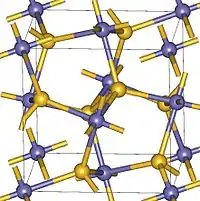
| 晶体结构 | 立方晶系 |
| 空间群 | Pa-3 |
| 危险性 | |
欧盟危险性符号 氧化性 O 氧化性 O | |
| 警示术语 | R:R9 |
| 安全术语 | S:S17, S24/25, S27 |
| NFPA 704 |
 0
3
1
|
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
性质
过氧化锌是白色至微黄色的粉末,无臭无味。微溶于水,并水解为过氧化氢和氢氧化锌。遇稀酸分解放出过氧化氢。pH 低于5时较易溶解。单独受热至150℃以上时迅速分解为氧化锌和氧,但如果存在湿的有机物或过渡金属如 或 时,在室温或略高于室温,过氧化锌就会迅速分解。[3]
过氧化锌是一种强氧化剂,与有机物接触可以发生燃烧。商品一般为白色粉末,其中过氧化锌和氧化锌大约各占一半。
X射线结果表明过氧化锌是一种真正的过氧化物, 与 离子排列成立方的黄铁矿结构,Zn-O 键长 211±1 pm,O-O 键长 148±3 pm,体积模量 174 GPa,在 5K 以上呈顺磁性。[4] 过氧化锌晶体的键具有明显的共价键性质。[3]
潮湿空气中,加热过氧化锌至200℃会生成少量的超氧化锌(Zn(O2)2)。产物超氧化锌只有与过氧化锌形成固熔体时才是稳定的。它的生成必定伴随着阳离子空穴的生成。
参考资料
- A.L. Companion. . Journal of Physics and Chemistry of Solids. 1962, 23: 1685. doi:10.1016/0022-3697(62)90205-6.
- D. Sebőka, T. Szabóa and I. Dékány. . Applied Surface Science. 2009, 255: 6953–6962. doi:10.1016/j.apsusc.2009.03.020.
- 吕云阳,王文绍,刘颂禹,季振平. . 北京: 科学出版社. 1995年12月: 719–720. ISBN 7-03-003647-6.
- W. Chen; et al. . J. Phys. Chem. C. 2009, 113: 1320. doi:10.1021/jp808714v.
- Akiba, M.; and A. S. Hashim. . Progress in Polymer Science. 1997, 22: 475–521. doi:10.1016/S0079-6700(96)00015-9.
- R. Hagel, K. Redecher, Patent US4363679-A, 1981
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.