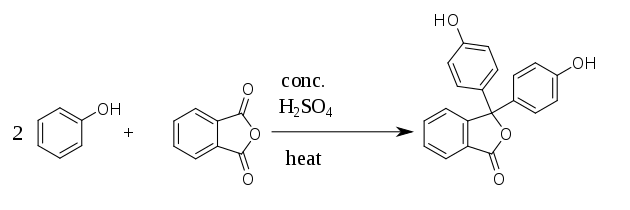
酚酞
酚酞(英語:)是一種化合物,分子式為C20H14O4,通常以简写形式写成“PP”、“HIn”、“HPh”、“phph”或简称为“Ph”。酚酞通常用作酸鹼指示劑。酚酞在酸性溶液中变为无色,在碱性溶液中变为粉红色。
| 酚酞 | |
|---|---|
 | |
 | |
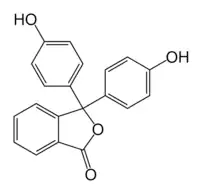
| IUPAC名 3,3-Bis(4-hydroxyphenyl)-2-benzofuran-1(3H)-one 3,3-雙(4-羥基苯基)-2-(3H)-苯並呋喃酮 | |
| 识别 | |
| CAS号 | 77-09-8 |
| PubChem | 4764 |
| SMILES |
|
| DrugBank | DB04824 |
| KEGG | D05456 |
| 性质 | |
| 化学式 | C20H14O4 |
| 318.323 g·mol⁻¹ | |
| 密度 | 1.277 g cm−3, 32 ℃ |
| 熔点 | 258℃~263℃([1]) |
| 溶解性(水) | 400mg/L |
| 溶解性(其他溶剂) | 不溶于苯,易溶于乙醇和醚,微溶于DMSO |
| λmax | 552 nm (1st) 374 nm (2nd) [1] nm |
| 危险性 | |
欧盟危险性符号 有害 Xn 有害 Xn | |
| 警示术语 | R:R22, R40, R45, R62, R68, |
| 安全术语 | S:S53, S45 |
GHS危险性符号 [1] [1] | |
| GHS提示词 | danger |
| H-术语 | H341, H350, H361[1] |
| P-术语 | P201, P281, P308+313[1] |
| NFPA 704 |
 3
2
0
|
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
酚酞微溶于水,通常溶解在醇中以用于实验。它是一种弱酸,可在溶液中失去H+离子。酚酞分子是无色的,失去质子的酚酞离子是紫红色的。其在较高pH中会进一步失去质子并导致褪色。浓硫酸中的酚酞离子是由于磺化引起的橙红色。[2]
用途
酸碱指示剂
| 酚酞(酸碱指示剂) | ||
| 低於pH 8.3 时 | 高於pH 10.0 时 | |
| 8.3 | ⇌ | 10.0 |
酚酞的常见用途是作为酸碱指示剂。其与甲基红、溴百里酚蓝和百里酚蓝一起作为通用指示剂的成分。[3]
酚酞在水溶液中根据溶液的pH產生不同的形式。[2][4][5][6]
文献中关于化合物的水合形式和硫酸中的颜色存在不一致。Wittke在1983年报告称,在强酸性条件下,其以质子化形式(HIn+)存在而呈现橙色。然而后来的论文表明,这种颜色是由于其被磺化为酚磺酞。[2]
在强酸性和弱碱性条件之间,内酯形式(HIn)是无色的。双去质子化(In2-)酚盐形式(苯酚的阴离子形式)產生熟悉的粉红色。在强碱性溶液中,酚酞转化为In(OH)3-形式,其粉红色会经历相当缓慢的褪色反应[6],当pH值大于13时变为完全无色。 酚酞的pKA值为9.05、9.50 和12,而酚磺酞的pKA值为1.2和7.70。[2]
| H3In+ | H2In | In2− | In(OH)3− | |
| 结构 |  | 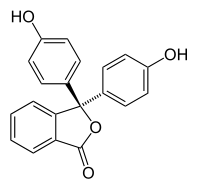 | 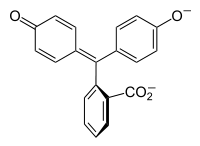 | 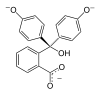 |
| 球棍模型 | 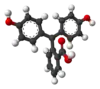 | 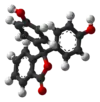 | 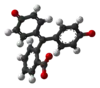 | 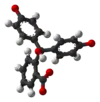 |
| pH | <-1 在H2SO4中[4] | 0−8.3 | 8.3−10.0[7] | >12 |
| 条件 | 强酸性 | 酸性、近中性 | 碱性 | 强碱性 |
| 颜色 | 橙色 | 无色 | 粉红色至品红色 | 无色 |
| 图片 |  |  |
 |
| 酚酞結構隨pH值的變化動畫: H3In+ → H2In → In2− → In(OH)3− |
参考资料
- . [2014-10-07]. (原始内容存档于2015-11-08).
- Tamura, Zenzo. . Analytical Sciences. December 1996, 12 (6): 927–930. doi:10.2116/analsci.12.927.
- . . (原始内容存档于September 25, 2006).
- Wittke, Georg. . Journal of Chemical Education. 1 March 1983, 60 (3): 239. Bibcode:1983JChEd..60..239W. ISSN 0021-9584. doi:10.1021/ed060p239.
- Abdel-Hamid, Refat. . Monatshefte für Chemie - Chemical Monthly. 1 September 1998, 129 (8): 817–826. S2CID 92339258. doi:10.1007/PL00013491.
- Kunimoto, Ko-Ki. . Spectrochimica Acta, Part A: Molecular and Biomolecular Spectroscopy (SAA). February 2001, 57 (2): 265–271. Bibcode:2001AcSpA..57..265K. PMID 11206560. doi:10.1016/S1386-1425(00)00371-1.
- Rathod, Balraj B.; Murthy, Sahana; Bandyopadhyay, Subhajit. . Journal of Chemical Education. 20 February 2019, 96 (3): 486–494. Bibcode:2019JChEd..96..486R. S2CID 104475433. doi:10.1021/acs.jchemed.8b00708.
- Dunnick, J. K.; Hailey, J. R. (PDF). Cancer Research. 1996, 56 (21): 4922–4926 [2022-02-22]. PMID 8895745. (原始内容存档 (PDF)于2022-02-17).
- Tice, R. R.; Furedi-Machacek, M.; Satterfield, D.; Udumudi, A.; Vasquez, M.; Dunnick, J. K. . Environmental and Molecular Mutagenesis. 1998, 31 (2): 113–124. PMID 9544189. doi:10.1002/(SICI)1098-2280(1998)31:2<113::AID-EM3>3.0.CO;2-N.
- Spiller, H. A.; Winter, M. L.; Weber, J. A.; Krenzelok, E. P.; Anderson, D. L.; Ryan, M. L. . The Annals of Pharmacotherapy. May 2003, 37 (5): 636–639. PMID 12708936. S2CID 31837142. doi:10.1345/aph.1C439.
- Cooper, G. S.; Longnecker, M. P.; Peters, R. K. . Pharmacoepidemiology and Drug Safety. 2004, 13 (1): 35–39 [2019-06-26]. PMID 14971121. S2CID 24783082. doi:10.1002/pds.824. (原始内容存档于2022-01-26).
- . echa.europa.eu. [2017-11-06]. (原始内容存档于2018-06-12) (英国英语).
- Baeyer, A. . Berichte der Deutschen Chemischen Gesellschaft. 1871, 4 (2): 555–558 [2020-09-02]. doi:10.1002/cber.18710040209. (原始内容存档于2021-02-14).
- Baeyer, A. . Berichte der Deutschen Chemischen Gesellschaft. 1871, 4 (2): 658–665 [2019-06-26]. doi:10.1002/cber.18710040247. (原始内容存档于2021-10-11).
- Baeyer, A. . Polytechnisches Journal. 1871, 201 (89): 358–362 [2022-02-22]. (原始内容存档于2021-10-11).
- Max Hubacher, 美國專利第2,192,485号 (1940 to Ex Lax Inc)
- 美國專利第2,522,939号
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.