阿姆斯特朗酸
阿姆斯特朗酸(英文:;學名:1,5-萘二磺酸())是化學式為 C10H6(SO3H)2 的有機化合物。阿姆斯特朗酸是萘二磺酸的數種同分異構物之一。無色固體,一般為四水合物。[1]它和其他磺酸一樣都是強酸。它是以英國化學家亨利·愛德華·阿姆斯特朗之姓氏來命名。[2]
| 阿姆斯特朗酸 | |
|---|---|
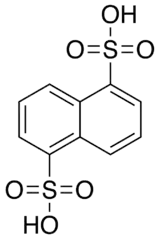 | |
| IUPAC名 Naphthalene-1,5-disulfonic acid | |
| 别名 | Armstrong's acid |
| 识别 | |
| CAS号 | 81-04-9 |
| PubChem | 6666 |
| ChemSpider | 6414 |
| SMILES |
|
| InChI |
|
| InChIKey | XTEGVFVZDVNBPF-UHFFFAOYAR |
| ChEBI | 30890 |
| 性质 | |
| 化学式 | C10H8S2O6 |
| 288.299 g/mol g·mol⁻¹ | |
| 外观 | 無色固體 |
| 危险性 | |
| 主要危害 | corrosive |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
反應
阿姆斯特朗酸可與氫氧化鈉融合生成二鈉鹽1,5-二羥基萘,並可進一步酸化生成二醇。這個水解反應的中間產物1-羥基萘-5-磺酸()也十分有用。阿姆斯特朗酸亦可硝化生成氨基衍生物的前體:硝化雙磺酸。
二鈉鹽有時可作為形成鹼性藥物鹽的二價抗衡離子,並作為替代甲磺酸酯或對甲苯磺醯基的相關鹽類。二鈉鹽也可以用作在某些種類的色譜法的電解質。[3]
參考文獻
- Booth, Gerald. . . Weinheim, Germany: Wiley-VCH Verlag GmbH & Co. KGaA: a17_009. 2000-06-15 [2021-10-09]. ISBN 978-3-527-30673-2. doi:10.1002/14356007.a17_009. (原始内容存档于2022-04-19) (英语).
- Senning, Alexander. . Elsevier. 2006-10-30 [2021-10-09]. ISBN 978-0-08-048881-3. (原始内容存档于2021-10-09) (英语).
- Terabe, Shigeru. . TrAC Trends in Analytical Chemistry. 1989-04, 8 (4): 129–134 [2021-10-09]. doi:10.1016/0165-9936(89)85022-8. (原始内容存档于2020-11-06) (英语).
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.