高碘酸盐
高碘酸盐 /pəˈraɪ.ədeɪt/ 是一种阴离子 ,由碘和氧组成。它是碘含氧阴离子里碘可以达到的最高氧化态,其中碘的氧化态为 +7。不像其它高卤酸根,例如高氯酸根,高碘酸根有两种形态:偏高碘酸根 IO−
4 和 原高碘酸根 IO5−
6。在这一点上,它与碲酸盐类似。 高碘酸根可以和阳离子结合,形成高碘酸盐,也就是高碘酸的盐。
| 高碘酸盐 | |
|---|---|
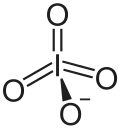 | |
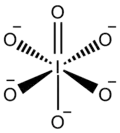 | |
| 系统名 tetraoxoiodate(1−) hexaoxoiodate(5−) | |
| 识别 | |
| CAS号 | 15056-35-6(偏高碘酸盐) |
| PubChem | 167232(偏高碘酸盐) 6857432(原高碘酸盐) |
| ChemSpider | 146311 (偏高碘酸盐), 5256770 (原高碘酸盐) |
| SMILES |
|
| InChI |
|
| InChIKey | KHIWWQKSHDUIBK-UHFFFAOYSA-M(偏高碘酸盐) TWLXDPFBEPBAQB-UHFFFAOYSA-I(原高碘酸盐) |
| 性质 | |
| 化学式 | IO4− 或 IO65- |
| 相关物质 | |
| 其他阴离子 | 高氯酸盐 高溴酸盐 高锰酸盐 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
高碘酸盐是被海因里希·马格努斯和 C. F. Ammermüller发现的。他们也在 1833年发现了高碘酸。[1]
制备
传统上,高碘酸盐最常以高碘酸氢钠(Na3H2IO6)的形式产生。 [2] 这是可商购的,但是也可以通过用氯和氢氧化钠来氧化碘酸盐来生产。 [3] 用溴代替氯来氧化碘化物也是可行的。
- NaIO3 + Cl2 + 4 NaOH → Na3H2IO6 + 2 NaCl + H2O
- NaI + 4 Br2 + 10 NaOH → Na3H2IO6 + 8 NaBr + 4 H2O
现代工业规模生产涉及在PbO2阳极上碘酸盐的电化学氧化,并具有以下标准电极电位:
偏高碘酸盐一般由硝酸来对高碘酸氢钠进行脱水而成的。[2]在 100 °C 的真空下,高碘酸氢钠也可以脱水成高碘酸盐。
- Na3H2IO6 + 2 HNO3 → NaIO4 + 2 NaNO3 + 2 H2O
- H5IO6 → HIO4 + 2 H2O
它们也可以由碘酸盐和强氧化剂如:次氯酸盐反应而成:
- NaIO3 + NaOCl → NaIO4 + NaCl
形态和变化
高碘酸盐可以以多种形式存在于水性介质中,其中pH是控制因素。原高碘酸盐具有许多酸解离常数。 [5][6]
H5IO6 ⇌ H
4IO−
6+ H+ pKa = 3.29 H
4IO−
6⇌ H
3IO2−
6+ H+ pKa = 8.31 H
3IO2−
6⇌ H
2IO3−
6+ H+ pKa = 11.60
原高碘酸四氢根和偏高碘酸根存在平衡。
- H
4IO−
6 ⇌ IO−
4 + 2 H2O, K = 29
由于这个原因,原高碘酸盐经常被认为是偏高碘酸盐的二水合物,[7] 写作 IO−
4·2H2O。 但是,由于H5IO6的X射线晶体学结果显示它有5个一样的I-OH基团,因此该描述并不准确。 [8]
在极端的pH值下,高碘酸盐可能会形成其他物质。 在碱性条件下,高碘酸三氢盐会脱水形成二碘酸盐。
- 2 H
3IO2−
6 ⇌ H
2I
2O4−
10 + 2 H2O, K = 820
在超强酸下,高碘酸也会被质子化,形成六氢氧化碘阳离子。[9]
- H
6IO+
6 ⇌ H5IO6 + H+, pKa = −0.8
结构和成键
不管是偏高碘酸根还是原高碘酸根,碘原子都处于超价状态,也就是可以形成超过符合八隅体规则所需要的键的数量的键。这可以用配位键进行了解释,也证实了这些分子中不存在双键。 [10]
高碘酸根的真正结构就看阳离子是什么,但是平均而言,原高碘酸盐采用略有变形的八面体结构,X射线衍射显示I–O键长为1.89 Å。 [11][8] 偏高碘酸根的结构则是变形四面体, I–O 键长为 1.78 Å。[12][13]
反应
热分解
高碘酸盐在水热条件下进行热分解,可以用于制备碘酸盐:[14]
- 2 La(H2O)3{IO4(OH)2} + 4 H5IO6 → 2 La(IO3)3·1⁄2H2O + 3 O2 + 17 H2O
裂解反应
高碘酸盐可以在各种1,2-双官能化烷烃上裂解碳-碳键。 [15][16] 最常见的例子是二醇裂解,它也是第一个被发现的(Malaprade反应)。 [17] 除二醇外,高碘酸盐还可裂解1,2-羟酮,1,2-二酮,α-酮酸,α-羟酸,氨基酸,[18] 1,2-胺醇,[19] 1,2-二胺和[20]环氧化物[21] 并形成醛,酮和羧酸。
.svg.png.webp)
烯烃也可以在Lemieux–Johnson氧化反应中被氧化和裂解。 这利用了四氧化锇的催化负载,该负载由高碘酸盐原位再生。 整个过程等同于臭氧化反应。
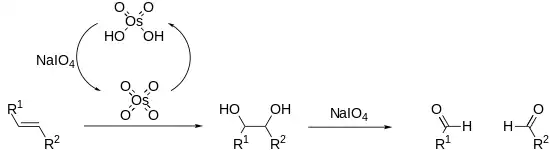
裂解反应通过称为高碘酸酯的环状中间体进行。 其形成可能受pH和温度的影响 [22] 但是底物的几何形状影响最大,cis-二醇的反应明显快于trans-二醇。 [23] 反应是放热的,并且通常在0℃下进行。 由于高碘酸盐仅易溶于水,因此反应通常在水性介质中进行。 在溶解度很重要的情况下,可以使用高碘酸,因为它可溶于醇。 相转移催化剂在多相液体混合物中反应也有效。 在极端情况下,高碘酸盐可能会交换四乙酸铅,后者以相似的方式反应并溶于有机溶剂(Criegee反应)。
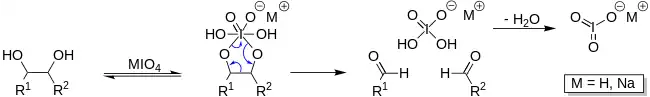
高碘酸盐裂解通常在分子生物化学中用于修饰糖类环的目的,因为许多五元和六元糖具有邻位二醇。 从历史上看,它也被用来确定单糖的结构。 [24][25]
其它含氧阴离子
高碘酸盐是碘的含氧阴离子之一。碘可以形成氧化态为 −1(其实不是), +1, +3, +5或 +7 的含氧阴离子。 一系列中性的碘的氧化物也是已知的。
| 碘的氧化态 | −1 | +1 | +3 | +5 | +7 |
|---|---|---|---|---|---|
| 名字 | 碘化物 | 次碘酸盐 | 亚碘酸盐 | 碘酸盐 | 高碘酸盐 |
| 化学式 | I− | IO− | IO− 2 |
IO− 3 |
IO− 4 或 IO5− 6 |
| 结构 |  |
参考资料
- Ammermüller, F.; Magnus, G. . Annalen der Physik und Chemie. 1833, 104 (7): 514–525. Bibcode:1833AnP...104..514A. doi:10.1002/andp.18331040709 (德语).
- Riley, edited by Georg Brauer; translated by Scripta Technica, Inc. Translation editor Reed F. 2nd. New York, N.Y.: Academic Press. 1963: 323–324. ISBN 012126601X.
- Hill, Arthur E. . Journal of the American Chemical Society. October 1928, 50 (10): 2678–2692. doi:10.1021/ja01397a013.
- Parsons, Roger. . Butterworths Scientific Publications Ltd. 1959: 71.
- Aylett, founded by A.F. Holleman; continued by Egon Wiberg; translated by Mary Eagleson, William Brewer; revised by Bernhard J. 1st English ed., [edited] by Nils Wiberg. San Diego, Calif.: Berlin: Academic Press, W. de Gruyter. 2001: 454. ISBN 0123526515.
- Burgot, Jean-Louis. . New York: Springer. : 358. ISBN 1441983821.
- Ropp, Richard C. . Oxford: Elsevier Science. : 96. ISBN 0444595538.
- Feikema, Y. D. . Acta Crystallographica. 1966, 20 (6): 765–769. doi:10.1107/S0365110X66001828.
- Greenwood, N.N.; Earnshaw, A.
 2nd. Oxford: Butterworth-Heinemann. 2006: 874. ISBN 0750633654.
2nd. Oxford: Butterworth-Heinemann. 2006: 874. ISBN 0750633654. - Ivanov, A.; Popov, A.; Boldyrev, A.; Zhdankin, V. . Angew. Chem. Int. Ed. 2014, 53: 9617–9621. doi:10.1002/anie.201405142.
- Tichý, K.; Rüegg, A.; Beneš, J. . Acta Crystallographica Section B. 1980, 36 (5): 1028–1032. doi:10.1107/S0567740880005225.
- Levason, W.; Webster, M. . Acta Crystallographica Section C. 15 June 1999, 55 (6): IUC9900052. doi:10.1107/S0108270199099394
 .
. - Kálmán, A.; Cruickshank, D. W. J. . Acta Crystallographica Section B. 1970, 26 (11): 1782–1785. doi:10.1107/S0567740870004880.
- Hydrothermal Synthesis of Rare Earth Iodates from the Corresponding Periodates: Structures of Sc(IO3)3, Y(IO3)3 · 2 H2O, La(IO3)3 · 1/2 H2O and Lu(IO3)3 · 2 H2O. doi:10.1002/1521-3749(200201)628:1<198::AID-ZAAC198>3.0.CO;2-L. ZAAC. 2002.
- Sklarz, B. . Quarterly Reviews, Chemical Society. 1967, 21 (1): 3. doi:10.1039/QR9672100003.
- Bamford, edited by C.H.; Tipper, C.F.H. . Amsterdam: Elsevier Pub. Co. 1972: 435. ISBN 9780080868011.
- L. Malaprade, Bull. Soc. Chim. Fr. 3, 1, 833 (1934)
- Clamp, J.R.; Hough, L. . The Biochemical Journal. Jan 1965, 94: 17–24. PMC 1206400
 . PMID 14342227. doi:10.1042/bj0940017.
. PMID 14342227. doi:10.1042/bj0940017. - Nicolet, Ben H.; Shinn, Leo A. . Journal of the American Chemical Society. June 1939, 61 (6): 1615–1615. doi:10.1021/ja01875a521.
- Maros, László; Molnár-Perl, Ibolya; Schissel, Enikó; Szerdahelyi, Vilmos. . Journal of the Chemical Society, Perkin Transactions 2. 1980, (1): 39. doi:10.1039/P29800000039.
- Telvekar, Vikas N.; Patel, Dharmeshkumar J.; Mishra, Sanket J. . Synthetic Communications: 311–315. doi:10.1080/00397910802372574.
- Buist, G. J.; Bunton, C. A.; Hipperson, W. C. P. . Journal of the Chemical Society B: Physical Organic. 1971: 2128. doi:10.1039/J29710002128.
- McMurry, John.
 8th ed., [international ed.] Singapore: Brooks/Cole Cengage Learning. 2012: 312. ISBN 084005453X.
8th ed., [international ed.] Singapore: Brooks/Cole Cengage Learning. 2012: 312. ISBN 084005453X. - Jackson, Ernest L.; Hudson, C. S. . Journal of the American Chemical Society. June 1937, 59 (6): 994–1003. doi:10.1021/ja01285a010.
- Robyt, John F. . New York: Springer. 1998. ISBN 0387949518.
- Yu, Jiugao; Chang, Peter R.; Ma, Xiaofei. . Carbohydrate Polymers. January 2010, 79 (2): 296–300. doi:10.1016/j.carbpol.2009.08.005.
- Weidman, S. W.; Kaiser, E. T. . Journal of the American Chemical Society. December 1966, 88 (24): 5820–5827. doi:10.1021/ja00976a024.
- Leonard, Nelson J.; Johnson, Carl R. . The Journal of Organic Chemistry. January 1962, 27 (1): 282–284. doi:10.1021/jo01048a504.
- Lemieux, R. U.; Rudloff, E. Von. . Canadian Journal of Chemistry. November 1955, 33 (11): 1701–1709. doi:10.1139/v55-208.
- Pappo, R.; Allen, Jr., D. S.; Lemieux, R. U.; Johnson, W. S. . The Journal of Organic Chemistry. 1956, 21 (4): 478–479. ISSN 0022-3263. doi:10.1021/jo01110a606.
- Dieter Weber, Róza Vöfély, Yuehua Chen, Yulia Mourzina, Ulrich Poppe: Variable resistor made by repeated steps of epitaxial deposition and lithographic structuring of oxide layers by using wet chemical etchants. Thin Solid Films (2013) DOI: 10.1016/j.tsf.2012.11.118
- Moretti, Jared D.; Sabatini, Jesse J.; Chen, Gary. . Angewandte Chemie International Edition. 9 July 2012, 51 (28): 6981–6983. PMID 22639415. doi:10.1002/anie.201202589.
- . U.S. Army. [31 October 2013]. (原始内容存档于2016-10-09).