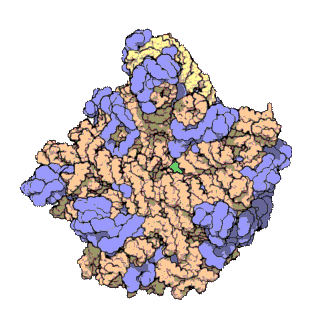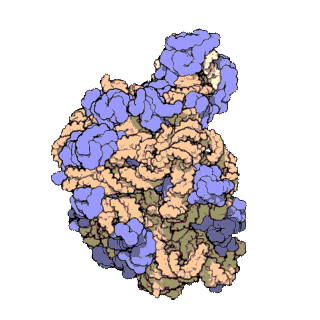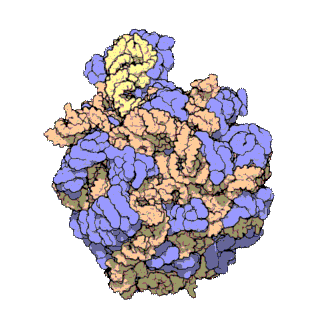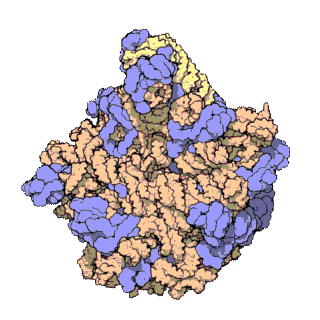
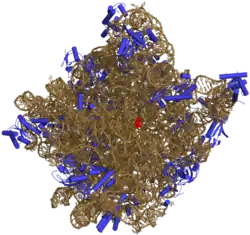
50S核糖体亚基
50核糖体亚基是原核细胞内70S核糖体中的较大亚基。该亚基由一条5S rRNA、一条23S rRNA及约34个核糖体蛋白质分子构成,在原核轉译中负责在tRNA转运来的氨基酸分子之间形成肽键。50S核核糖体亚基是某些抗生素(如氯霉素、氯洁霉素及截短侧耳素等)的结合位点,这些抗生素可通过阻断蛋白质生物合成来杀灭细菌。
组成与结构
50S核糖体亚基是70S核糖体中较大的亚基,由多种核糖体蛋白质及两种rRNA结合形成。50S核糖体亚基中的rRNA分子不仅具有二级结构,还在二级结构的基础上建立了更复杂的三级结构。50S核糖体亚基中RNA的三级结构是70S核糖体维持一定形态并产生催化活性的关键。
研究人员通过利用电子显微镜及X射线晶体学方面的技术获得了死海盐盒菌(Haloarcula marismortui)50S核糖体亚基2.4Å解析度的电子密度图。
50S核糖体亚基的质量约为30S核糖体亚基的两倍。Steitz实验室于2000年制作的50S核糖体亚基结构模型中,包含该实验室测定的50S核糖体亚基23S rRNA2923个核苷酸中的 2711个、5S rRNA中所有的共122个核苷酸及31个核糖体蛋白质中的27个。
50S核糖体亚基中的23S rRNA在二级结构上可分为六大结构域。其中,结构域Ⅴ的作用对70S核糖体肽酰转移酶活性的贡献是最大的。在三级结构的层面上看,50S核糖体亚基中的rRNA是一个独立的巨大结构域,而30S核糖体亚基中的rRNA则仍具有3个结构域。这个不同导致50S核糖体亚基的挠性比30S核糖体亚基的低,使50S核糖体亚基的结构更稳定,符合其需具备的催化功能对其结构的精确要求。
50S核糖体亚基中的蛋白质大部分都位于该亚基的表面而离活性位点较远。约17种50S核糖体亚基的蛋白质呈球形,其余约13种都是完全延展开来的或拥有凸出的延伸区域。50S核糖体亚基的大部分表面区域由核糖体蛋白质覆盖被认为可以提供自由能以固定该亚基整体结构,使其内部形成稳定的缺少蛋白质的催化区域。研究人员另发现50S核糖体亚基中的某些核糖体蛋白质位于翻译因子结合位点处,它们的可能被用于与翻译因子产生相互作用。
功能与作用机制
50S核糖体亚基具有催化肽酰转移的活性、防止合成中的肽链被水解、为G蛋白因子(用于辅助转录起始、延伸及终止提供结合位点)并辅助合成后的肽链折叠从而形成蛋白质。
转肽
研究人员利用诱导契合说解释了50S核糖体亚基如何催化肽酰转移反应并防止肽链水解[3]:
氨基酰-tRNA进入核糖体A位点,其转运的氨基酸分子的氨基便进攻在核糖体P位点的肽酰-tRNA羧基中的碳原子,使A位点中的tRNA肽链末端通过酯化反应增加一分子氨基酸并使P位点中的tRNA去酰化。
当核糖体A位点被新氨基酰-tRNA占据后,50S核糖体亚基23S rRNA的核苷酸U2620(E. coli中为2585)、A2486(2451)和C2106 (2063)将位于它们之间的羧基夹持,使其取向变为面对A位点。因为从酯基平面发起的最佳进攻角度约为105°,所以新取向能防止羧基受到任何来自A位点的亲核进攻。当具有完整CCA序列的tRNA的接纳茎结合在A位点时,该tRNA分子中的C74与核苷酸U2590(2555)发生堆叠后便诱导50S核糖体亚基产生构象上的变化,令核苷酸U2541(2506)、U2620(2585)发生越过G2618(2583)的运动。碱基之间相对位置的改变让酯基获得一个可接受来自A位点亲核进攻的新构象。
核苷酸A2486(2451)的N3是离50S核糖体亚基中正在形成的肽键最近的原子,它可能具有使A位点中的氨基酰-tRNA的氨基更易于发动亲核进攻的作用。A2486(2451)通过一种电核中继机制( charge relay mechanism)使其pKa提高5个单位并与该氨基间形成氢键以增大自身的亲核性。A2486(2451)能和与A2486(2450)嵌入的磷酸基以氢键连接的G2482(G2447)相互作用。该嵌入磷酸基可使这两个稀有的亚胺基异构化的碱基更稳定,并令N3拥有负电荷密度。
参考文献
- Ban N, Nissen P, Hansen J, Moore P, Steitz T. . Science. 2000, 289 (5481): 905–20. PMID 10937989. doi:10.1126/science.289.5481.905.
- Nissen P, Hansen J, Ban N, Moore P, Steitz T. . Science. 2000, 289 (5481): 920–929 [2011-03-05]. doi:10.1126/science.289.5481.920. (原始内容存档于2015-09-24).
- Schmeing T, Huang K, Strobel S, Steitz T. (PDF). Nature. 2005, 438: 520–524 [2011-03-05]. doi:10.1038/nature04152. (原始内容存档 (PDF)于2006-09-07).
- Basu A, Ghosh J, Bhattacharya A, Pal S, Chowdhury S, DasGupta C. (PDF). Current Science. 2003, 84: 1123–1125 [2011-03-05]. (原始内容存档 (PDF)于2004-10-31).
外部链接
- 50S核糖体亚基-抗生素复合物的资料
- 蛋白质合成抑制剂类抗生素资料(页面存档备份,存于)
- 醫學主題詞表(MeSH):23S+Ribosomal+RNA
- 醫學主題詞表(MeSH):5S+Ribosomal+RNA