细胞色素P450
细胞色素P450[1](英語:,缩写 CYP)是包含血基質(heme)作为辅因子的一个庞大的酶超家族,具单加氧酶功能[2][3][4]。在哺乳动物中,这些蛋白质氧化类固醇、脂肪酸和异生物质(外源化学物),对多种化合物的清除,以及激素的合成和分解都很重要。在植物中,这些蛋白质对于防御性化合物、脂肪酸和激素的生物合成很重要[3]。
CYP酶已在所有生命界中被发现:动物,植物,真菌,原生生物,细菌和古菌以及病毒[5]。 但是,它们并不是无处不在。 例如,在大肠杆菌中尚未发现它们[4][6] 。 已知有超过50,000种不同的CYP蛋白[7]。
CYP通常是电子转移链中的末端氧化酶,大致可归类为含P450的系统(P450-containing systems)。 术语“ P450”是从处于还原状态并与一氧化碳络合的酶的最大特征吸收波长(450 nm)处的分光光度的峰值而得名P450。 大多数CYP都需要蛋白质伴侣来传递一个或多个电子以还原铁(并且最终还原分子氧)。
大多数细胞色素P450酶的功能是催化氧化有机化合物。细胞色素P450的受質包括有:如脂质与類固醇激素的代谢中间产物,亦有药物与其他毒性化学物质等非生物物质。细胞色素P450类是涉及肝臟药物代谢与生物激活作用的主要酶类,约占到各种代谢反应总数的75%。
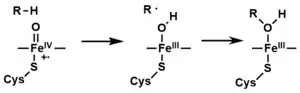
由细胞色素P450催化的最常见反应就是单加氧酶反应,例如将氧气中的一个氧原子插入到有机底物(以RH表示)中,而另一个氧原子被还原形成水:
RH + O2 + 2H+ + 2e– → ROH + H2O
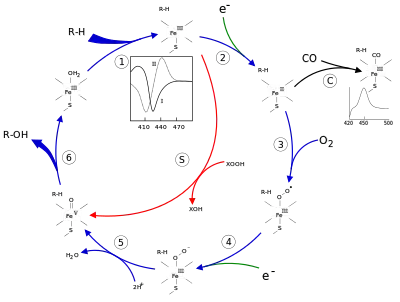
在P450催化循环。左下角的“Fe(V)中间体”是一种简化:它是带有自由基血红素配体的Fe(IV)。
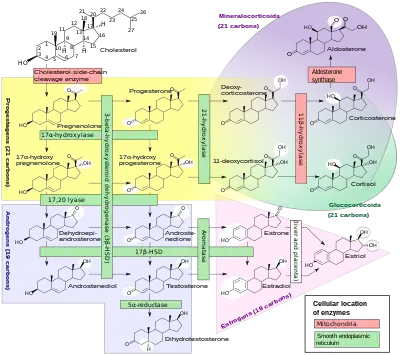
类固醇生成(Steroidogenesis),显示出细胞色素P450酶执行的许多酶活性[8] 。 HSD:羟基类固醇脱氢酶。
酶活检测
抑制剂
抑制剂强度分级规则
细胞色素P450 酶的抑制剂强度分级规则[10]如下:
- IC50 <1 μmol·L-1为强抑制剂
- 1μmol·L-1< IC50 <10μmol·L-1 为中等强度抑制剂
- 10 μmol·L-1< IC50 <100 μmol·L-1 为弱抑制剂
- IC50 >100 μmol·L-1 ,在临床上产生明显酶抑制作用的可能性较小
參見
- 类固醇生成酶
- 类固醇生成抑制剂
- 羊毛甾醇14α-脫甲基酶(Lanosterol 14 alpha-demethylase)
- 含P450的系统(P450-containing systems)
参考文献
- 汉语推荐使用规范名词,“细胞色素P450/cytochrome P450/一类以还原态与CO结合后在波长450nm处有吸收峰的含血红素的单链蛋白质” (页面存档备份,存于),全国科学技术名词审定委员会
- Gonzalez FJ, Gelboin HV. . Environmental Health Perspectives. November 1992, 98: 81–5. PMC 1519618
 . PMID 1486867. doi:10.1289/ehp.929881.
. PMID 1486867. doi:10.1289/ehp.929881. - . InterPro. [2020-06-07]. (原始内容存档于2013-05-14).
- Danielson PB. . Current Drug Metabolism. December 2002, 3 (6): 561–97. PMID 12369887. doi:10.2174/1389200023337054.
- Lamb DC, Lei L, Warrilow AG, Lepesheva GI, Mullins JG, Waterman MR, Kelly SL. . Journal of Virology. August 2009, 83 (16): 8266–9. PMC 2715754
 . PMID 19515774. doi:10.1128/JVI.00289-09.
. PMID 19515774. doi:10.1128/JVI.00289-09. - Sigel R, Sigel A, Sigel H. . New York: Wiley. 2007. ISBN 978-0-470-01672-5.
- Nelson D. . Human Genomics (University of Tennessee). 2009, 4 (1): 59–65 [2014-11-13]. PMC 3500189
 . PMID 19951895. doi:10.1186/1479-7364-4-1-59. (原始内容存档于2010-06-27).
. PMID 19951895. doi:10.1186/1479-7364-4-1-59. (原始内容存档于2010-06-27). - Häggström, Mikael; Richfield, David. . WikiJournal of Medicine. 2014, 1 (1). ISSN 2002-4436. doi:10.15347/wjm/2014.005
 .
. - 郭喻,汪晖. 人细胞色素 P450 同工酶探针底物特异性的研究进展[J]. 中国药理学通报, 2007, 23( 7) : 851 -4.
- Parmentier Y,Bossant M J,Bertrand M,et al. In vitro studies of drug metabolism[M]/ / Testa B,van de Waterbeemd H. Comprehensive Medicinal Chemistry Ⅱ - ADME- Tox Approaches. Beijing:Science Press, 2007: 246.
外部連結
| 维基共享资源上的相关多媒体资源:细胞色素P450 |
- Degtyarenko K. . International Centre for Genetic Engineering and Biotechnology. 2009-01-09 [2009-02-10]. (原始内容存档于2016-07-16).
- Estabrook R. . Drug Metab Dispos. 2003, 31 (12): 1461–73. PMID 14625342. doi:10.1124/dmd.31.12.1461.
- Feyereisen R. . Institut National de la Recherche Agronomique. 2005-12-19 [2009-02-10]. (原始内容存档于2014-05-30).
- Flockhart DA. . Indiana University-Purdue University Indianapolis. 2007 [2009-02-10]. (原始内容存档于2007-08-30).
- Fowler L, Mercer A. . School of Pharmacy, London. [2009-02-10]. (原始内容存档于2016-05-17).
- Preissner S. . Nucleic Acids Research. 2010. (原始内容存档于2011-11-03).
- Sim SC. . Karolinska Institutet. 2008-09-04 [2009-02-10]. (原始内容存档于2009-02-08).
- Hazai E. . 2012-02-12. (原始内容存档于2011-02-15).
- Performance of P450 inhibition Studies (页面存档备份,存于) The performance of in vitro cytochrome P450 inhibition studies studies including analysis of the data.
- DDI Regulatory Guidance (页面存档备份,存于) Request a guide to drug-drug interaction regulatory recommendations.
- Expanding the toolbox of cytochrome P450s through enzyme engineering (页面存档备份,存于) Video by the Turner Group, University of Manchester, UK
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.