SOX2
SRY盒-2(SRY:性別決定區,Sex Determining Region Y),又稱「Sox2」(人的Sox2應寫爲SOX2),是一種對未分化的胚胎幹細胞(ESC)、神經幹細胞等再生能力以及多能性維持至關重要轉錄因子[6]。對Sox2的研究對幹細胞生物學、再生醫學的發展有重要意義[7]。
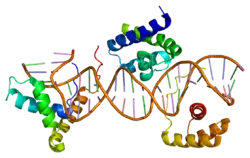
Sox2隸屬於SOX轉錄因子家族。Sox轉錄因子家族在哺乳動物的發育過程中扮演重要角色。該家族的蛋白質都有一個保守的DNA結合結構域,長約80個氨基酸殘基,稱爲高迁移率组(High-mobility group,HMG)盒結構域[6]。
功能
幹性維持
白血病抑制因子(LIF)能通過激活Sox2調控的下游,諸如JAK-STAT信號通路,繼而激活Klf4(Kruppel樣因子家族下的一種蛋白質)的表達,以維持胚胎幹細胞的幹性。Oct4、Sox2以及Nanog能增強所有LIF調控的通路相關的蛋白質的表達[8]。
Npm1是一種與細胞增殖相關的轉錄調節蛋白,在胚胎幹細胞中能與Sox2、Oct4、Nanog形成蛋白複合物[9]。Sox2、Oct4、Nanog三個轉錄因子共同組成了一個與多能性維持相關的轉錄調控網絡。Sox2能與Oct4一同與DNA非回文序列結合,以激活與多能性維持的關鍵因子轉錄[10]。令人驚訝的是,對Oct4-Sox2增強子的調控即使沒有Sox2也可以發生,可能是因爲其他Sox家族的蛋白質的表達。不過,已有研究人員確認Sox2在胚胎幹細胞幹性維持中的主要作用是控制Oct4的表達。另外,Oct4、Sox2一旦表達,就會自我維持持續表達的狀態[11]。
向體細胞中轉入Sox2加上Oct4、c-Myc、Klf4四個因子的基因就可以誘導iPSC的產生[12]。
一些Sox2、Oct4的結合位點的高甲基化以及miR134對Sox2的轉錄後抑制調控男性生殖細胞多能性丟失[13][14]。
Sox2不同的表達水平決定了胚胎幹細胞的分化命運。Sox2能抑制胚胎幹細胞分化爲中胚層、內胚層的細胞,並能促進其分化爲外胚層的神經細胞[15]。在細胞分化爲外胚層系細胞的過程中,Npm1/Sox2複合物能持續表達,說明Sox2在外胚層分化過程中發揮的重要作用[9]。
通過對基因敲除鼠的研究,已證明Sox2表達的缺失會使神經畸形,對胚胎是致死的。進一步說明Sox2對胚胎發育的重要性[16]。
神經幹細胞
神經發生過程中,Sox2在神經管細胞以及中樞神經系統祖細胞增殖過程中會表達。然而,在祖細胞退出細胞週期,進入G0期的過程中,Sox2的表達會下調[17]。細胞表達Sox2能促進細胞增殖,也能促進細胞分化爲神經細胞,而細胞增殖和分化的能力正是幹細胞的兩個最顯著的特徵。表達Sox2的(Sox2+)神經幹細胞能進行細胞分裂,產生與其相同的Sox2+神經幹細胞,同時還能產生神經細胞前體細胞[18]。
使用成體神經幹細胞(其Sox2以及c-Myc的表達水平高於胚胎幹細胞),只需要轉入兩種因子(其中一個必須是Oct4)就足以產生誘導多能性幹細胞,減少了轉入多個因子時可能產生的風險以及副作用[19]。
眼畸形
人SOX2基因突變與双眼眼球炎,一種嚴重的結構性眼畸形有關[20]。
癌症
在肺發育過程中,Sox2控制支氣管分支的形態發生以及空氣通道上皮的分化[21]。在通常情況下,Sox2對氣管上皮的基底細胞的自我更新以及比例維持至關重要。然而,Sox2的過表達會造成上皮增生,並最終在發育中以及成體小鼠體內誘發肺部癌變[22]。
鳞状细胞癌中,常常可以檢出3q26.3區基因的擴增。Sox2基因即位於該區域,說明Sox2是一種原癌基因。Sox2能誘發鱗狀細胞癌,激活許多與腫瘤發生相關的基因表達。Sox2的過表達與Lkb1的不表達能促進小鼠肺部鱗狀上皮細胞的癌變[23]。Sox2的過表達也可以激活細胞的遷移以及錨定非依賴性生長[24]。
甲狀腺激素的調控
Sox2啓動子的上游(即增強子區域)有三個甲狀腺激素應答元件(TRE),甲狀腺激素(T3)能通過這些區域下調Sox2的表達。在神經幹細胞的增殖遷移過程中,TRα1(一種甲狀腺激素的受體)的表達會上調。此現象提示甲狀腺激素能通過甲狀腺激素信號通路對Sox2進行轉錄抑制,促進神經幹細胞從腦室下區遷出並分化。人胚胎發育過程中甲狀腺激素的缺失,尤其是胚胎發育的頭三個月中的缺失,會造成中樞神經系統發育的異常。因此,可以得出結論,在胚胎發育中,甲狀腺激素水平低會造成神經性缺陷,諸如以發育不良爲特徵的呆小症[28]。
參考
- .
- GRCh38: Ensembl release 89: ENSG00000181449 - Ensembl, May 2017
- GRCm38: Ensembl release 89: ENSMUSG00000074637 - Ensembl, May 2017
- . National Center for Biotechnology Information, U.S. National Library of Medicine.
- . National Center for Biotechnology Information, U.S. National Library of Medicine.
- . NCBI. (原始内容存档于2016-01-05).
- Rizzino A. . Wiley Interdisciplinary Reviews. Systems Biology and Medicine. 2009, 1 (2): 228–36. PMC 2794141
 . PMID 20016762. doi:10.1002/wsbm.12.
. PMID 20016762. doi:10.1002/wsbm.12. - Niwa H, Ogawa K, Shimosato D, Adachi K. . Nature. July 2009, 460 (7251): 118–22. PMID 19571885. doi:10.1038/nature08113.
- Johansson H, Simonsson S. . Aging. November 2010, 2 (11): 815–22. PMC 3006024
 . PMID 21076177. doi:10.18632/aging.100222.
. PMID 21076177. doi:10.18632/aging.100222. - Chambers I, Tomlinson SR. . Development. July 2009, 136 (14): 2311–22. PMC 2729344
 . PMID 19542351. doi:10.1242/dev.024398.
. PMID 19542351. doi:10.1242/dev.024398. - Masui S, Nakatake Y, Toyooka Y, Shimosato D, Yagi R, Takahashi K, Okochi H, Okuda A, Matoba R, Sharov AA, Ko MS, Niwa H. . Nature Cell Biology. June 2007, 9 (6): 625–35. PMID 17515932. doi:10.1038/ncb1589.
- Takahashi K, Yamanaka S. . Cell. August 2006, 126 (4): 663–76. PMID 16904174. doi:10.1016/j.cell.2006.07.024.
- Imamura M, Miura K, Iwabuchi K, Ichisaka T, Nakagawa M, Lee J, Kanatsu-Shinohara M, Shinohara T, Yamanaka S. . BMC Developmental Biology. 2006, 6: 34. PMC 1564388
 . PMID 16859545. doi:10.1186/1471-213X-6-34.
. PMID 16859545. doi:10.1186/1471-213X-6-34. - Tay Y, Zhang J, Thomson AM, Lim B, Rigoutsos I. . Nature. October 2008, 455 (7216): 1124–8. PMID 18806776. doi:10.1038/nature07299.
- Thomson M, Liu SJ, Zou LN, Smith Z, Meissner A, Ramanathan S. . Cell. June 2011, 145 (6): 875–89. PMID 21663792. doi:10.1016/j.cell.2011.05.017.
- Ferri AL, Cavallaro M, Braida D, Di Cristofano A, Canta A, Vezzani A, Ottolenghi S, Pandolfi PP, Sala M, DeBiasi S, Nicolis SK. . Development. August 2004, 131 (15): 3805–19. PMID 15240551. doi:10.1242/dev.01204.
- Graham V, Khudyakov J, Ellis P, Pevny L. . Neuron. August 2003, 39 (5): 749–65. PMID 12948443. doi:10.1016/S0896-6273(03)00497-5.
- Suh H, Consiglio A, Ray J, Sawai T, D'Amour KA, Gage FH. . Cell Stem Cell. November 2007, 1 (5): 515–28. PMC 2185820
 . PMID 18371391. doi:10.1016/j.stem.2007.09.002.
. PMID 18371391. doi:10.1016/j.stem.2007.09.002. - Kim JB, Zaehres H, Wu G, Gentile L, Ko K, Sebastiano V, Araúzo-Bravo MJ, Ruau D, Han DW, Zenke M, Schöler HR. . Nature. July 2008, 454 (7204): 646–50. PMID 18594515. doi:10.1038/nature07061.
- . (原始内容存档于2010-04-13).
- Gontan C, de Munck A, Vermeij M, Grosveld F, Tibboel D, Rottier R. . Developmental Biology. May 2008, 317 (1): 296–309. PMID 18374910. doi:10.1016/j.ydbio.2008.02.035.
- Lu Y, Futtner C, Rock JR, Xu X, Whitworth W, Hogan BL, Onaitis MW. . PLoS ONE. 2010, 5 (6): e11022. PMC 2883553
 . PMID 20548776. doi:10.1371/journal.pone.0011022.
. PMID 20548776. doi:10.1371/journal.pone.0011022. - Mukhopadhyay A, Berrett KC, Kc U, Clair PM, Pop SM, Carr SR, Witt BL, Oliver TG. . Cell Reports. July 2014, 8 (1): 40–9. PMID 24953650. doi:10.1016/j.celrep.2014.05.036.
- Hussenet T, Dali S, Exinger J, Monga B, Jost B, Dembelé D, Martinet N, Thibault C, Huelsken J, Brambilla E, du Manoir S. . PLoS ONE. 2010, 5 (1): e8960. PMC 2813300
 . PMID 20126410. doi:10.1371/journal.pone.0008960.
. PMID 20126410. doi:10.1371/journal.pone.0008960. - Kregel S, Kiriluk KJ, Rosen AM, Cai Y, Reyes EE, Otto KB, Tom W, Paner GP, Szmulewitz RZ, Vander Griend DJ. . PLoS ONE. 2013, 8 (1): e53701. PMC 3543364
 . PMID 23326489. doi:10.1371/journal.pone.0053701.
. PMID 23326489. doi:10.1371/journal.pone.0053701. - Tani Y, Akiyama Y, Fukamachi H, Yanagihara K, Yuasa Y. . Journal of Cancer Research and Clinical Oncology. April 2007, 133 (4): 263–9. PMID 17136346. doi:10.1007/s00432-006-0165-x.
- Piva M, Domenici G, Iriondo O, Rábano M, Simões BM, Comaills V, Barredo I, López-Ruiz JA, Zabalza I, Kypta R, Vivanco Md. . EMBO Molecular Medicine. January 2014, 6 (1): 66–79. PMC 3936493
 . PMID 24178749. doi:10.1002/emmm.201303411.
. PMID 24178749. doi:10.1002/emmm.201303411. - López-Juárez A, Remaud S, Hassani Z, Jolivet P, Pierre Simons J, Sontag T, Yoshikawa K, Price J, Morvan-Dubois G, Demeneix BA. . Cell Stem Cell. May 2012, 10 (5): 531–43. PMID 22560077. doi:10.1016/j.stem.2012.04.008.
- Aota S, Nakajima N, Sakamoto R, Watanabe S, Ibaraki N, Okazaki K. . Developmental Biology. May 2003, 257 (1): 1–13. PMID 12710953. doi:10.1016/S0012-1606(03)00058-7.
- Shi W, Wang H, Pan G, Geng Y, Guo Y, Pei D. . Journal of Biological Chemistry. August 2006, 281 (33): 23319–25. PMID 16714766. doi:10.1074/jbc.M601811200.
拓展閱讀
- Kamachi Y, Uchikawa M, Kondoh H. . Trends in Genetics. April 2000, 16 (4): 182–7. PMID 10729834. doi:10.1016/S0168-9525(99)01955-1.
- Schepers GE, Teasdale RD, Koopman P. . Developmental Cell. August 2002, 3 (2): 167–70. PMID 12194848. doi:10.1016/S1534-5807(02)00223-X.
- Hever AM, Williamson KA, van Heyningen V. . Clinical Genetics. June 2006, 69 (6): 459–70. PMID 16712695. doi:10.1111/j.1399-0004.2006.00619.x.
- Yuan H, Corbi N, Basilico C, Dailey L. . Genes & Development. November 1995, 9 (21): 2635–45. PMID 7590241. doi:10.1101/gad.9.21.2635.
- Stevanovic M, Zuffardi O, Collignon J, Lovell-Badge R, Goodfellow P. . Mammalian Genome. October 1994, 5 (10): 640–2. PMID 7849401. doi:10.1007/BF00411460.
- Bonaldo MF, Lennon G, Soares MB. . Genome Research. September 1996, 6 (9): 791–806. PMID 8889548. doi:10.1101/gr.6.9.791.
- Helland R, Berglund GI, Otlewski J, Apostoluk W, Andersen OA, Willassen NP, Smalås AO. . Acta Crystallographica Section D. January 1999, 55 (Pt 1): 139–48. PMID 10089404. doi:10.1107/S090744499801052X.
- Güre AO, Stockert E, Scanlan MJ, Keresztes RS, Jäger D, Altorki NK, Old LJ, Chen YT. . Proceedings of the National Academy of Sciences of the United States of America. April 2000, 97 (8): 4198–203. PMC 18195
 . PMID 10760287. doi:10.1073/pnas.97.8.4198.
. PMID 10760287. doi:10.1073/pnas.97.8.4198. - Ambrosetti DC, Schöler HR, Dailey L, Basilico C. . The Journal of Biological Chemistry. July 2000, 275 (30): 23387–97. PMID 10801796. doi:10.1074/jbc.M000932200.
- Kamachi Y, Uchikawa M, Tanouchi A, Sekido R, Kondoh H. . Genes & Development. May 2001, 15 (10): 1272–86. PMC 313803
 . PMID 11358870. doi:10.1101/gad.887101.
. PMID 11358870. doi:10.1101/gad.887101. - Fantes J, Ragge NK, Lynch SA, McGill NI, Collin JR, Howard-Peebles PN, Hayward C, Vivian AJ, Williamson K, van Heyningen V, FitzPatrick DR. . Nature Genetics. April 2003, 33 (4): 461–3. PMID 12612584. doi:10.1038/ng1120.
- Wiebe MS, Nowling TK, Rizzino A. . Journal of Biological Chemistry. May 2003, 278 (20): 17901–11. PMID 12637543. doi:10.1074/jbc.M212211200.
- Aota S, Nakajima N, Sakamoto R, Watanabe S, Ibaraki N, Okazaki K. . Developmental Biology. May 2003, 257 (1): 1–13. PMID 12710953. doi:10.1016/S0012-1606(03)00058-7.
- Schepers G, Wilson M, Wilhelm D, Koopman P. . Journal of Biological Chemistry. July 2003, 278 (30): 28101–8. PMID 12732652. doi:10.1074/jbc.M304067200.
- Reményi A, Lins K, Nissen LJ, Reinbold R, Schöler HR, Wilmanns M. . Genes & Development. August 2003, 17 (16): 2048–59. PMC 196258
 . PMID 12923055. doi:10.1101/gad.269303.
. PMID 12923055. doi:10.1101/gad.269303. - Williams DC, Cai M, Clore GM. . Journal of Biological Chemistry. January 2004, 279 (2): 1449–57. PMID 14559893. doi:10.1074/jbc.M309790200.
- Tsukamoto T, Inada K, Tanaka H, Mizoshita T, Mihara M, Ushijima T, Yamamura Y, Nakamura S, Tatematsu M. . Journal of Cancer Research and Clinical Oncology. March 2004, 130 (3): 135–45. PMID 14655050. doi:10.1007/s00432-003-0519-6.
外部連結
- Young Lab- Core Transcriptional Regulatory Circuitry in Human Embryonic Stem Cells
- GeneReviews/NCBI/NIH/UW entry on SOX2-related eye disorders(页面存档备份,存于)
- Generating iPS Cells from MEFS through Forced Expression of Sox-2, Oct-4, c-Myc, and Klf4 (Journal of Visualized Experiments)(页面存档备份,存于)
- GeneReviews/NCBI/NIH/UW entry on Anophthalmia / Microphthalmia Overview(页面存档备份,存于)