X-gal
X-gal(亦可縮寫BCIG,為5 -溴-4 -氯-3 -吲哚基-β-D-吡喃半乳糖苷)是一種由半乳糖連接取代吲哚所組成的有機化合物。於1964年,由杰羅姆·霍維茨和在密歇根州底特律的合作者共同開發出合成方法。[1] 正式的化學名稱經常為了少去麻煩的短語而縮短到不準確,例如:bromochloroindoxyl半乳糖苷。這個X 吲哚酚很可能是來自X-gal收縮源中的X。X-gal多應用於分子生物學中測試β-半乳糖苷酶。它也被用來檢測組織化學和細菌學各種酶的活性。X-gal可以透過許多吲哚酚糖苷和酯,經由酶催化水解產生類似於靛藍色且不溶的藍色化合物。[2]
| X-gal | |
|---|---|
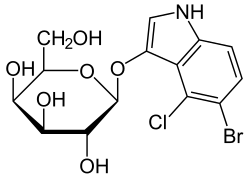 | |
| IUPAC名 5-bromo-4-chloro-3-indolyl-β-D-galactopyranoside | |
| 识别 | |
| CAS号 | 7240-90-6 |
| PubChem | 65181 |
| ChemSpider | 58680 |
| SMILES |
|
| InChI |
|
| InChIKey | OPIFSICVWOWJMJ-AEOCFKNEBZ |
| ChEBI | 75055 |
| MeSH | X-gal |
| 性质 | |
| 化学式 | C14H15BrClNO6 |
| 408.629 g·mol⁻¹ | |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
用途
X-gal的是一個模擬的乳糖,因此可以藉由β-半乳糖苷酶來對裂解D-乳糖中的β-糖苷鍵中來進行水解。X-gal當由β-半乳糖苷酶裂解,則會產生半乳糖和5-溴-4-氯-3-羥基吲哚。後者然後自發地二聚化並氧化成5,5'-二溴-4,4'-二氯靛藍,此化合物為一種不溶性的深藍色產物。X-gal的本身是無色,但產生的產物為明顯的藍色,因此可被用作測定是否有β-半乳糖苷酶的存在。這種容易識別β-半乳糖苷酶的基因(在lacZ啟動要使用的基因)的所產生的酶是否具有活性被用來當成報導基因的應用。[3]
反應
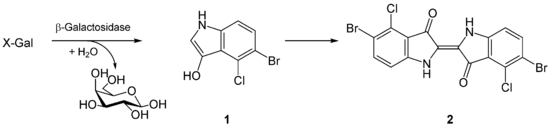
複製(克隆)
在基因的複製中,X-gal的被用作於藍/白篩的測試中,此測試為表現出細胞中之β-半乳糖苷酶是否具有活性。這種篩選方法是區別出基因複製成功的產物與失敗品的一種相當便捷的方式。
在藍/白篩選的方法中,宿主大腸桿菌菌株攜帶包含ω-肽的LacZ基因缺失突變體(lacZΔM15 ),而所用的質體攜帶lacZα序列中第59殘基的β-半乳糖苷酶α-肽。無論本身的功能性,然而,當這兩個肽一起表達,因為當該細胞含有質體被變換成lacZΔM15的lacZα的序列,所以它們得以形成一個具有功能性的β-半乳糖苷酶。
藍/白篩選方法的作用原理是通過破壞該α-互補的過程。lacZα序列內部的質體攜帶多複製端點(MCS)。這些lacZα中的MCS序列可以透過限制性內切酶進行切割,使lacZ α基因可以插入外源DNA,進而破壞該基因與製造α-肽。於是,在含有和插入的質體的細胞,會形成沒有任何功能與活性的β-半乳糖苷酶。
可以通過X-gal方式檢測到是否有有活性的β-半乳糖苷酶存在,具活性β-半乳糖苷酶可切割無色的模擬乳糖,之後形成5 -溴-4 -氯-吲哚酚,然後自發地二聚化以及氧化形成一個不溶於5,5' -二溴-4,4' -二氯靛的明亮的藍色顏料。這造成帶有β-半乳糖苷酶的細胞產生特別的藍色。藍色菌落表示它們可能含有一個不間斷的lacZα載體(因此,沒有插入外來DNA);而白色菌落,其中的X-gal不會被水解,則外源轉植物於lacZα中存在,擾亂了具有活性的β-半乳糖苷酶形成。
變種
X-gal的有許多不同的變異體,它們是相似的分子且僅具有些微的差別,主要的功能為產生顏色,並以產生藍色以外的的信號為主。
| Short name | Long name | Color |
|---|---|---|
| 藍-半乳糖,Bluo-半乳糖 | 5-溴-3-吲哚基β-D-吡喃半乳糖苷 | 深藍色[4] |
| 羅斯-半乳糖,鮭魚,半乳糖,Y-半乳糖,紅-半乳糖 | 6-氯-3-吲哚基-β-D-吡喃半乳糖苷 | 粉紅色[5] |
| 紫色-β-D-半乳糖 | 5-碘-3-吲哚基-β-D-吡喃半乳糖苷 | 紫[6] |
| 紫紅色葡萄糖苷,GLC-洋紅,品紅半乳糖 | 5-溴-6-氯-3-吲哚基-β-D-吡喃葡糖苷 | 洋紅色[7] |
| 綠-β-D-半乳糖苷酶 | N-甲基-β-D-吡喃半乳糖苷 | 綠色[8] |
| MUG, MUGA | 4-β-D-吡喃半乳糖苷甲基繖形酮酰 | 螢光(λex = 365, λem = 455) Fluorescent[9] |
參考文獻
- Horwitz JP and 7 others, 1964. Substrates for cytochemical demonstration of enzyme activity. I. Some substituted 3-indolyl-β-D-glycopyranosides. Journal of Medicinal Chemistry 7: 574-575.
- Kiernan JA 2007. Indigogenic substrates for detection and localization of enzymes. Biotechnic & Histochemistry 82(2): 73-103.
- Sandhu, Sardul Singh. . I K International Publishing House. 2010: 116. ISBN 978-9380578446.
- . [4 February 2014]. (原始内容存档于2015-06-22).
- . [4 February 2014]. (原始内容存档于2014-02-21).
- . [4 February 2014]. (原始内容存档于2014-02-21).
- . [4 February 2014]. (原始内容存档于2015-06-22).
- . [4 February 2014]. (原始内容存档于2014-02-21).
- . [4 February 2014]. (原始内容存档于2015-09-24).
- Joung J, Ramm E, Pabo C. . Proc Natl Acad Sci USA. 2000, 97 (13): 7382–7 [2014-06-18]. PMC 16554
 . PMID 10852947. doi:10.1073/pnas.110149297. (原始内容存档于2008-05-02).
. PMID 10852947. doi:10.1073/pnas.110149297. (原始内容存档于2008-05-02).