染色体
染色體(英語:),主要由雙股螺旋的去氧核糖核酸和5种被称为组蛋白的蛋白质构成,是基因的主要載體。染色体是细胞内具有遗传性质的遗传物质深度压缩形成的聚合体,易被碱性染料染成深色,所以叫染色体(由染色质组成)。染色质和染色体是同一物质在细胞分裂间期和分裂期的不同形态表现。染色体出现于分裂期。染色质出现于间期,呈丝状。其本质都是脱氧核糖核酸(DNA)和蛋白质的组合(即核蛋白组成),不均匀地分布于细胞核中 ,是遗传信息(基因)的主要载体,但不是唯一载体(如细胞质内的腺粒体)。
發現歷程
1879年,德国生物學家華爾瑟·弗萊明(Walther Flemming)称这种丝状体为染色体(英語:;希臘語:=颜色,希臘語:=体),意即可染色的小体,并猜测染色体与遗传有关。1902年,博韦里(Theodor·Boveri)和萨顿(Walter·S·Sutton)指出,染色体在细胞分裂中的行为与孟德尔的遗传因子平行:两者在体细胞中都成对存在,而在生殖细胞中则是单獨存在的;成对的染色体或遗传因子在细胞减数分裂时彼此分离,进入不同的子细胞中,不同对的染色体或遗传因子可以自由组合。因此,博韦里和萨顿认为,染色体很可能是遗传因子的载体。
結構

核小體是染色體结構的最基本单位。核小体的核心是由4對組織蛋白(H2A、H2B、H3和H4)各两个分子构成的扁球状8聚体。现在我们知道,脫氧核糖核酸分子具有典型的双螺旋结构,一个脫氧核糖核酸分子就像是一条长长的双螺旋的飘带。一条染色体有一个脫氧核糖核酸分子。脫氧核糖核酸双螺旋依次在每个组蛋白8聚体分子的表面盘绕约1.75圈,其长度相当于140个碱基对。组蛋白8聚体与其表面上盘绕的脫氧核糖核酸分子共同构成核小体。在相邻的两个核小体之间,有长约50~60个碱基对的脫氧核糖核酸连接线。在相邻的连接线之间结合着一个第5种组蛋白(H1)的分子。密集成串的核小体形成了核质中的100埃左右的纤维,这就是染色体的“一级结构”。在这里,脫氧核糖核酸分子大约被压缩了7倍。
染色体的一级结构经螺旋化形成中空的线状体,称为螺线体或称核丝,这是染色体的“二级结构”,其外径约300埃,内径100埃,相邻螺旋间距为110埃。螺丝体的每一周螺旋包括6个核小体,因此脫氧核糖核酸的长度在这个等级上又被再压缩了6倍。
300埃左右的螺线体(二级结构)再进一步螺旋化,形成直径为0.4微米的筒状体,称为超螺旋体。这就是染色体的“三级结构”。到这里,脫氧核糖核酸又再被压缩了40倍。超螺旋体进一步折叠盘绕后,形成染色单体—染色体的“四级结构”。两条染色单体组成一条染色体。到这里,脫氧核糖核酸的长度又再被压缩了5倍。从染色体的一级结构到四级结构,脫氧核糖核酸分子一共被压缩了7×6×40×5=8400倍。例如,人的染色体中脫氧核糖核酸分子伸展开来的长度平均约为几个厘米,而染色体被压缩到只有几个微米长。
现代关于染色体超微结构的概念
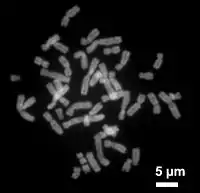
染色体的超微结构显示染色体是由直径僅100埃(A)的去氧核糖核酸-组蛋白高度螺旋化的纤维所组成。每一条染色单体可看作一条双螺旋的脫氧核糖核酸分子。有丝分裂间期时,解螺旋而形成无限伸展的细丝,此时不易为染料所着色,光镜下呈无定形物质,称之为染色质。有丝分裂时脫氧核糖核酸高度螺旋化而呈现特定的形态,此时易为碱性染料着色,称之为染色体。
1970年后陆续问世的各种显带技术对染色体的识别作出了很大贡献。中期染色体经过DNA变性、胰酶消化或荧光染色等处理,可出现沿纵轴排列的明暗相间的带纹。按照染色体上特征性的标志可将每一个臂从内到外分为若干区,每个区又可分为若干条带,每条带又再分为若干个亚带,例如“9q34.1”即表示9号染色体长臂第3区第4条带的第1个亚带。由于每条染色体带纹的数目和宽度是相对恒定的,根据带型的不同可识别每条染色体及其片段。
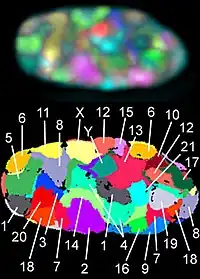
1980年代以来根据脫氧核糖核酸双链互补的原理,应用已知序列的DNA探针进行荧光原位杂交(Fluorescence in situ hybridization,FISH)可以识别整条染色体、染色体的1个臂、1条带甚至一个基因,因而大大提高了染色体识别的准确性和敏感性。染色体是遗传物质—基因的载体,控制人类形态、生理和生化等特征的结构基因呈直线排列在染色体上。由此可见,染色体和基因二者密切相关,染色体的任何改变必然导致基因的异常。
2000年6月26日人類基因组计划(HGP)已宣布完成人類基因组序列框架圖。2001年2月12日HGP和塞雷拉公司公布了人類基因组圖譜和初步分析结果。人類基因组共有3~3.5万个基因,而不是以往認為的10萬個。
形態
染色体在细胞分裂(cell division)之前才形成。在细胞的代谢期或间期,染色体分散成一级结构或伸展开的脫氧核糖核酸分子,组成细胞核内的染色质(chromatin)或核质(nucleoplasm or karyoplasm)。

染色体的形态以中期时最为典型。每条染色体由两条染色单体组成,中间狭窄处称为中節(centromere),又称主缢痕(primary constriction),它将染色体分为短臂(p)和长臂(q)。按着丝粒位置的不同,人类染色体可分为中着丝粒染色体、亚中着丝粒染色体和近端着丝粒染色体等3种类型。近端着丝粒染色体的短臂末端有一个叫做随体(satellite)的结构,它呈圆球形,中间以细丝与短臂相连。有的染色体长臂上还可看到另一些较小的狭窄区,称为次缢痕(secondary constriction)。染色体臂的末端存在着一种叫做端粒(telomere)的结构,它有保持染色体完整性的功能。
各种生物体细胞核内染色体数目
真核生物
真核细胞中細胞核外的其他染色體(例如線粒體內的小染色體或類質粒小染色體)的數量是不固定的,可能數以千計。
进行無性生殖的物種的所有細胞中只有一套染色體,這一套染色體在所有體細胞中都是相同的。
进行有性生殖的物種的體細胞中有兩套染色體,一套來自父方;一套來自母方。而生殖細胞只有一套染色體,這一套染色體來自於具兩套染色體精原細胞或卵母細胞的減數分裂。減數分裂進行時,同大染色體(一對成對的染色體)可能會染色體互換,由此產生與父母方的都不完全一樣,子代不是完全繼承父方或母方的新染色體。
某些生物是多倍體,體細胞有三套甚至更多套染色體。
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
巴爾氏體
巴爾氏體(英語:Barr body,也譯作巴氏小體或巴爾小體),得名自其發現者穆雷·巴爾,是具有兩個以上X染色體(或Z染色體)的細胞中,為了避免該染色體上基因的過度表現,而將其中一條X染色體或Z染色體去活化而成的緊密結構。X染色體去活化機制由「Xist基因」控制,該基因可使X染色體受到較高度的DNA甲基化與較低度的組蛋白乙醯基化(histone acetylation)從而形成更緊密結構使去活化,成為一種異染色質,即巴爾氏體。
巴爾氏體上除了偽體染色體區(pseudoautosomal region)的基因仍可表現外,其餘片段的基因都受到抑制,這種現象稱為基因沉默(gene silencing)。巴爾氏體產生的目的和避免雌性的X染色體(或雄性的Z染色體)劑量過多有關,造成雌性身體由關閉不同X染色體的兩群不同的細胞組成,稱為嵌合體(mosaic),可以產生兩種不同的表現型,這也是花貓有三種毛色的原因。
染色體數目的變異
正常的情況下,一個生物體內,含有一定數量的染色體(見上表),而且是成對出現(2n)。而多倍體生物的細胞內具有超過兩套以上的染色體。三倍體的生成,可能是在形成配子的減數分裂的過程中,染色體發生了無分離(nondisjunction)現象而出現了2n的配子,故受精後產生三倍體的子代。四倍體的形成,可能是在2n的合子再行有絲分裂時,複製完成的染色體發生了無分離,導致產生含有四套染色體的子代。多倍體的果實通常都較巨大。
参考文献
- Armstrong SJ, Jones GH. . J. Exp. Bot. January 2003, 54 (380): 1–10. PMID 12456750. doi:10.1093/jxb/54.380.1.
- Gill BS, Kimber G. . Proc. Natl. Acad. Sci. U.S.A. April 1974, 71 (4): 1247–9. PMC 388202
 . PMID 4133848. doi:10.1073/pnas.71.4.1247.
. PMID 4133848. doi:10.1073/pnas.71.4.1247. - Kato A, Lamb JC, Birchler JA. . Proc. Natl. Acad. Sci. U.S.A. September 2004, 101 (37): 13554–9. PMC 518793
 . PMID 15342909. doi:10.1073/pnas.0403659101.
. PMID 15342909. doi:10.1073/pnas.0403659101. - Dubcovsky J, Luo MC, Zhong GY; et al. . Genetics. 1996, 143 (2): 983–99. PMC 1207354
 . PMID 8725244.
. PMID 8725244. - Ellison, W. (PDF). Genetica. 1935, 17 (1): 1–26 [2008-05-11]. doi:10.1007/BF01984179.
- Kenton A, Parokonny AS, Gleba YY, Bennett MD. . Mol. Gen. Genet. August 1993, 240 (2): 159–69. PMID 8355650. doi:10.1007/BF00277053.
- Leitch IJ, Soltis DE, Soltis PS, Bennett MD. . Ann. Bot. 2005, 95 (1): 207–17 [2009-07-11]. PMID 15596468. doi:10.1093/aob/mci014. (原始内容存档于2010-02-03).
- Umeko Semba, Yasuko Umeda, Yoko Shibuya, Hiroaki Okabe, Sumio Tanase and Tetsuro Yamamoto. . International Immunopharmacology. 2004, 4 (10-11): 1391–1400 [2009-07-11]. doi:10.1016/j.intimp.2004.06.003. (原始内容存档于2008-03-08).
- Vitturi R, Libertini A, Sineo L; et al. . Micron. 2005, 36 (4): 351–7. PMID 15857774. doi:10.1016/j.micron.2004.12.010.
- Vitturi R, Colomba MS, Pirrone AM, Mandrioli M. . J. Hered. 2002, 93 (4): 279–82 [2009-07-11]. PMID 12407215. doi:10.1093/jhered/93.4.279. (原始内容存档于2009-02-07).
- Nie W, Wang J, O'Brien PC; et al. . Chromosome Res. 2002, 10 (3): 209–22. PMID 12067210. doi:10.1023/A:1015292005631.
- De Grouchy J. . Genetica. 1987, 73 (1-2): 37–52. PMID 3333352.
- Houck ML, Kumamoto AT, Gallagher DS, Benirschke K. . Cytogenet. Cell Genet. 2001, 93 (3-4): 249–52. PMID 11528120. doi:10.1159/000056992.
- Wayne RK, Ostrander EA. . Bioessays. 1999, 21 (3): 247–57. PMID 10333734. doi:10.1002/(SICI)1521-1878(199903)21:3 (不活跃 2009-03-11).
- Burt DW. . Cytogenet. Genome Res. 2002, 96 (1-4): 97–112. PMID 12438785. doi:10.1159/000063018.
- Ciudad J, Cid E, Velasco A, Lara JM, Aijón J, Orfao A. . Cytometry. 2002, 48 (1): 20–5. PMID 12116377. doi:10.1002/cyto.10100.
- Yasukochi Y, Ashakumary LA, Baba K, Yoshido A, Sahara K. . Genetics. 2006, 173 (3): 1319–28. PMID 16547103. doi:10.1534/genetics.106.055541.
- Smith J, Burt DW. . Anim. Genet. 1998, 29 (4): 290–4. PMID 9745667. doi:10.1046/j.1365-2052.1998.00334.x.
參見
- 遺傳刪除
- 染色體遺傳演算法
- 遗传算法
- 染色體雙中節