馬來酸
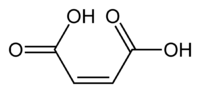
馬來酸(),,化學式為 HO2CCHCHCO2H,是一種二羧酸,即一個含有兩個羧酸官能基的有機化合物。馬來酸和反丁烯二酸(延胡索酸)互為順反異構物。馬來酸常用來製備反丁烯二酸,馬來酸的酸酐為顺丁烯二酸酐,和其酸酐比較起來,馬來酸的應用範圍較少。
| 马来酸 Maleic acid | |
|---|---|
 | |
 | |
 | |
 | |
| IUPAC名 Maleic acid (Z)-Butenedioic acid | |
| 别名 | (Z)-butenedioic acid, cis-butenedioic acid, malenic acid, maleinic acid, toxilic acid |
| 识别 | |
| CAS号 | 110-16-7 |
| ChemSpider | 392248 |
| SMILES |
|
| InChI |
|
| InChIKey | VZCYOOQTPOCHFL-UPHRSURJBG |
| EINECS | 203-742-5 |
| ChEBI | 18300 |
| RTECS | OM9625000 |
| KEGG | C01384 |
| 性质 | |
| 化学式 | C4H4O4 |
| 摩尔质量 | 116.07 g·mol−1 |
| 外观 | 白色固体 |
| 密度 | 1.59 g/cm³ [1],固体 |
| 熔点 | 135 °C(408 K)(分解[2]) |
| 沸点 | 202 °C (在1大氣壓下) |
| 溶解性(水) | 788 g/L[2] |
| pKa | pka1 = 1.9 pka2 = 6.07 [3] |
| 危险性 | |
欧盟危险性符号 有害 Xn 有害 Xn | |
| 警示术语 | R:R22 R36/37/38 |
| 安全术语 | S:S2 S26 S28 S37 |
| MSDS | MSDS from J. T. Baker |
| NFPA 704 |
 0
3
0
|
| 闪点 | 182.981°C |
| 相关物质 | |
| 相关羧酸 | 反丁烯二酸 琥珀酸 巴豆酸 |
| 相关化学品 | 马来酸酐 马来酰亚胺 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
馬來酸和其酸酐都不是核准的食品添加物,但美國及歐盟有限度的允許使用顺丁烯二酸酐在和食品直接或間接接觸的包材中,美國也允許將馬來酸用為化妝品中的酸鹼調和劑[4]。
名称
马来酸是对maleic的音译,得名自该化合物最早是由苹果酸(malic acid,羟基丁二酸)蒸馏而得。
物理特性
馬來酸相對反丁烯二酸來說比較沒那麼穩定。 順丁烯二酸為22.7 kJ·mol−1,反丁烯二酸則是 -1355 kJ/mole.[5] 順丁烯二酸在水中的溶解度比反丁烯二酸更好,順丁烯二酸的熔點(135℃)也比反丁烯二酸(287℃)低得多。分子內氫鍵可以解釋這兩種屬性的差異[6]。
化学性质
因为马来酸属于羧酸,故而水溶解度较高(25℃时为78g/100mL)。其几何异构体为反丁烯二酸,它们是世界上最早被发现的一对几何异构体。
加热至135℃时分解,可得到环状的马来酸酐,这是因为马来酸有两个接近的羧基。
而與马来酸不同,延胡索酸因为其两个羟基并不接近,所以不能环化。
製備方法
工業上生產順丁烯二酸的方法是透過水解順丁烯二酸酐,而後者可透過在五氧化二釩催化下,於450~500℃用空氣把苯或丁烷氧化[7]。
反丁烯二酸異構物
順丁烯二酸的主要工業用途使其轉化為反丁烯二酸,這種異構化轉換藉由各種試劑的催化,如無機酸和硫脲。其次,在水中的溶解度大使得反丁烯二酸純化輕鬆。
馬來酸和反丁烯二酸無法自發地互相轉換,是因為碳碳雙鍵部分;然而,順式異構體是利用少量溴的存在下通過光解轉換成反式異構體。 [8] 溴自由基的光轉換,溴烷烴自由基攻擊烯烴溴元素,形成的溴自由基再與反丁烯二酸結合。 另一種方法(用於實驗課堂)順丁烯二酸於12M鹽酸溶液中通過加熱可使中央C-C鍵形成更穩定,不易溶於反丁烯二酸。
順丁烯二酸鹽
順丁烯二酸離子是經由順丁二酸離子化形成,在生物化學中的順丁烯二酸離子作為轉氨酶反應的抑製劑,也被稱為順丁烯二酸酯、順丁烯二酸,例如順丁烯二酸二甲酯。
物質毒性
順丁烯二酸可能抑制代謝中某些酵素,例如胺基酸代謝之轉胺酶,而胺基酸代謝主要在肝臟與腎臟,因此長期攝入順丁烯二酸可能造成肝腎損害;此外,粒線體之檸檬酸循環中,某些酵素亦可能受到於順丁烯二酸影響,動物實驗中,會導致狗的腎小管損傷,產生不可逆的傷害。動物試驗中,傷害程度與劑量、攝入時間成正比。對人體是否會造成傷害,因缺少人體試驗,目前不清楚,但動物實驗中證實,順丁烯二酸極可能對人體細胞具有毒性。[9][10]。
參看
- 2013年台灣毒澱粉事件
參考資料
- Budavari, Susan (编), 12th, Merck, 1996, ISBN 0911910123
- Record in the GESTIS Substance Database from the IFA
- CRC Handbook of Chemistry and Physics, 73rd ed.; CRC Press: Boca Raton, FL., 1993
- 呂廷璋. . 台灣大學食品與生物分子研究中心. 2013-05-20 [2013-05-27]. (原始内容存档于2013-09-04). (页面存档备份,存于)
- Maleic Anhydride, Maleic Acid, and Fumaric Acid (页面存档备份,存于), Huntsman Petrochemical Corporation
- M. N. G James, G. J. B Williams. . Acta Crystallographica. 1974,. B30 (5) (5): 1249–1275. doi:10.1107/S0567740874004626.
- Kurt Lohbeck, Herbert Haferkorn, Werner Fuhrmann and Norbert Fedtke "Maleic and Fumaric Acids" in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2000. doi:10.1002/14356007.a16_053
- Light isomerization experiment 的存檔,存档日期2005-11-27. (from the University of Regensburg, with video)
- 林思宇 . . 聯合報. 2013年5月27日 [2013年5月27日]. (原始内容存档于2013年6月7日) (中文(臺灣)). (页面存档备份,存于)
- 施靜茹. . 聯合報. 2013年5月28日 [2013年5月28日]. (原始内容存档于2015年5月12日) (中文(臺灣)). (页面存档备份,存于)
外部連結
- International Chemical Safety Card 1186
- Titration of Fumaric and Maleic Acid (页面存档备份,存于) (from the University of Regensburg, about pH, solubility and melting point)
- Calculator: Water and solute activities in aqueous maleic acid (页面存档备份,存于)