谷胱甘肽
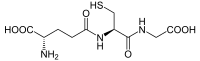
穀胱甘肽(英語:,簡稱:GSH),又称或麩氨基硫,[1]屬於三肽,由穀氨酸、半胱氨酸及甘氨酸所構成,其中第一个肽键与普通的肽键不同,是由穀氨酸的γ-羧基与半胱氨酸的氨基组成的,在分子中半胱氨酸巯基是该化合物的主要功能基团。谷胱甘肽是植物、动物、真菌和一些细菌和古菌中的一种抗氧化剂。谷胱甘肽能够防止活性氧、自由基、过氧化物、脂质过氧化物和重金属等来源对重要细胞成分造成的损害。[2] 作为動物細胞中的抗氧化剂,存在於充滿水的細胞內部,可以保護DNA免於氧化。穀胱甘肽以兩種型態存在於人體,一是还原型態、另一是氧化型態。菠菜含有穀胱甘肽。
| 谷胱甘肽 | |
|---|---|
 | |
 | |
 | |
| IUPAC名 γ-Glutamylcysteinylglycine | |
| 别名 | γ-L-Glutamyl-L-cysteinylglycine (2S)-2-Amino-4-({(1R)-1-[(carboxymethyl)carbamoyl]-2-sulfanylethyl}carbamoyl)butanoic acid |
| 缩写 | |
| 识别 | |
| CAS号 | 70-18-8 |
| PubChem | 124886 |
| ChemSpider | 111188 |
| SMILES |
|
| ChEBI | 16856 |
| DrugBank | DB00143 |
| KEGG | C00051 |
| MeSH | Glutathione |
| 性质 | |
| 化学式 | C10H17N3O6S |
| 307.325 g·mol⁻¹ | |
| 熔点 | 195[1] |
| 溶解性(水) | 易溶[1] |
| 溶解性(甲醇, 乙醚) | 不溶[1] |
| 药理学 | |
| ATC代码 | V03AB32(V03) |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
生物合成和储存
谷胱甘肽生物合成涉及两个三磷酸腺苷依赖的步骤:
- 首先,γ-谷氨酰半胱氨酸由 L-谷氨酸和 L-半胱氨酸合成。此转化需要酶谷氨酸-半胱氨酸连接酶 (GCL,谷氨酸半胱氨酸合酶)。此反应是谷胱甘肽合成中的限速步骤。[3]
- 其次,将甘氨酸添加到γ-谷氨酰半胱氨酸的C末端。该缩合反应由谷胱甘肽合成酶催化。
虽然所有动物细胞都能够合成谷胱甘肽,但已证明肝脏中的谷胱甘肽合成至关重要。GCLC基因敲除小鼠由于缺乏肝脏GSH合成而在出生后一个月内死亡。[4][5] 谷胱甘肽中不寻常的γ酰胺键保护它免受肽酶的水解。[6]
储存
谷胱甘肽是动物细胞中最丰富的非蛋白硫醇(含 R-SH 的化合物),含量范围为 0.5 至 10 mmol/L。它存在于细胞质和细胞器中。在健康细胞和组织中,[6]总谷胱甘肽池的 90% 以上为还原形式(GSH),其余为二硫化物氧化形式(GSSG)。[7]80-85% 的细胞GSH存在于细胞质中,10-15% 存在于线粒体中。[8]
人体能够合成谷胱甘肽,但少数真核生物不会合成谷胱甘肽,包括豆科植物、内阿米巴属和贾第鞭毛虫属的部分成员。已知唯一能合成谷胱甘肽的古细菌是盐杆菌纲。某些细菌,如“蓝藻”和假单胞菌,可以生物合成谷胱甘肽。[9][10]
口服谷胱甘肽的全身利用度生物利用度较差,因为三肽是消化道蛋白酶(肽酶)的底物,并且由于细胞膜水平上缺乏谷胱甘肽的特定载体。[11][12]服用半胱氨酸前体药物 N-乙酰半胱氨酸 (NAC) 有助于补充细胞内 GSH 水平。[13]专利化合物 RiboCeine 已被研究作为一种补充剂,可增强谷胱甘肽的产生,从而有助于缓解高血糖。[14][15]
生物学功能
谷胱甘肽以还原(GSH)和氧化(GSSG)状态存在。[16]细胞内还原谷胱甘肽与氧化谷胱甘肽的比率是细胞氧化应激的量度,[17][8]其中 GSSG 与 GSH 比率增加表明氧化应激更大。

在还原状态下,半胱氨酰残基的硫醇基团是一个还原当量的来源。由此生成谷胱甘肽二硫化物 (GSSG)的氧化状态通过NADPH[18]转化为还原状态(GSH)。该转化由谷胱甘肽还原酶催化
- NADPH + GSSG + H2O → 2 GSH + NADP+ + OH−
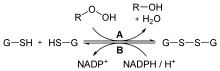 GSH和GSSG的转化过程
GSH和GSSG的转化过程
作用
抗氧化剂
GSH通过中和(减少)活性氧来保护细胞。[19][6]这种转化可以通过过氧化物的还原来说明:
- 2 GSH + R2O2 → GSSG + 2 ROH (R = 氢,烷基 )
以及自由基:
- GSH + R• → 1/2 GSSG + RH
调节
除了使自由基和活性氧化剂失活外,谷胱甘肽还参与硫醇保护和氧化应激下细胞硫醇蛋白的氧化还原调节,通过蛋白质“S”-谷胱甘肽化,一种氧化还原调节的翻译后硫醇修饰。一般反应涉及从可保护蛋白质 (RSH) 和 GSH 形成不对称二硫化物:[20]
- RSH + GSH + [O] → GSSR + H2O
谷胱甘肽还用于解毒氧化应激产生的有毒代谢物甲基乙二醛和甲醛。该解毒反应由乙二醛酶系统进行。乙二醛酶I (EC 4.4.1.5) 催化甲基乙二醛和还原谷胱甘肽转化为 S-D-乳酰谷胱甘肽。乙二醛酶II (EC 3.1.2.6) 催化 S-D-乳酰谷胱甘肽水解为谷胱甘肽和D-乳酸。
新陈代谢
在其参与的众多代谢过程中,谷胱甘肽是白三烯和前列腺素生物合成所必需的。它在半胱氨酸的储存中发挥作用。谷胱甘肽增强了瓜氨酸作为一氧化氮循环一部分的功能。[24]它是一种辅因子并作用于谷胱甘肽过氧化物酶。[25] 谷胱甘肽用于生成 S-硫烷基谷胱甘肽,它是硫化氢代谢的一部分。[26]
用途
参考文献
- Haynes, William M. (编). 97th. CRC Press. 2016: 3.284. ISBN 9781498754293.
- Pompella A, Visvikis A, Paolicchi A, De Tata V, Casini AF. . Biochemical Pharmacology. October 2003, 66 (8): 1499–1503. PMID 14555227. doi:10.1016/S0006-2952(03)00504-5.
- White CC, Viernes H, Krejsa CM, Botta D, Kavanagh TJ. . Analytical Biochemistry. July 2003, 318 (2): 175–180 [2024-03-22]. PMID 12814619. doi:10.1016/S0003-2697(03)00143-X. (原始内容存档于2020-09-27).
- Chen Y, Yang Y, Miller ML, Shen D, Shertzer HG, Stringer KF, Wang B, Schneider SN, Nebert DW, Dalton TP. . Hepatology. May 2007, 45 (5): 1118–1128. PMID 17464988. S2CID 25000753. doi:10.1002/hep.21635
 .
. - Sies H. . Free Radical Biology & Medicine. 1999, 27 (9–10): 916–921. PMID 10569624. doi:10.1016/S0891-5849(99)00177-X.
- Guoyao Wu; Yun-Zhong Fang; Sheng Yang; Joanne R. Lupton; Nancy D. Turner. . Journal of Nutrition. 2004, 134 (3): 489–492. PMID 14988435. doi:10.1093/jn/134.3.489
 .
. - Halprin KM, Ohkawara A. . The Journal of Investigative Dermatology. 1967, 48 (2): 149–152. PMID 6020678. doi:10.1038/jid.1967.24
 .
. - Lu SC. . Biochimica et Biophysica Acta. May 2013, 1830 (5): 3143–3153. PMC 3549305
 . PMID 22995213. doi:10.1016/j.bbagen.2012.09.008.
. PMID 22995213. doi:10.1016/j.bbagen.2012.09.008. - Copley SD, Dhillon JK. . Genome Biology. 29 April 2002, 3 (5): research0025. PMC 115227
 . PMID 12049666. doi:10.1186/gb-2002-3-5-research0025
. PMID 12049666. doi:10.1186/gb-2002-3-5-research0025  .
. - Wonisch W, Schaur RJ. . Grill D, Tausz T, De Kok LJ (编). . Springer. 2001. ISBN 978-1-4020-0178-9 –Google Books.
- Witschi A, Reddy S, Stofer B, Lauterburg BH. . European Journal of Clinical Pharmacology. 1992, 43 (6): 667–669. PMID 1362956. S2CID 27606314. doi:10.1007/bf02284971.
- . Drugs.com. [2024-03-23]. (原始内容存档于2015-09-23).
- Atkuri, K. R.; Mantovani, J. J.; Herzenberg, L. A.; Herzenberg, L. A. . Current Opinion in Pharmacology. 2007, 7 (4): 355–359. PMC 4540061
 . PMID 17602868. doi:10.1016/j.coph.2007.04.005.
. PMID 17602868. doi:10.1016/j.coph.2007.04.005. - Nagasawa, Herbert T. . ppubs.uspto.gov. United States Patent Office: 16. November 27, 2014 [October 31, 2023]. (原始内容存档于2023-10-31).
30. A method of increasing ATP and/or glutathione...
- Ukwenya VO, Alese MO, Ogunlade B, Folorunso IM, Omotuyi OI. . J Diabetes Metab Disord. 2022, 22 (1): 455–468. PMC 10225389
 . PMID 37255827. doi:10.1007/s40200-022-01165-2.
. PMID 37255827. doi:10.1007/s40200-022-01165-2. - Iskusnykh IY, Zakharova AA, Pathak D. . Molecules. January 2022, 27 (1): 324. PMC 8746815
 . PMID 35011559. doi:10.3390/molecules27010324
. PMID 35011559. doi:10.3390/molecules27010324  .
. - Pastore A, Piemonte F, Locatelli M, Lo Russo A, Gaeta LM, Tozzi G, Federici G. . Clinical Chemistry. August 2001, 47 (8): 1467–1469 [2024-03-21]. PMID 11468240. doi:10.1093/clinchem/47.8.1467
 . (原始内容存档于2016-03-03).
. (原始内容存档于2016-03-03). - Couto N, Malys N, Gaskell SJ, Barber J. (PDF). Journal of Proteome Research. June 2013, 12 (6): 2885–2894 [2024-03-21]. PMID 23631642. doi:10.1021/pr4001948. (原始内容存档 (PDF)于2024-03-19).
- Michael Brownlee. . Diabetes. 2005, 54 (6): 1615–1625. PMID 15919781. doi:10.2337/diabetes.54.6.1615
 .
. - Dalle-Donne, Isabella; Rossi, Ranieri; Colombo, Graziano; Giustarini, Daniela; Milzani, Aldo. . Trends in Biochemical Sciences. 2009, 34 (2): 85–96. PMID 19135374. doi:10.1016/j.tibs.2008.11.002.
- Dringen R. . Progress in Neurobiology. December 2000, 62 (6): 649–671. PMID 10880854. S2CID 452394. doi:10.1016/s0301-0082(99)00060-x.
- Scholz RW, Graham KS, Gumpricht E, Reddy CC. . Annals of the New York Academy of Sciences. 1989, 570 (1): 514–517. Bibcode:1989NYASA.570..514S. S2CID 85414084. doi:10.1111/j.1749-6632.1989.tb14973.x.
- Hughes RE. . Nature. 1964, 203 (4949): 1068–1069. Bibcode:1964Natur.203.1068H. PMID 14223080. S2CID 4273230. doi:10.1038/2031068a0.
- Ha SB, Smith AP, Howden R, Dietrich WM, Bugg S, O'Connell MJ, Goldsbrough PB, Cobbett CS. . The Plant Cell. June 1999, 11 (6): 1153–1164. JSTOR 3870806. PMC 144235
 . PMID 10368185. doi:10.1105/tpc.11.6.1153.
. PMID 10368185. doi:10.1105/tpc.11.6.1153. - Grant CM. . Molecular Microbiology. 2001, 39 (3): 533–541. PMID 11169096. S2CID 6467802. doi:10.1046/j.1365-2958.2001.02283.x
 .
. - Melideo, SL; Jackson, MR; Jorns, MS. . Biochemistry. 22 July 2014, 53 (28): 4739–53. PMC 4108183
 . PMID 24981631. doi:10.1021/bi500650h.
. PMID 24981631. doi:10.1021/bi500650h. - Hayes, John D.; Flanagan, Jack U.; Jowsey, Ian R. . Annual Review of Pharmacology and Toxicology. 2005, 45: 51–88. PMID 15822171. doi:10.1146/annurev.pharmtox.45.120403.095857.
- Noctor G, Foyer CH. . Annual Review of Plant Physiology and Plant Molecular Biology. June 1998, 49 (1): 249–279. PMID 15012235. doi:10.1146/annurev.arplant.49.1.249.
- Ha SB, Smith AP, Howden R, Dietrich WM, Bugg S, O'Connell MJ, Goldsbrough PB, Cobbett CS. . The Plant Cell. June 1999, 11 (6): 1153–1164. PMC 144235
 . PMID 10368185. doi:10.1105/tpc.11.6.1153.
. PMID 10368185. doi:10.1105/tpc.11.6.1153. - Parisy V, Poinssot B, Owsianowski L, Buchala A, Glazebrook J, Mauch F. (PDF). The Plant Journal. January 2007, 49 (1): 159–172 [2024-04-04]. PMID 17144898. doi:10.1111/j.1365-313X.2006.02938.x
 . (原始内容存档 (PDF)于2022-04-03).
. (原始内容存档 (PDF)于2022-04-03). - Rouhier N, Lemaire SD, Jacquot JP. (PDF). Annual Review of Plant Biology. 2008, 59 (1): 143–166 [2024-04-04]. PMID 18444899. doi:10.1146/annurev.arplant.59.032607.092811. (原始内容存档 (PDF)于2024-01-07).
- Rigaud J, Cheynier V, Souquet JM, Moutounet M. . Journal of the Science of Food and Agriculture. 1991, 57 (1): 55–63. Bibcode:1991JSFA...57...55R. doi:10.1002/jsfa.2740570107.
- Vallverdú-Queralt A, Verbaere A, Meudec E, Cheynier V, Sommerer N. . Journal of Agricultural and Food Chemistry. January 2015, 63 (1): 142–149. PMID 25457918. doi:10.1021/jf504383g.
参见
- 活性多肽
- 谷氧还蛋白