亚胺
亚胺(英語:imine)是一种含碳-氮双键的官能团或有机化合物,通式为:R1R2C=NR3,其中氮原子连接一个氢原子(H)或一个有机基团(R3),碳原子则与另两个基团以单键连接。[1][2][3]
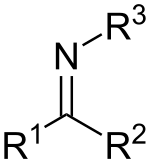
亚胺的通式
命名与分类
亚胺可视为醛或酮中氧原子被NR基团(R可以是氢或有机基团)所取代得到的产物。若NR3中的R3=H,化合物为一级亚胺;若R3=烃基,则化合物为二级亚胺。亚胺是一种可参与多种反应的化合物,其应用在有机化学中随处可见。[3] 若R3=OH,则称为:肟;若R3=NH2,则称为:腙。
亚胺的合成
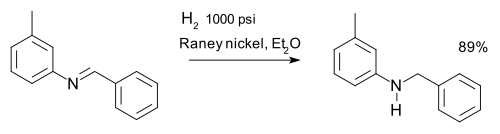
制备亚胺的典型方法是通过伯胺和醛发生缩合反应(与酮缩合相比较少见)。该反应机理是胺的孤对电子先进攻羰基发生亲核加成,得到半缩醛胺(-C(OH)(NHR)-)中间体,而后继续消除一分子水得到亚胺(更详细的机理参见烷基亚胺去氧双取代反应)。由于反应平衡更倾向于羰基化合物与胺一侧,因此反应过程需要共沸蒸馏、回流分水或使用脱水试剂如:分子筛,以使平衡向形成亚胺化合物的方向移动。
下列为合成亚胺的一些方法:
亚胺的反应
亚胺参与的最重要的反应为水解反应,即合成相应的胺与羰基化合物的反应,其他亚胺参与的反应大多类似于醛与酮类化合物的反应。
- 亚胺与另一分子胺反应得到缩醛胺,例如合成:瓜环。
- 在氮杂双烯狄尔斯–阿尔德反应中,亚胺与二烯烃反应得到四氢吡啶。
- 亚胺可与间氯过氧苯甲酸(mCPBA)发生氧化反应得到氧杂氮杂环丙烷。
- 在Povarov反应中,芳香亚胺与烯醇醚反应得到喹啉。
- 氮杂-贝里斯-希尔曼反应中,对甲苯磺酰亚胺与α,β-不饱和羰基化合物反应得到烯丙基胺。
- Eschweiler-Clarke反应中,胺与甲酸进行烷基化反应过程中,亚胺作为中间体存在。
- 亚胺可作为中间体参与糖化学中的重排反应,如:Amadori重排反应。
- 亚胺可通过不稳定的锍叶立德,发生亚甲基转移反应从而制备氮丙啶衍生物。
- 还原胺化反应中,亚胺是重要的中间体。
生物作用
亚胺在自然中很常见,如: 维生素B6可促进氨基酸通过亚胺化合物来进行脱氨。
参考文献
- 國際純化學和應用化學聯合會,化學術語概略,第二版。(金皮書)(1997)。在線校正版: (2006–) "imines"。doi:10.1351/goldbook.I02957.html
- March Jerry; (1985). Advanced Organic Chemistry reactions, mechanisms and structure (3rd ed.). New York: John Wiley & Sons, inc. ISBN 0-471-85472-7
- Fletcher, Dermer, Fox, Nomenclature of Organic Compounds (1974) doi:10.1021/ba-1974-0126.ch023
- 國際純化學和應用化學聯合會,化學術語概略,第二版。(金皮書)(1997)。在線校正版: (2006–) "aldimines"。doi:10.1351/goldbook.A00209.html
- 國際純化學和應用化學聯合會,化學術語概略,第二版。(金皮書)(1997)。在線校正版: (2006–) "ketimines"。doi:10.1351/goldbook.K03381.html
- W. J. Middleton and H. D. Carlson (1988). "Hexafluoroacetone imine". Org. Synth.; Coll. Vol. 6: 664..
- C. F. H. Allen and James VanAllan (1955). "m-Tolylbenzylamine". Org. Synth.: 827; Coll. Vol. 3.
- 例如:Ieva R. Politzer and A. I. Meyers (1988). "Aldehydes from 2-Benzyl-4,4,6-trimethyl-5,6-dihydro-1,3(4H)-oxazine: 1-Phenylcyclopentanecarboxaldehyde". Org. Synth.; Coll. Vol. 6: 905.
- Langlois, N. . Tet. Lett. 1973, 14: 4865. doi:10.1016/S0040-4039(01)87358-5.
- Kobayashi, Shū; Ishitani, Haruro. . Chem. Rev. 1999, 99: 1069. doi:10.1021/cr980414z.
- J. Martens: Reduction of Imino Groups (C=N) in (G. Helmchen, R. W. Hoffmann, J. Mulzer, E. Schaumann) Houben-Weyl Stereoselective Synthesis, Workbench Edition E21 Volume 7, S. 4199-4238, Thieme Verlag Stuttgart, 1996, ISBN 3-13-106124-3.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.
-skeletal.svg.png.webp)
-skeletal.svg.png.webp)
-skeletal.svg.png.webp)
-skeletal.svg.png.webp)