受体 (生物化学)
受體(receptors),又称受器、接收器,是一個生物化學上的概念,指一類能傳導細胞外信號,並在細胞內產生特定效應的分子。產生的效應可能僅在短時間內持續,比如改變細胞的代謝或者細胞的運動。也可能是長效的效應,比如上調或下調某個或某些基因的表達[1][2][3]。
受體通過與特定的配體結合而感知到細胞外的信號。隨後,受體的結構發生變化,並誘導細胞內產生相應的效應。受體通過信号级联效應,逐步以指數級擴大細胞內產生的效應的強度。信號級聯的第一步可能是產生cAMP等第二信使分子,誘導下一級反應[3]。根據受體所在的位置,可以分爲細胞表面受體和細胞內受體兩類。其中細胞表面受體位於細胞表面,處於內環境中的配體可以直接與之結合。大部分的細胞內受體都屬於核受體。在未與配體結合時,這些受體位於細胞質中,配體需要穿過細胞膜進入細胞內,才能與該受體結合。在與配體結合後,核受體會轉入細胞核中發揮效應。另一類細胞內受體是細胞內的酶、RNA、核糖體等,配體通過與這些受體結合發揮效應[4][5]。
細胞表面受體
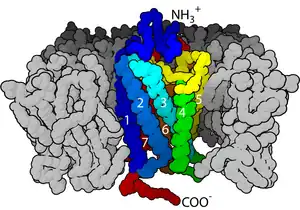
細胞表面受體是一類位於細胞表面的受體,可與細胞外的配體結合結合,並引發細胞內的反應。目前已發現的細胞表面受體中,較經典的有5類:G蛋白偶聯受體(G protein-coupled receptor)、受體酪氨酸激酶(Receptor tyrosine kinases)、鳥苷酸環化酶偶聯受體(Guanylate cyclase-coupled receptor)、離子通道(ion channel),以及黏附受體(adhesion receptor),其中以G蛋白偶連受體的數量最多,相關的研究也是最深入的,諾貝爾化學獎以及諾貝爾生理醫學獎都有授予給G蛋白偶聯受體的研究者的紀錄[6][7][3][8]。
G蛋白偶聯受體
G蛋白偶聯受體是目前發現最主要的一種細胞表面受體,對它的研究也是最透徹的。G蛋白偶聯受體可分爲A-F六類,不同分類之間並沒有顯著的同源關係[9][10][11][12]。G蛋白偶聯受體的一個特徵是,它有一個穿膜7次結構域的受體,肽鏈的N端位於細胞外側,C端則位於細胞內。另一個特徵則是該受體與G蛋白偶聯。G蛋白通常含有三個亞基α、β、γ,其中α亞基靜息狀態下與GDP結合。當受體被配體激活後,受體會使與G蛋白結合的GDP轉化爲GTP,從而使G蛋白活化,α亞基分離,引起下一步反應,通過肌醇三磷酸(IP3)、cAMP等第二信使引發下一級反應[3][8]。
受體酪氨酸激酶
受體酪氨酸激酶是一類有著單次穿膜結構域的受體,在細胞內側偶聯着酪氨酸激酶。當該類受體激活後,內側的酪氨酸激酶會發生活化,對蛋白肽鏈上的酪氨酸(Tyr)進行磷酸化,進而產生下一步效應。胰島素受體、IGF1R,以及IGF2R都屬於受體酪氨酸激酶[13][14][8]。
鳥苷酸環化酶偶聯受體
鳥苷酸環化酶偶聯受體(Guanylate cyclase-coupled receptor),亦稱爲受體鳥苷酸環化酶(Receptor guanylate cyclase),是一種單次穿膜的細胞表面受體,該受體因爲可在激活後將鳥苷酸環化爲cGMP,以cGMP分子作爲第二信使而得名。在人體內,因爲不同組織中鳥苷酸環化酶偶聯受體的類型不同,這類受體的具體功能也不同。腎臟中的心房利鈉肽(ANF)受體NRP1、NRP2、NRP3就屬於鳥苷酸環化酶偶聯受體。另外,亦存在位於細胞內的鳥苷酸環化酶偶聯受體,比如可溶性一氧化氮激活鳥苷酸環化酶(soluble NO-activated guanylate cyclase)[8][15]。
細胞內受體
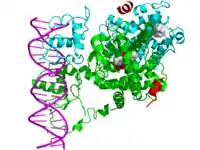
位於細胞內的受體稱爲細胞內受體。大部分的細胞內受體是核受體,在未激活時位於細胞質中。因爲配體需要穿過細胞膜,擴散入細胞質中後才可以與核受體結合,因而核受體的配體大部分是小分子脂類物質。核受體在與配體結合後,會進入細胞核內,對基因的表達進行調控,因而核受體可認爲是一類轉錄因子。因爲核受體的效應是改變基因表達,因而相比細胞表面受體,核受體產生效應所需時間相對較長,同時產生的效應相對也能持續較長時間[19][20][5]。
除核受體外,還有一類細胞內受體的化學本質是細胞內的酶、結構性蛋白、核糖體或RNA。比如藥物(配體)甲氧苄氨嘧啶可以作用於受體微管、紅黴素可以作用於細菌的50s核糖體亞基[5]。
信號級聯
受體在接受胞外信號後,會向細胞內傳遞信號。在這個過程中,信號通過不斷向下一級傳遞的方式逐漸增大,這個過程稱爲信號級聯。雖然受體最初只能產生小部分的效應分子,但每個效應分子又能激活幾個下一級的信號分子,這樣,一個受體的信號會以指數級的方式不斷擴大,最後在細胞內產生明顯的效應,比如使數個基因的表達發生變化。一些受體在激活後會產生一些效應分子,如cAMP等,並由這些分子開始信號級聯反應,這樣的分子稱爲第二信使[21][22][8]。
受體脫敏
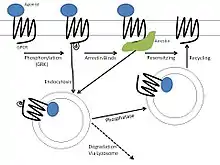
受體脫敏(desensitization)是指受體在反覆受到配體刺激活化後,對配體反應的敏感性的強度下降的現象。在藥理學中,快速抗藥即由受體脫敏造成。受體脫敏的一種機制是,受體通過內吞作用被運回細胞內部,使細胞表面的受體數量減少,能與內環境中配體結合的受體也就減少。此外,一部分受體,如一些離子通道,在激活後需要經過一定的靜息期方可再次被激活[5][8]。 细胞对外界信号作出适度的反应既涉及信号的有效刺激和启动,也依赖于信号的接触与细胞的反应终止。而解除与终止信号的重要方式,就是细胞使受体脱敏。这是一种负反馈调控机制。 概括起来,靶细胞对信号分子的脱敏机制有如下5种方式: (1)受体没收:细胞通过配体依赖性的受体介导的内吞作用减少细胞表面可利用受体的数目,以网格蛋白/AP包被膜泡的形式摄入细胞,内吞泡脱包被形成无包被的早期胞内体,受体被暂时扣留,受pH降低的影响(pH5.0)受体-配体复合物在晚期胞内体解离,扣留的受体可返回质膜再利用(如LDL受体),配体进入溶酶体被消化。这是细胞对多种肽类或其他激素受体发生脱敏反应的一种基本途径。有时即使缺乏配体结合的情况下,细胞通过批量膜流也会使细胞表面受体以相对较低的速率被内化,然后再循环利用,从而减少细胞表面可利用受体的数目。 (2)受体下调:通过受体介导的内吞作用,受体-配体复合物转移到胞内溶酶体消化降解而不能重新利用,因此细胞通过表面自由受体数目减少和配体的清除导致细胞对信号敏感性下调。 (3)受体失活:通过信号通路将受体进行一些修饰从而让其失活,这是一种快速的受体脱敏机制。以视杆细胞对周围光强度变化的适应为例,由光激活的视蛋白是视紫红质激酶的底物,活化的视蛋白其胞质面3个丝氨酸残基恰是视紫红质激酶的磷酸化位点。视蛋白的磷酸化一方面显著降低视蛋白分子激活G蛋白α亚基的能力,另一方面视蛋白胞质面磷酸-丝氨酸位点为胞质抑制蛋白β-arrestin的结合提供了锚定位点,β-arrestin的结合完全阻断G蛋白α亚基与磷酸化的视蛋白的相互作用,从而关闭所有视杆细胞的活性。这种引发靶细胞对信号刺激的脱敏机制也是其他G蛋白偶联受体在高配体水平条件下引发脱敏反应的普遍机制,导致受体磷酸化的激酶包括PKA、PKC和G蛋白偶联受体激酶(GRK)家族。GRK只结合已经被激活的受体,使其C端胞质域特定氨基酸残基磷酸化,从而结合β-arrestin,这是G蛋白偶联受体脱敏的重要方式之一。 (4)信号蛋白失活:受体本身不受影响,但级联反应中细胞内的信号蛋白受阻,不能诱导正常的细胞反应。 (5)抑制蛋白产生:受体被激活之后,在下游的反应中产生异质性的蛋白,形成负反馈环从而阻止之后的信号转导过程。 [23]
学说发展史
1878年,约翰·牛波特·朗勒提出了最早的受体假设,他用“受体物质”来解释阿托品和毛果芸香碱对猫唾液分泌的拮抗作用。1913年,保羅·埃爾利希根据实验结果提出了“锁和钥匙”的药物与受体的互补关系,但当时认为受体和配体都是静止不动的。1933年,阿爾弗雷德·約瑟夫·克拉克在研究药物对蛙心的量效关系中,定量的阐明了药物于受体的相互作用。这些说法为受体学说奠定了基础。[24]
20世纪50-60年代,阿里恩斯和斯蒂芬森(R P 'Steve' Stephenson)从实验发现药物产生最大效应不一定占领全部受体,由此提出的备用受体学说和速率学说,从动力学的角度解释了受体拮抗剂和激动剂的作用。[24]
20世纪70年代以后,随着蛋白质晶体学的发展,许多配体和受体的结构被人们所认识,从而阐明了受体亚型、离子通道等的分布和功能。变构学说彻底打破了蛋白质静止不动的认识,认为受体在有活性与无活性的构象状态间转化。1977年,格里夫斯(Greaves)提出的能动受体学说,把受体的微观变化同生理、生化或药理反应相联系,说明了受体在细胞膜内传递信息的作用机制。[24]
參考
- Hall, JE. . Philadelphia, PA: Elsevier Saunders. 2016: 930–937. ISBN 978-1-4557-7005-2.
- Alberts, Bruce; Bray, Dennis; Hopkin, Karen; Johnson, Alexander; Lewis, Julian; Raff, Martin; Roberts, Keith; Walter, Peter. Fourth. New York, NY, USA: Garland Science. 2014: 534. ISBN 978-0-8153-4454-4.
- Harvey Lodish; et al. . . Macmillan Higher Education. 2013: 674–683. ISBN 978-1-4641-0981-2.
- Rang HP, Dale MM, Ritter JM, Flower RJ, Henderson G. 7th. Elsevier Churchill Livingstone. 2012. ISBN 978-0-7020-3471-8.
- Michelle A. Clark; et al. 5th. 北京大學醫學出版社. 2013: 26–36. ISBN 978-7-5659-0620-6.
- . Nobel Foundation. [2007-07-28]. (原始内容存档于2007-07-18).
- Royal Swedish Academy of Sciences. . 2012-10-10 [2012-10-10]. (原始内容存档于2012-10-12).
- David L. Nelson; Michael M. Cox; et al. 6th. New York: W. H. Freeman and Company. 2013: 436-484. ISBN 978-1-4292-3414-6.
- Attwood TK, Findlay JB. . Protein Eng. 1994, 7 (2): 195–203 [2018-05-22]. PMID 8170923. doi:10.1093/protein/7.2.195. (原始内容存档于2007-10-12).
- Kolakowski LF Jr. . Receptors Channels. 1994, 2 (1): 1–7. PMID 8081729.
- Foord SM, Bonner TI, Neubig RR, Rosser EM, Pin JP, Davenport AP, Spedding M, Harmar AJ. . Pharmacol Rev. 2005, 57 (2): 279–88. PMID 15914470. doi:10.1124/pr.57.2.5.
- . [2018-05-22]. (原始内容存档于2008-02-21).
- Robinson DR, Wu YM, Lin SF. . Oncogene. November 2000, 19 (49): 5548–57. PMID 11114734. doi:10.1038/sj.onc.1203957.
- Ségaliny et al. (2015) "Receptor tyrosine kinases: Characterisation, mechanism of action and therapeutic interests for bone cancers". Bone Oncology 23;4 (1):1-12. (页面存档备份,存于) Retrieved on 2017-09-17
- George J. Siegel; R. Wayne Albers. . Academic Press. 2006: 368– [2010-12-16]. ISBN 978-0-12-088397-4.
- . HUGO Gene Nomenclature Committee. [2018-05-22]. (原始内容存档于2017-11-14).
- 道兰氏医学词典中的ligand-gated channel
- Purves, Dale, George J. Augustine, David Fitzpatrick, William C. Hall, Anthony-Samuel LaMantia, James O. McNamara, and Leonard E. White. . Sinauer Associates. 2008: 156–7. ISBN 978-0-87893-697-7.
- Evans RM. . Science. May 1988, 240 (4854): 889–95. PMID 3283939. doi:10.1126/science.3283939.
- Olefsky JM. . The Journal of Biological Chemistry. October 2001, 276 (40): 36863–4. PMID 11459855. doi:10.1074/jbc.R100047200.
- Lalli E, Sassone-Corsi P. . The Journal of Biological Chemistry. Jul 1994, 269 (26): 17359–62. PMID 8021233.
- Rosen OM. . Science. Sep 1987, 237 (4821): 1452–8. Bibcode:1987Sci...237.1452R. PMID 2442814. doi:10.1126/science.2442814.
- 定量细胞生物学(第4版),翟中和
- 李端 殷明. 药理学. 人民卫生出版社. 11-15. ISBN 978-7-117-08905-0
