奥希替尼
奥希替尼 (英語:,又名奥沙替尼)[2][3] 是一种用于治疗非小细胞肺癌的小分子靶向抗肿瘤药物,[4][5] 它由阿斯利康公司开发,为第三代表皮生长因子受体抑制剂。该药物于2017年被FDA和欧盟批准用于治疗非小细胞肺癌,2018年被CFDA批准用于治疗晚期或转移性非小细胞肺癌。
 | |
| 臨床資料 | |
|---|---|
| 商品名 | Tagrisso, Tagrix |
| 其他名稱 | AZD9291 |
| AHFS/Drugs.com | tagrisso |
| 核准狀況 | |
| 给药途径 | Oral 片剂 |
| ATC碼 | |
| 法律規範狀態 | |
| 法律規範 |
|
| 藥物動力學數據 | |
| 血漿蛋白結合率 | Probably high[1] |
| 药物代谢 | Oxidation (CYP3A) |
| 生物半衰期 | 48 hours |
| 排泄途徑 | Feces (68%), urine (14%) |
| 识别 | |
| |
| CAS号 | 1421373-65-0 |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| PDB配體ID | |
| 化学 | |
| 化学式 | C28H33N7O2 |
| 摩尔质量 | 499.62 g·mol−1 |
| 3D模型(JSmol) | |
| |
| |
临床用途
奥希替尼用于治疗EGFR T790M基因突变阳性且第一代和第二代表皮生长因子受体抑制剂治疗无效的晚期或转移性非小细胞肺癌。[6]该突变往往是由于癌细胞天然耐药性或第一代及第二代表皮生长因子受体抑制剂(如吉非替尼、阿法替尼等)治疗过程中产生耐药性所导致的。[7]
在美国,用奥希替尼来治疗T790M阳性非小细胞肺癌的患者在治疗之前必须接受由联邦政府批准的伴随诊断测试来测定患者T790M突变的情况,从而确定合理的治疗方案,FDA已批准FoundationOne伴随诊断用于该测试。[8] 在欧洲和其他国家,T790M突变的情况可以通过基因诊断技术来分析。[9]
接受奥希替尼治疗的患者通常在开始治疗后大约第10个月产生耐药性。[10] 大多数临床的耐药性病例主要是由外显子20C797S突变所引起的。[11]
用法用量
既往至少接受过一种治疗的成人慢性淋巴细胞白血病(CLL)/小淋巴细胞淋巴瘤(SLL)患者:推荐剂量为每次 150 mg,口服,每日一次, 直至疾病进展或出现不可耐受的毒性。[12]
药理学
奥希替尼能与T790M突变阳性的EGFR蛋白结合;[6] 它还能与L858R突变阳性的EGFR结合并能使EFGR上的19外显子失活。
奥希替尼在体内的吸收及代谢过程遵循线性药物动力学,其血药浓度达峰时间约为6小时,半衰期约为48小时,清除率为14.2L/h。原形药经肝脏代谢后68%通过粪便排泄,14%通过尿液排泄。
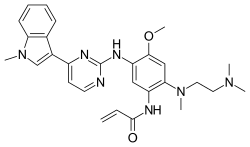
化学结构
临床上主要应用的为奥希替尼的甲磺酸盐(即甲磺酸奥希替尼),化学式为C28H33N7O2•CH4O3S,分子量为596g/mol,IUPAC名称为N-(2-2-二甲氨基乙基-甲基氨基-4-甲氧基-5-[4-(1-甲基吲哚-3-基)嘧啶-2-基]氨基苯基)丙-2-烯胺甲磺酸盐。
历史
奥希替尼的研发于2009年开始,并于2012年取得目标化合物。该项目通过针对靶点的药物结构设计方法,旨在找到能选择性针对T790M突变阳性非小细胞癌的第三代表皮生长因子受体抑制剂。[13]
奥希替尼在第一阶段研究结果发表后于2014年4月被FDA指定加入突破治疗法案计划,[13] 并于2015年11月得到了FDA加速批准程序与优先审查。[14]
2016年2月EMA临时批准奥希替尼进入加速审批程序,它也是该程序成立以来第一个接受此程序的药物。[13]
药品经济学
该药在美国上市初的价格为一个月疗程12,750美元。[15]:59
参考文献
- (PDF). FDA. November 2015 [2019-07-17]. (原始内容存档 (PDF)于2017-02-16). Index page for NDA 208065 (页面存档备份,存于)
- . AdisInsight. [2017-02-27]. (原始内容存档于2018-08-23) (英语).
- (PDF). International Nonproprietary Names for Pharmaceutical Substances (INN). 2015, 29 (2): 285 [2015-11-16]. (原始内容存档 (PDF)于2017-04-28).
- Ayeni D, Politi K, Goldberg SB. . Clin. Cancer Res. 2015, 21 (17): 3818–20. PMC 4720502
 . PMID 26169963. doi:10.1158/1078-0432.CCR-15-1211.
. PMID 26169963. doi:10.1158/1078-0432.CCR-15-1211. - Tan CS, Gilligan D, Pacey S. . Lancet Oncol. 2015, 16 (9): e447–59. PMID 26370354. doi:10.1016/S1470-2045(15)00246-6.
- . UK Electronic Medicines Compendium. 2017-01-26 [2017-02-27]. (原始内容存档于2017-02-27) (英语).
- Xu M, Xie Y, Ni S, Liu H. . Ann Transl Med. 2015, 3 (7): 96. PMC 4430733
 . PMID 26015938. doi:10.3978/j.issn.2305-5839.2015.03.60.
. PMID 26015938. doi:10.3978/j.issn.2305-5839.2015.03.60. - Health, Center for Devices and Radiological. . www.fda.gov. [2018-01-17]. (原始内容存档于2018-01-25) (英语).
- (PDF). European Medicines Agency. [2018-01-17]. (原始内容存档 (PDF)于2018-01-17).
- Patel, Harun; Pawara, Rahul; Ansari, Azim; Surana, Sanjay. . European Journal of Medicinal Chemistry. 2017, 142: 32–47 [2019-07-17]. PMID 28526474. doi:10.1016/j.ejmech.2017.05.027. (原始内容存档于2018-08-23).
- Wang, Shuhang; Song, Yongping; Liu, Delong. . Cancer Letters. 2017, 385: 51–54 [2019-07-17]. PMID 27840244. doi:10.1016/j.canlet.2016.11.008. (原始内容存档于2020-09-01).
- (PDF). wuxuwang. 2021-06-01 [2021-06-01]. (原始内容存档 (PDF)于2021-08-23) (cn).
- Yver, A. . Annals of Oncology. June 2016, 27 (6): 1165–70 [2019-07-17]. PMID 26961148. doi:10.1093/annonc/mdw129. (原始内容存档于2017-02-27).
- . FDA Center for Drug Evaluation and Research. 2015-11-13 [2019-07-17]. (原始内容存档于2017-02-27) (英语).
- (PDF). AHRQ. December 2015 [2019-07-17]. (原始内容 (PDF)存档于2017-04-30).