放能反應
放能反應(英語:Exergonic reaction)是化學反應中的自由能改變為負值(有自由能的淨釋放),[1]這表示如果封閉系統中的初始和最終溫度相同,則會發生自發過程。對於在恆定壓力和溫度下在封閉系統中進行的過程中使用吉布斯自由能,而亥姆霍茲自由能則是與恆定體積和溫度下進行的反應有關。根據熱力學第二定律,在沒有輸入電能或光子能量的情況下,在恆定溫度下發生的任何反應都是放能的,例如:細胞呼吸。
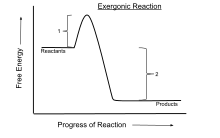
放能反應(例如:細胞呼吸)是在反應過程中釋放自由能的反應。 該反應的進度由該線顯示。 活化能(1)減慢了反應速度。放能反應(在恆定的壓力和溫度下)的吉布斯自由能,因為能量損失(2),(ΔG)的變化為負。
象徵性地,在一次放能反應(在恆定壓力和溫度下)下釋放的自由能ΔG表示為:
儘管放能反應是自發反應的,但這並不意味著該反應可被肉眼所見的速度發生,例如:過氧化氫的歧化反應釋放自由能,但在沒有合適的催化劑的情況下的反應速度非常緩慢。在這種情況下,渴望(英語:eager)[2]是一個更直觀的術語。更籠統地說,放能反應(英語:exergonic)和吸能反應(英語:endergonic)(參見:同化作用)涉及任何過程中的自由能變化不僅僅是化學反應,相反,放熱過程(英語:exothermic)和吸熱過程(英語:endothermic)封閉系統中的焓變,通常與熱交換有關。
參見
- 吸能反應(英語:Endergonic reaction)
參考資料
- IUPAC Gold Book definition: exergonic reaction (exoergic reaction) (页面存档备份,存于)
- Hamori, Eugene; James E. Muldrey. . Journal of Chemical Education. 1984, 61 (8): 710. Bibcode:1984JChEd..61..710H. doi:10.1021/ed061p710.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.