氯化镨
氯化镨(III)是一种无机化合物,化学式为PrCl3。它是蓝绿色的固体,在潮湿空气中迅速吸水,转变为亮绿色的七水合物。
| 氯化镨 | |||
|---|---|---|---|
-chloride-heptahydrate.jpg.webp) | |||
| |||
| IUPAC名 氯化镨 Praseodymium(III) chloride | |||
| 别名 | 三氯化镨 | ||
| 识别 | |||
| CAS号 | 10361-79-2 ? | ||
| PubChem | 66317 | ||
| SMILES |
| ||
| InChI |
| ||
| 性质 | |||
| 化学式 | PrCl3 | ||
| 247.24 g/mol(无水) 373.77 g/mol(七水) g·mol⁻¹ | |||
| 外观 | 蓝绿色固体(无水) 亮绿色固体(七水) | ||
| 密度 | 4.02 g/cm3(无水) 2.250 g/cm3(七水) | ||
| 熔点 | 786 °C | ||
| 沸点 | 1905 °C[1] | ||
| 溶解性(水) | 104.0 g/100 ml (13°C) | ||
| 结构 | |||
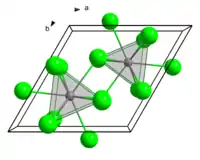
| 晶体结构 | 六方[1],hP8 | ||
| 空间群 | P63/m, No. 176 | ||
| 配位几何 | Tricapped trigonal prismatic (nine-coordinate) | ||
| 危险性 | |||
| 欧盟编号 | 未列出 | ||
| 主要危害 | 有刺激性 | ||
| 相关物质 | |||
| 其他阴离子 | 三氟化镨 溴化镨 碘化镨 硝酸镨 | ||
| 其他阳离子 | 氯化铈 氯化钕 | ||
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |||
制备
- 2 Pr + 6 HCl → 2 PrCl3 + 3 H2
它通常通过真空升华法提纯[4]
氯化镨的水合物可以由金属镨或碳酸镨(III)与盐酸溶液反应得到:
- Pr2(CO3)3 + 6 HCl + 15 H2O → 2 [Pr(H2O)9]Cl3 + 3 CO2
无水氯化镨可以利用氯化铵在400℃对其水合物作用来脱水,[4][5]也可以用氯化亚砜来脱水[4][6][1]:
- PrCl3·6H2O + 6 SOCl2 → PrCl3 + 6 SO2↑ + 12 HCl↑
- 4 Pr2O3 + 3 S2Cl2 + 9 Cl2 → 8 PrCl3 + 6 SO2 (400~700℃反应)
- 4 Pr2O3 + 12 S2Cl2 → 8 PrCl3 + 2 SO2 + 18 S (250~500℃反应)
- Pr2O3 + 3 SOCl2 → 2 PrCl3 + 3 SO2 (450℃反应)
- Pr2O3 + 3 CCl4 → 2 PrCl3 + 3 Cl2 + 3 CO (400~500℃反应)
- Pr2O3 + 6 NH4Cl → 2 PrCl3 + 3 H2O + 6 NH3 (加热反应)
化学反应
氯化镨是一种路易斯酸,根据HSAB理论归类为“硬”。对水合氯化镨的迅速加热会产生少量的水解,产生PrOCl。[4][7]
无水氯化镨很容易吸水并潮解[7],也能吸收氨,生成氨合物(PrCl3·nNH3)。[1]
氯化镨和氯化钾反应,可以形成一个稳定的路易斯酸碱络合物K2PrCl5,这种化合物展现出有趣的光学和磁的性质.[2]
氯化镨的水溶液可以制备难溶的镨化合物。例如,磷酸镨(III)和氟化镨(III)可以通过相应的复分解反应制备:
- PrCl3 + K3PO4 → PrPO4 + 3 KCl
- PrCl3 + 3 NaF → PrF3 + 3 NaCl
当和碱金属氯化物加热时,会形成一系列的三元化合物,它们的化学式为MPr2Cl7, M3PrCl6、 M2PrCl5和M3Pr2Cl9。(其中M = K, Rb, Cs)[8]
参考资料
- 《无机化学丛书》.第七卷 钪 稀土元素.易宪武 等. 科学出版社. ISBN 978-7-03-030574-9. 1.3.3 氧化态+3的化合物. P160. 2. 卤素化合物
- J. Cybinska, J. Sokolnicki, J. Legendziewicz, G. Meyer, Journal of Alloys and Compounds, 341, 115–123 (2002).
- L. F. Druding, J. D. Corbett, "Lower Oxidation States of the Lanthanides. Neodymium(II) Chloride and Iodide", J. Am. Chem. Soc. 83, 2462 (1961); J. D. Corbett, Rev. Chim. Minerale 10, 239 (1973),
- F. T. Edelmann, P. Poremba, in: Synthetic Methods of Organometallic and Inorganic Chemistry, (W. A. Herrmann, ed.), Vol. 6, Georg Thieme Verlag, Stuttgart, 1997.
- M. D. Taylor, P. C. Carter, "Preparation of anhydrous lanthanide halides, especially iodides", J. Inorg. Nucl. Chem., 24, 387 (1962); J. Kutscher, A. Schneider, Inorg. Nucl. Chem. Lett., 7, 815 (1971).
- J. H. Freeman, M. L. Smith, "The preparation of anhydrous inorganic chlorides by dehydration with thionyl chlorid", J. Inorg. Nucl. Chem., 7, 224 (1958).
- Rare Earth Coordination Chemistry: Fundamentals and Applications. Chun-Hui Huang. John Wiley & Sons (Asia) Pte. Ltd. 2 Clementi Loop, #02-01, Singapore 129809. p26. 1.5.2 Rare Earth Halide and Perchlorate Compounds
- Gerd Meyer, "Ternary Chlorides and Bromides of the Rare-Earth Elements", Inorganic Syntheses, 1990, Volume 30, pp. 72–81. doi:10.1002/9780470132616.ch15
补充阅读
- CRC Handbook of Chemistry and Physics (58th edition), CRC Press, West Palm Beach, Florida, 1977.
- N. N. Greenwood, A. Earnshaw, Chemistry of the Elements, Pergamon Press, 1984.
- S. Sugiyama, T. Miyamoto, H. Hayashi, M. Tanaka, J. B. Moffat Journal of Molecular Catalysis A, 118, 129-136 (1997).
- Druding L. F., Corbett J. D., Ramsey B. N. . Inorganic Chemistry. 1963, 2 (4): 869–871. doi:10.1021/ic50008a055.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.
_2.png.webp)