硫酸钠
硫酸钠是一种无机化合物,化学式为Na2SO4,是一种白色固体,易溶于水。其十水合物的年产量为600万吨,是一种主要的化工产品。它主要用于制造粉状家用洗衣剂的填料,应用于纸浆制造中的硫酸盐制浆法,以及制造高碱性的硫化物。[3]
| 硫酸钠 | |
|---|---|
 | |
 | |
| IUPAC名 Sodium sulfate | |
| 别名 | 元明粉 芒硝 格勞勃鹽 |
| 识别 | |
| CAS号 | 7757-82-6 7727-73-3(十水) |
| PubChem | 24436 |
| ChemSpider | 22844 |
| SMILES |
|
| InChI |
|
| ChEBI | 32149 |
| RTECS | WE1650000 |
| 性质 | |
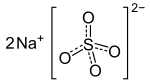
| 化学式 | Na2SO4 |
| 无水:142.04 g/mol 十水:322.20 g·mol⁻¹ | |
| 外观 | 白色結晶狀固體 有吸濕性 |
| 氣味 | 无味 |
| 密度 | 2.664 g/cm3(无水) 1.464 g/cm3(十水) |
| 熔点 | 884 °C(1157 K) |
| 沸点 | 1429 °C(1702 K) |
| 溶解性(水) | 无水: 4.76 g/100 mL (0 °C) 28.1 g/100 mL (25 °C)[1] 42.7 g/100 mL (100 °C) 十水: 19.5 g/100 mL (0 °C) 44 g/100 mL (20 °C) |
| 溶解性 | 难溶于乙醇 可溶于甘油、水和碘化氢 |
| 磁化率 | −52.0·10−6 cm3/mol |
| 折光度n D |
1.468(无水) 1.394(十水) |
| 结构 | |
| 晶体结构 | 斜方(无水)[2] 单斜(十水) |
| 药理学 | |
| ATC代码 | A06AD13(A06),A12 |
| 危险性 | |
| 主要危害 | 刺激性 |
| NFPA 704 |
 0
1
0
|
| 闪点 | 不可燃 |
| 相关物质 | |
| 其他阴离子 | 硒酸钠 碲酸钠 |
| 其他阳离子 | 硫酸锂 硫酸钾 硫酸铷 硫酸铯 |
| 相关化学品 | 硫酸氢钠 亚硫酸钠 过硫酸钠 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
形态
历史
十水硫酸钠被称为格勞勃鹽,以荷兰/德国化学家和药剂师約翰·格勞勃的名字命名。他于1625年在奥地利的泉水中发现了这种盐。因为其晶体具有通用泻药的药用价值,将其命名为(神奇的盐),直到20世纪才發现其他有類似作用的藥物[8][9]。
在18世纪,芒硝开始被用作工业生产纯碱(碳酸钠)的原料。由于对纯碱的需求增加,硫酸钠的供应也必须相应增加。因此在19世纪,大规模的勒布朗制鹼法以生产合成硫酸钠作为关键的中间物质,成为纯碱生产的主要方法。[10]
化学性质
硫酸钠是一种典型的静电结合的离子硫酸盐。当加入钡或铅盐形成难溶性硫酸盐,可证明溶液中存在游离的硫酸根离子:
- Na2SO4 + BaCl2 → 2 NaCl + BaSO4
硫酸钠对大多数氧化剂或还原剂都没有反应。在高温下,它可以通过碳热还原转化为硫化钠:[11]
- Na2SO4 + 2 C → Na2S + 2 CO2
这一反应被用于勒布朗工艺,这是一条已经过时的生产碳酸钠的工业路线。
- Na2SO4 + H2SO4 ⇌ 2 NaHSO4
硫酸钠略微显示出形成复盐的性质。与常见的三价金属形成的矾只有NaAl(SO4)2(在39℃以上不稳定)和NaCr(SO4)2,而硫酸钾和硫酸铵则形成许多稳定的矾。[14]
物理性质

硫酸钠在水中具有不寻常的溶解特性。[15]其在水中的溶解度在0°C和32.384°C之间上升了10倍以上,達到的最大值为49.7 g/100 mL,隨後溶解度逐漸下降,這個溫度对应结晶水的释放和水合盐的熔化,可作为温度计校准的精确温度参考。
结构
十水合物的晶体由具有八面体形分子构型的[Na(H2O)6]+离子组成。这些八面体共享边,故10个水分子中有8个与钠结合,另外2个是间隙性的,与硫酸根氢键结合。这些阳离子通过氢键与硫酸根阴离子相连。Na-O的距离约为240pm。结晶的十水硫酸钠在水合盐中也是不寻常的,它具有可测量的余熵(绝对零度时的熵),为6.32J/(K-mol)。这是因为与大多数水合物相比,它能够更迅速地分布水。[16]
生产
硫酸钠的世界产量,几乎完全以十水合物的形式存在,每年约为550万至600万吨(Mt/a)。1985年产量为450Mt/a,一半来自自然资源,一半来自化工生产。21世纪后在2006年之前处于稳定的水平,自然生产增加到4Mt/a,化学生产减少到1.5至2 Mt/a,总产量为5.5至6 Mt/a。[17][18][19][20]对于所有的应用,自然生产和化学生产的硫酸钠实际上可互换。
自然资源
世界上三分之二的十水盐产量来自矿物芒硝,例如在萨斯喀彻温省南部的湖床上发现的。1990年,墨西哥和西班牙是世界上自然硫酸钠的主要生产国(各约50万吨),俄罗斯、美国和加拿大各约35万吨。[18]天然资源估计在10亿吨以上。[17][18]
用以制备硫酸钠的天然矿物主要有芒硝、无水芒硝、钙芒硝三种,其中芒硝和无水芒硝为硫酸钠及其水合物,钙芒硝为含钙钠的硫酸盐矿物,化学式为Na2Ca(SO4)2,理论成分为22.29%Na2O,20.16%CaO,57.55%SO3,单斜晶系。这三种矿石均主要用于工业制备无水硫酸钠和硫化钠,且其矿床常有互相伴生关系。[21]
化学生产
世界上大约三分之一的硫酸钠是作为化学工业中其他工艺的副产品生产的。这种生产的大部分是初级工艺中固有的化学成分,而且只有很小的经济效益。作为副产品的硫酸钠生产正在下降。
最重要的硫酸钠化学生产是在盐酸生产过程中,在曼海姆工艺中由氯化钠和硫酸生产,或在哈格里夫斯工艺中由二氧化硫生产。这些过程中产生的硫酸钠被称为盐饼。
- 2 NaCl + H2SO4 → 2 HCl + Na2SO4
- 4 NaCl + 2 SO2 + O2 + 2 H2O → 4 HCl + 2 Na2SO4
硫酸钠的第二个主要生产过程是用硫酸中和剩余的氢氧化钠。这种方法也是一种经常应用和方便的实验室制备方法。
- 2 NaOH(aq) + H2SO4(aq) → Na2SO4(aq) + 2 H2O(l) ΔH = -112.5 kJ(高度放热)
在实验室中,它也可以从碳酸氢钠和硫酸镁的反应中,通过沉淀碳酸镁制备。
- 2 NaHCO3 + MgSO4 → Na2SO4 + MgCO3 + CO2 + H2O
由于商业来源很容易获得,通常不会在实验室制备。
过去硫酸钠也是制造重铬酸钠的副产品,将硫酸加入铬酸钠溶液中形成重铬酸钠,或随后形成铬酸。另外,硫酸钠在生产碳酸锂、螯合剂、间苯二酚、抗坏血酸、硅石颜料、硝酸和苯酚的过程中形成或曾经形成。[17]
散装硫酸钠通常通过十水合物形式提纯,因为无水形式往往会吸引铁化合物和有机化合物。通过温和加热,无水物很容易从水合物中产生。
应用
商業用途
硫酸钠是一种非常便宜的材料。最大的用途是作为家用洗衣粉的填充剂,消耗了世界产量的大约50%。随着消费者逐渐改用不含硫酸钠的紧凑型或液体洗涤剂,这种用途正在减少。[17]
造纸业
硫酸钠以前的另一个主要用途是用于制造木浆的硫酸盐制浆法。然而,由于在20世纪60年代初牛皮纸回收过程中热效率的提高,实现了更有效的硫回收,对硫酸钠的需求也大幅减少。[22] 因此,美国和加拿大纸浆行业对硫酸钠的使用从1970年的每年140万吨下降到2006年的大约15万吨。
玻璃制造
玻璃工业是硫酸钠的另一个重要用途,是欧洲的第二大用途。硫酸钠被用作熔炼剂,以帮助去除熔融玻璃中的小气泡。它能使玻璃透明,并防止玻璃熔体在精炼过程中形成浮渣。从1970年到2006年,欧洲的玻璃工业每年的消费量稳定在110,000吨。[23]
纺织面料
硫酸钠在纺织品的生产中很重要,尤其在日本。添加硫酸钠是为了增加溶液的离子强度,减少纺织纤维上的负电荷,使染料能够均匀地渗透。与替代品氯化钠不同,它不会腐蚀用于染色的不锈钢容器。2006年,日本和美国的这种应用消耗了大约10万吨。[17]
热储存
硫酸钠在从固体到液体的相变中具有很高的储热能力,以及32 °C(90 °F)的有利相变温度,使这种材料特别适合于储存低级别的太阳能热量,以便未来在空间升温中释放。在一些应用中,该材料被纳入放置在阁楼空间的热瓦中,而在其他应用中,该盐被纳入被太阳能加热的水包围的电池中。相变使得有效储热所需的材料质量大幅降低(十水硫酸钠的熔融热为82kJ/mol或252kJ/kg[25]),而且只要有足够的适当相的材料,温度就能保持一致。
对于冷却应用,与氯化钠(NaCl)的混合物将熔点降低到18 °C(64 °F)。NaCl·Na2SO4·10H2O混合物的熔化热略微增加到286kJ/kg。[26]
小规模应用
在实验室中,无水硫酸钠广泛用于惰性中性干燥剂,用于去除有机溶液中的微量水分。[27]它比类似的硫酸镁更有效,但作用较慢。它只在30℃以下有效,但由于其化学性质相当惰性,所以可以用于各种材料。
十水硫酸钠被用作泻药。它可以有效从体内清除扑热息痛(对乙酰氨基酚)等药物,如在用药过量之后。[28][29]
1953年,硫酸钠被提议用于被动式太阳能采暖系统的蓄热。这利用了其不寻常的溶解特性和高结晶热(78.2kJ/mol)。[30]
硫酸钠的其他用途包括为窗户除霜、淀粉制造、作为地毯清新剂的添加剂,以及作为牛饲料的添加剂。
至少有一家公司Thermaltake,在絎縫塑料墊內使用十水硫酸鈉製造筆記本電腦冷卻墊(iXoft Notebook Cooler)。該材料會慢慢變成液體並再循環,從而平衡筆記本電腦的溫度並起到絕緣作用。[31]
安全性
虽然硫酸钠通常被认为是无毒的[24],但应小心处理。粉尘可能导致暂时性哮喘或眼睛刺激,这种风险可以通过使用眼睛保护和纸质面具来预防。
参考资料
- . PubChem. [2023-05-06]. (原始内容存档于2023-04-18) (英语).
- Zachariasen, W. H.; Ziegler, G. E. . Zeitschrift für Kristallographie, Kristallgeometrie, Kristallphysik, Kristallchemie (Wiesbaden: Akademische Verlagsgesellschaft). 1932, 81 (1–6): 92–101. S2CID 102107891. doi:10.1524/zkri.1932.81.1.92.
- Helmold Plessen. . Ullmann's Encyclopedia of Industrial Chemistry (Weinheim: Wiley-VCH). 2000. ISBN 978-3527306732. doi:10.1002/14356007.a24_355.
- 叶铁林. . 北京: 北京工业大学出版社. 2006: 380–381. ISBN 7-5639-7157-2 (中文(简体)).
- 许晓慧. . 北京: 中央广播电视大学出版社. 2014: 72–73. ISBN 978-7-304-06061-9 (中文(简体)).
- 姚迎等. . 济南: 济南出版社. 1995: 95. ISBN 7-80572-969-7 (中文(简体)).
- 化学工业部天津化工研究院. . 北京: 化学工业出版社. 1982: 441. ISBN 7-5025-0203-3 (中文(简体)).
- Szydło, Zbigniew. . Polish Academy of Sciences, Institute for the History of Science. [2023-05-06]. ISBN 978-83-86062-45-4 (英语).
- Westfall, Richard S. . The Galileo Project. 1995. (原始内容存档于2011-11-18).
- Aftalion, Fred. . Philadelphia: University of Pennsylvania Press. 1991: 11–16. ISBN 978-0-8122-1297-6.
-
 71st. Ann Arbor, Michigan: CRC Press. 1990. ISBN 9780849304712.
71st. Ann Arbor, Michigan: CRC Press. 1990. ISBN 9780849304712. - 7th. Rahway, New Jersey, US: Merck & Co. 1960.
- Nechamkin, Howard.
 . New York: McGraw-Hill. 1968.
. New York: McGraw-Hill. 1968. - Lipson, Henry; Beevers, C. A. . Proceedings of the Royal Society A. 1935, 148 (865): 664–80. Bibcode:1935RSPSA.148..664L. doi:10.1098/rspa.1935.0040
 .
. - Linke, W. F.; A. Seidell. 4th. Van Nostrand. 1965. ISBN 978-0-8412-0097-5.
- Brodale, G.; W. F. Giauque. . Journal of the American Chemical Society. 1958, 80 (9): 2042–2044. doi:10.1021/ja01542a003.
- Suresh, Bala; Kazuteru Yokose. . CEH Marketing Research Report (Zurich: Chemical Economic Handbook SRI Consulting). May 2006: 771.1000A–771.1002J. (原始内容存档于2007-03-14).
- . Reston, Virginia: US Geological Survey, Minerals Information. 1997 [2007-04-22]. (原始内容存档于2007-03-07).
- Eighth. London: Roskill Information Services. 1999.
- . London: Chem Systems International. November 1984.
- 《矿产资源工业要求手册》编委会. 2014修订版. 北京: 地质出版社. 2014: 373–375. ISBN 978-7-116-06850-6 (中文(简体)).
- Smook, Gary. . 2002: 143. (原始内容存档于2016-08-07).
- Min’ko, N. I.; Binaliev, I. M. . Glass and Ceramics. 2013-03-01, 69 (11): 361–365 [2023-05-06]. ISSN 1573-8515. doi:10.1007/s10717-013-9479-8. (原始内容存档于2018-06-10) (英语).
- . World Health Organization. 2000 [2007-06-06]. (原始内容存档于2007-09-04).
- (PDF). [2014-06-19]. (原始内容存档 (PDF)于2015-09-24).
- (PDF). [2014-06-19]. (原始内容存档 (PDF)于2015-09-24). p.8
- Vogel, Arthur I.; B.V. Smith; N.M. Waldron. 3rd. London: Longman Scientific & Technical. 1980.
- Cocchetto, D.M.; G. Levy. . J Pharm Sci. 1981, 70 (3): 331–3. PMID 7264905. doi:10.1002/jps.2600700330.
- Prescott, L. F.; Critchley, J. A. J. H. . Annual Review of Pharmacology and Toxicology. 1979, 23: 87–101. PMID 6347057. doi:10.1146/annurev.pa.23.040183.000511.
- Telkes, Maria. . British Patent No. GB694553. 1953 [2023-05-05]. (原始内容存档于2008-10-06).
- . Thermaltake Technology Co., Ltd. [2015-08-15]. (原始内容存档于2016-03-12).
外部链接
- Calculators: surface tensions (页面存档备份,存于), and densities, molarities and molalities (页面存档备份,存于) of aqueous sodium sulfate