不成對電子
不成對電子指在分子軌道中只以單顆存在的電子,而不形成電子對。原子的分子軌道能容納一對不同自旋的電子,而成對的電子較為穩定,電子常以化學鍵或孤電子對的方式存在,不成對電子在化學中是相對罕見的。具有不成對電子的原子則較易發生反應。在有機化學中,不成對電子以自由基的形式短暫出現於化學反應中,此概念在以解釋反應的過程尤為重要。
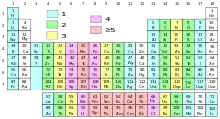
圖中著色的元素具有不成對電子
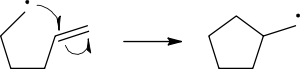
自由基生成環化反應
簡介
自由基很少出現在s區及p區的反應中,因不成對電子佔用p價軌域、sp、sp2或sp3的混成軌域。這些軌域方向性極強,傾向交疊以形成強共價鍵,使自由基傾向組成穩定的二聚體。若電子成對會形成較弱的鍵,自由基會更為穩定;或不成對電子以離域電子的形式穩定存在。在d和f軌域中的自由基是頗常見的,因這兩種軌域較不具方向性和分散,其擴展較小,因此不成對電子較難交疊,傾向形成較弱的鍵,不利二聚體組成。[1]
在一些穩定的分子中也會出現不成對電子。氧原子中有兩顆不成對電子,而一氧化氮中有一顆。同一分子軌道中的電子對自旋方向相反,它們的磁矩會互相抵消。而不成對電子則具磁矩,使其原子成為磁偶極並與磁場交互作用。據洪德最大多重度規則,氧分子中不成對電子的自旋方向必然一致,因此氧元素表現出順磁性。其他具不成對電子的物質也可表現出鐵磁性、反鐵磁性等。
鑭系元素及錒系元素中的不成對電子是最穩定的,它們的f軌域不太與外界反應,不成對電子更難形成化學鍵。具有最多不成對電子的離子是Gd3+和Cm3+,有七顆不成對電子。
參考
- N. C. Norman. . Oxford University Press. 1997: 43. ISBN 0-19-855961-5.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.