正丁胺
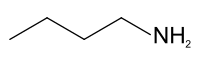
正丁胺是一种胺,化学式 CH3(CH2)3NH2。这种无色液体是一种是丁胺的四个异构体之一,剩下三个为仲丁胺、叔丁胺和异丁胺。它有类似其它胺的鱼味和氨味。该液体在空气中储存后呈黄色,可溶于所有有机溶剂。
| 正丁胺 | |
|---|---|
 | |
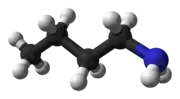 | |
| IUPAC名 Butan-1-amine | |
| 英文名 | |
| 别名 |
|
| 识别 | |
| 缩写 | NBA |
| CAS号 | 109-73-9 |
| PubChem | 8007 |
| ChemSpider | 7716 |
| SMILES |
|
| Beilstein | 605269 |
| Gmelin | 1784 |
| UN编号 | 1125 |
| EINECS | 203-699-2 |
| ChEBI | 43799 |
| RTECS | EO29750002 |
| DrugBank | DB03659 |
| MeSH | n-butylamine |
| 性质 | |
| 化学式 | C4H11N |
| 摩尔质量 | 73.14 g·mol−1 |
| 外观 | 无色液体 |
| 氣味 | 鱼味,氨味 |
| 密度 | 740 mg mL−1 |
| 熔点 | -49 °C(224 K) |
| 沸点 | 77-79 °C(350-352 K) |
| 溶解性(水) | 混溶 |
| log P | 1.056 |
| 蒸氣壓 | 9.1 kPa (当 20 °C) |
| kH | 570 μmol Pa−1 kg−1 |
| pKb | 3.22 |
| 磁化率 | -58.9·10−6 cm3/mol |
| 折光度n D |
1.401 |
| 黏度 | 500 µPa s(当 20 °C) |
| 热力学 | |
| ΔfHm⦵298K | −128.9–−126.5 kJ mol−1 |
| ΔcHm⦵ | −3.0196–−3.0174 MJ mol−1 |
| 热容 | 188 J K−1 mol−1 |
| 危险性 | |
GHS危险性符号   | |
| GHS提示词 | DANGER |
| H-术语 | H225, H302, H312, H314, H332 |
| P-术语 | P210, P280, P305+351+338, P310 |
| NFPA 704 |
 3
2
0
|
| 爆炸極限 | 1.7–9.8% |
| PEL | C 5 ppm (15 mg/m3) [skin][1] |
| 致死量或浓度: | |
LD50(中位剂量) |
|
LCLo(最低) |
4000 ppm (rat, 4 hr) 263 ppm (mouse, 2 hr)[2] |
| 相关物质 | |
| 相关烷基胺 | |
| 相关化学品 | 2-甲基-2-亚硝基丙烷 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
制备和反应
正丁胺可以由正丁醇和氨在氧化铝上反应而成:
- CH3(CH2)3OH + NH3 → CH3(CH2)3NH2 + H2O
正丁胺是一种弱碱。[CH3(CH2)3NH3]+ 的pKa为 10.78。[3]
正丁胺表现出其他简单烷基胺的典型反应,即烷基化、酰基化、以及与羰基化合物缩合。它也会和金属离子形成配合物,例如顺式和反式的[PtI2(NH2Bu)2]。[4]
用处
正丁胺可用于生产农药(如硫代碳酰肼)、药品和乳浊液。它也是N,N′-二正丁基硫脲,一种橡胶硫化加速剂和N-丁基苯磺酰胺,一种尼龙的塑化剂的前体。它也用于生产芬加宾、杀真菌剂苯菌灵和抗糖尿病药甲苯磺丁脲。[5]

正丁胺是杀真菌剂苯菌灵的前体
安全
正丁胺的LD50 为 366 mg/kg(大鼠,口服)。[6]
关于职业暴露于正丁胺,美国职业安全卫生署和美国国家职业安全卫生研究所已将皮肤接触的职业接触限值设为 5 ppm (15 mg/m3)。[7]
参考资料
- NIOSH Pocket Guide to Chemical Hazards. . NIOSH.
- . Immediately Dangerous to Life and Health Concentrations (IDLH). National Institute for Occupational Safety and Health (NIOSH).
- H. K. Hall, Jr. . J. Am. Chem. Soc. 1957, 79 (20): 5441–5444. doi:10.1021/ja01577a030.
- Rochon, Fernande D.; Buculei, Viorel. . Inorganica Chimica Acta. 2004, 357 (8): 2218–2230. doi:10.1016/j.ica.2003.10.039.
- Karsten Eller, Erhard Henkes, Roland Rossbacher, Hartmut Höke, "Amines, Aliphatic" Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2005.doi:10.1002/14356007.a02_001
- (PDF). [2013-11-12]. (原始内容 (PDF)存档于2013-11-12).
- . [2021-09-11]. (原始内容存档于2021-12-17).
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.