六甲苯
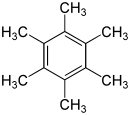
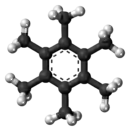
六甲苯是一种碳氢化合物,化学式 C12H18,结构式 C6(CH3)6。它是由苯的六个氢原子都被甲基取代而生的化合物。1929年,凯瑟琳·朗斯代尔报告了六甲苯的晶体结构,证明苯环是平面六边形的[1],从而结束了关于苯的结构的持续争论。无论是对于X射线晶体学抑或研究芳香性的領域,這皆是一個具有歷史意義的成果。[2][3]
| 六甲苯 | |
|---|---|
 | |
 | |
 | |
| IUPAC名 Hexamethylbenzene | |
| 别名 | 1,2,3,4,5,6-六甲基苯 六甲基苯 |
| 识别 | |
| CAS号 | 87-85-4 |
| PubChem | 6908 |
| ChemSpider | 6642 |
| SMILES |
|
| InChI |
|
| InChIKey | YUWFEBAXEOLKSG-UHFFFAOYAF |
| ChEBI | 39001 |
| 性质 | |
| 化学式 | C12H18 |
| 摩尔质量 | 162.27 g·mol−1 |
| 外观 | 白色晶体 |
| 密度 | 1.0630 g cm−3 |
| 熔点 | 164.9-166.3 °C(438-439 K) |
| 沸点 | 265.2 °C(538 K) |
| 溶解性(水) | 不溶 |
| 溶解性 | 乙酸、丙酮、苯、氯仿、乙醚和乙醇 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
六甲苯可以通过苯酚与甲醇在高温和合适的固体催化剂(如氧化铝)下反应而生成。[4][5][6]这个反应的反应机理已被广泛研究,[7][8][9][10] 過程中含有几种反应中间体的存在。[6][11][12]在合适的催化剂存在下[13][14],二甲基乙炔的炔烃三聚也可生成六甲基苯。[15]六甲基苯可以被氧化成苯六甲酸,[16]后者的铝盐存在于稀有矿物蜜蠟石中。[17] 六甲基苯也是有机金属化合物中的一种配體。[18]其中一个例子是随着钌原子氧化态变化而改变结构的有机钌化合物,[19][20]而这个变化不存在于对应的有机铁化合物中。[19]
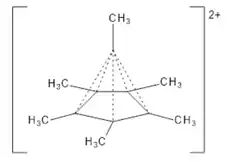
2016年,《应用化学》[21]報告了六甲基苯双阳离子的晶體結構。顯示出的結構為金字塔形,其中一個碳原子與其他六个碳原子具有鍵合相互作用。[22][23]这个结构是“空前未見的”,[21]因为碳通常的最高化合价是四,而这也吸引了《新科学人》、[22]《化学化工新闻》[23]和《科学新闻》等的注意。[24]这种结构並没有违反八隅体规则,因为这些碳-碳键不是两电子键。此結構在教學上可作為例子,说明碳原子“可以与四个以上的原子直接结合”。[24]斯蒂芬·巴哈拉赫證明了六甲基苯双阳离子是超配位的,而不是超价分子,并解释了其芳香性。[25]此类物种中的键合可以從有机金属化学的视角描述,此想法在1975年提出,[26]緊隨C
6(CH
3)2+
6的發現。[27][28][29]
性质
六甲苯是一种芳香化合物,有六个π电子(符合休克尔规则)離域於整個環狀平面系统之上;六个环碳原子之中的每一个都是sp2 杂化並展現出平面三角形分子构型,而每一个甲基碳皆是sp3杂化並有著四面体形分子构型,与其经验结构的描述一致。[1]六甲苯是一种无色到白色,正交晶系的晶体,[30]熔点 165–166 °C,[5]沸点 268 °C,密度1.0630 g cm−3。[30]它不溶于水,但溶于有机溶剂,例如苯和乙醇。[30]
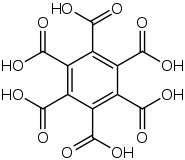
矿物蜜蠟石是苯六甲酸的铝盐的水合物,化学式 Al
2[C
6(CO
2)
6]•16H
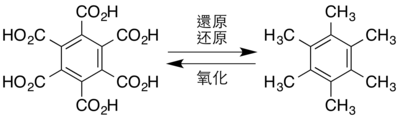
2O。[17]苯六甲酸本身可以从矿物中提取,[31]随着還原反應而产生六甲苯。相反,六甲苯也可以被氧化成苯六甲酸:[16]
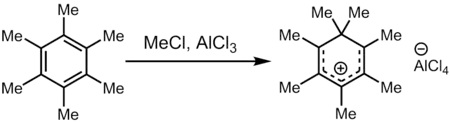
六甲苯和氯甲烷、三氯化铝的超级亲电混合物(Meδ⊕Cl---δ⊖AlCl3的来源)会产生七甲苯阳离子,是最早被直接观察到的碳正离子之一。
制备
1880年,约瑟夫·阿希耶·勒贝勒和威廉·H·葛林报告了[34]一個被形容為“不平凡”的,由氯化锌催化的一鍋合成法,過程中從甲醇合成了六甲苯。[35]在催化剂的熔点下 (283 °C),反应的吉布斯能 (ΔG) 为 −1090 kJ mol−1,反应如下:[35]
- 15 CH
3OH → C
6(CH
3)
6 + 3 CH
4 + 15 H
2O
勒贝勒和葛林提出了理論以解釋這個過程,內容涉及由甲醇脱水而成的亚甲基单元的芳香化,從而生成苯環,接著在原位用氯甲烷進行完全的傅-克甲基化。[35]反应主要产生饱和烃的混合物,六甲苯为次要产物。[36]六甲苯也是对二甲苯傅-克烷基化成均四甲苯的副产物,而通过烷基化均四甲苯或五甲苯产生的六甲苯皆有著可觀產率。[37]
六甲苯通常在高温气相中通过固体催化剂下制备。早期制备六甲苯的方法包括使丙酮和甲醇蒸气的混合物在400 °C的氧化铝催化剂下反应。[38]苯酚和甲醇在 410–440 °C 的乾燥二氧化碳氣體中也会产生六甲苯,[4]尽管它是作为苯甲醚(甲氧基苯)、甲酚(甲基苯酚)和其他甲基化苯酚的複雜混合物的一部分而被生成。[11]在《有機合成》收錄的制備方法中,甲醇和苯酚則在 530 °C的氧化铝催化剂下反应,產率約為66%,[5]而在其他不同條件下進行的合成方法也有被報道。[6]
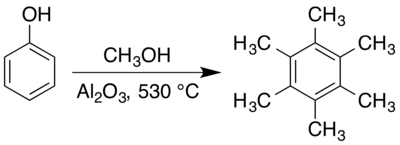
這種表面介導反應的機制已被妥善地研究,研究的過程中着眼於如何更好地控制反應结果,[8][39]特别是在尋找具有選擇性和受控的鄰位甲基化反應。[9][10][40][41]苯甲醚[11]和五甲苯[6]皆被報告為此過程的反應中間體。华伦汀·科普秋格和同事发现,六甲基环己二烯酮的异构体(2,3,4,4,5,6- 和 2,3,4,5,6,6-)亦是反應中的中間體,经過重排反應而形成六甲苯。[7][12]
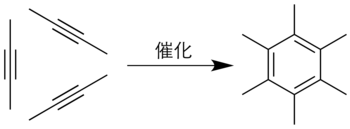
2-丁炔三聚也可以生成六甲苯。[15]此反应可被三苯基三(四氢呋喃)铬[13]或四氯化钛與三异丁基铝的配合物催化。[14]
用处
六甲苯可用作3He-NMR 光谱测试的溶剂。[42]
反应
它亦會被三氟过氧乙酸或过氧化氢氧化,产生 2,3,4,5,6,6-六甲基-2,4-环己二烯酮:[44][7][12]

就像苯本身一样,六甲苯中富含电子的芳香系统使其能在有机金属化学中充当配體。[18] 甲基是推电子基,使得相对于苯,它将中心环的碱性提高六到七个数量级。[45]有各种金属中心的这些配合物已被报告,包括钴、[46]铬、[13]铁、[19]铼、[47]铑、[46]钌[20]和钛。[14]钴和铑和六甲苯化学式 [M(C
6(CH
3)
6)
2]n+ (M = Co, Fe, Rh, Ru; n = 1, 2) 的夹心配合物阳离子,其中金属中心和两个芳烃的π电子结合,并且可以通过配体交换从适当的金属盐轻松合成,例如:[46]
- CoBr
2 + 2 AlBr
3 → [Co(C
6(CH
3)
6)
2]2+
+ 2 AlBr−
4
这些配合物可以参与氧化还原反应。铑和钴配合物的双阳离子可以用合适的活性金属(钴配合物用铝还原,铑配合物用锌还原)进行单电子还原,描述钴配合物的反应方程式如下:[46]
- 3 [Co(C
6(CH
3)
6)
2]2+
+ Al → 3 [Co(C
6(CH
3)
6)
2]+
+ Al3+
2redox_pi-highlight.png.webp)
左:n = 2, [RuII(η6-C6(CH3)6)2]2+
右:n = 0, [Ru0(η4-C6(CH3)6)(η6-C6(CH3)6)]
为清楚起见省略了甲基。与碳-钌键合相关的电子对是红色的
在有机钌化学中,双阳离子和电中性物种在乙腈中的还原电位为 −1.02 V,[19]并且伴随着结构的变化。[20][48]随着钌中心氧化态的变化,其中一个六甲苯配体的哈普托数会变化。[Ru(η6-C6(CH3)6)2]2+ 会还原成 [Ru(η4-C6(CH3)6)(η6-C6(CH3)6)],[20]它的结构变化是用来遵守18电子规则,增强稳定性。
类似的铁(II)配合物的单电子还原可逆(在乙醇水溶液中为−0.48 V),但双电子还原(−1.46 V)不可逆,[19]表明它的结构变化不同于在钌配合物中发现的结构变化。
双阳离子
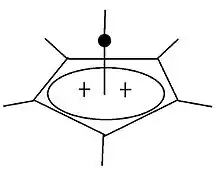
6(CH
3)2+
6的金字塔型碳阳离子
C
6(CH
3)
6H+
在1960年代对六甲基杜瓦苯的调查中首次报道,[49]基于核磁共振的证据提出了金字塔结构,[50]随后得到无序的[21]晶体结构数据的支持。[51]1970年代初期,由赫普克·霍赫芬领导的理论工作预测了金字塔形的双阳离子 C
6(CH
3)2+
6的存在,并且该意见很快得到了实验证据的支持。[27][28][29]对苯在极低温度(低于 4K)下的双电子氧化的光谱学研究表明,形成六边形的双阳离子,然后迅速重新排列成金字塔结构:[52]
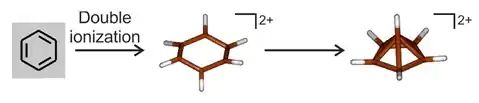
6(2%252B)_3D_skeletal.png.webp)
6(CH
3)2+
6有五角锥结构
一般預料六甲苯的雙電子氧化會令其重排為金字塔型碳陽離子,但以此方法試圖批量合成的嘗試皆沒有成功。[21]然而,在2016年霍赫芬的方法受到了改進,連帶得出了[C
6(CH
3)
6][SbF
6]
2•HSO
3F的高質素晶體結構。它的锥高为 1.18 埃格斯特朗,五个甲基都略高于底面,[21]形成反转的四面体构型。它的制备方法是六甲基杜瓦苯的环氧化物和魔酸反应,离去氧离子 (O2−
),形成双阳离子:[21]
6_(SbF6)2_synthesis.png.webp)
儘管先前的間接光谱證據和理論計算均已表明它們的存在,但對於‘帶有一個僅與其他碳原子結合的六配位碳’的特殊化學物種所做的分離和結構測定仍是前所未有的,[21]并吸引了《化学化工新闻》、[23]《新科学人》、[22]《科学新闻》[24]和ZME Science评论。[53]碳的化合价为四,而该例角锥顶点上的那个碳原子和六个原子键合,并不寻常。[23]该分子是芳香性的,在金字塔的底部与其顶点之间的五个键中总共只有六个电子,可以避免违反八隅体规则。也就是说,金字塔的每个斜边只有部分键,而不是一个正常的共价键。尽管顶部的碳确实与六个原子键合,但它总共使用不超过八个电子。[26]
注意形成双阳离子金字塔斜边的弱键(在结构中显示为虚线),它的键级约为 0.54,因此总键级为 5 × 0.54 + 1 = 3.7 < 4,所以此物种不是超价分子,但它是超配位分子。[25]双阳离子中,有三種不同的碳-碳键,一則環上的鍵,具有芳香性;二則環到甲基的單鍵;三則斜边,是弱的部分键。其差異也反映在碳-碳键长中:环的碳-碳键长为 1.439–1.445 Å(最短),环到甲基的碳-碳键长为 1.479–1.489 Å(居中),而环到六配位碳的碳-碳键长为1.694–1.715 Å(最長)[21]。从有机金属化学的角度来看,该物种可以被视为 [(η5
–C
5(CH
3)
5)C(CH
3)]
。[26]此理解下,碳(IV)的中心 (C4+
),與一个芳香性的 η5–环戊二烯阴离子(六个电子)和甲基阴离子(两个电子)鍵結,從而满足八隅体规则,类似于相关的气相有机锌化合物 [(η5
–C
5(CH
3)
5)Zn(CH
3)] ,其有同樣的配體键结到锌(II)中心(Zn2+
),符合18电子规则。[54][55]
對其評論指出“虽然我们被教导碳只能有四个朋友,但碳其實可以與四个以上的原子相關聯,这一点非常重要”,評論並補充指“從我們一般認為碳-碳键是雙電子鍵的想法出發,碳原子並不會形成六個鍵。”[24]“這一切都是關於讓化學家為無奇不有而感到驚訝的挑戰和可能性。”[22]
参考资料
- Lonsdale, Kathleen. . Proc. R. Soc. A. 1929, 123 (792): 494–515. doi:10.1098/rspa.1929.0081
 .
. - Lydon, John. (PDF). Newsletter of the History of Physcis Group. January 2006, (19): 8–11 [2021-08-29]. (原始内容存档 (PDF)于2017-01-09).
- Lydon, John. (PDF). Newsletter of the History of Physcis Group. July 2006, (20): 34–35 [2021-08-29]. (原始内容存档 (PDF)于2015-09-06).
- Briner, E.; Plüss, W.; Paillard, H. [Research on the catalytic dehydration of phenol-alcohol systems]. Helv. Chim. Acta. 1924, 7 (1): 1046–1056. doi:10.1002/hlca.192400701132 (法语).
- (1955) "Hexamethylbenzene". Org. Synth. 35: 73; Coll. Vol. 4: 520.
- Landis, Phillip S.; Haag, Werner O. . J. Org. Chem. 1963, 28 (2): 585. doi:10.1021/jo01037a517.
- Krysin, A. P.; Koptyug, V. A. . Russ. Chem. Bull. 1969, 18 (7): 1479–1482. doi:10.1007/BF00908756.
- Ipatiew, W.; Petrow, A. D. [On the catalytic condensation of acetone at high temperatures and pressures. (I. Communication)]. Ber. Dtsch. Chem. Ges. A/B. 1926, 59 (8): 2035–2038. doi:10.1002/cber.19260590859 (德语).
- Kotanigawa, Takeshi; Yamamoto, Mitsuyoshi; Shimokawa, Katsuyoshi; Yoshida, Yuji. . Bulletin of the Chemical Society of Japan. 1971, 44 (7): 1961–1964. doi:10.1246/bcsj.44.1961
 .
. - Kotanigawa, Takeshi. . Bull. Chem. Soc. Jpn. 1974, 47 (4): 950–953. doi:10.1246/bcsj.47.950
 .
. - Cullinane, N. M.; Chard, S. J. . J. Chem. Soc. 1945: 821–823. PMID 21008356. doi:10.1039/JR9450000821.
- Shubin, V. G.; Chzhu, V. P.; Korobeinicheva, I. K.; Rezvukhin, A. I.; Koptyug, V. A. . Russ. Chem. Bull. 1970, 19 (8): 1643–1648. doi:10.1007/BF00996497.
- Zeiss, H. H.; Herwig, W. . J. Am. Chem. Soc. 1958, 80 (11): 2913. doi:10.1021/ja01544a091.
- Franzus, B.; Canterino, P. J.; Wickliffe, R. A. . J. Am. Chem. Soc. 1959, 81 (6): 1514. doi:10.1021/ja01515a061.
- Weber, S. R.; Brintzinger, H. H. . J. Organomet. Chem. 1977, 127 (1): 45–54. doi:10.1016/S0022-328X(00)84196-0. hdl:2027.42/22975
 .
. - Wibaut, J. P.; Overhoff, J.; Jonker, E. W.; Gratama, K. . Recl. Trav. Chim. Pays-Bas. 1941, 60 (10): 742–746. doi:10.1002/recl.19410601005.
- Wenk, Hans-Rudolf; Bulakh, Andrey. . 2nd. Cambridge University Press. 2016 [2021-08-29]. ISBN 9781316423684. (原始内容存档于2022-03-14).
- Pampaloni, Guido. . Coord. Chem. Rev. 2010, 254 (5–6): 402–419. doi:10.1016/j.ccr.2009.05.014.
- Kotz, John C. . Fry, Albert J.; Britton, Wayne E. (编). . Springer Science & Business Media. 1986: 83–176 [2021-08-29]. ISBN 9781489920348. (原始内容存档于2021-08-29).
- Huttner, Gottfried; Lange, Siegfried; Fischer, Ernst O. . Angew. Chem. Int. Ed. Engl. 1971, 10 (8): 556–557. doi:10.1002/anie.197105561.
- Malischewski, Moritz; Seppelt, Konrad. . Angew. Chem. Int. Ed. 2017, 56 (1): 368–370. PMID 27885766. doi:10.1002/anie.201608795.
- Boyle, Rebecca. . New Scientist. 14 January 2017, (3108) [14 January 2017]. (原始内容存档于2017-01-16).
- Ritter, Stephen K. . Chem. Eng. News. 19 December 2016, 94 (49): 13 [2021-08-29]. doi:10.1021/cen-09449-scicon007. (原始内容存档于2017-01-09).
- Hamers, Laurel. . Science News. 24 December 2016, 190 (13): 17 [2021-08-29]. (原始内容存档于2017-02-03).
- Bachrach, Steven M. . comporgchem.com. 17 January 2017 [18 January 2017]. (原始内容存档于2017-01-19).
- Hogeveen, Hepke; Kwant, Peter W. . Acc. Chem. Res. 1975, 8 (12): 413–420. doi:10.1021/ar50096a004.
- Hogeveen, Hepke; Kwant, Peter W. . Tetrahedron Lett. 1973, 14 (19): 1665–1670. doi:10.1016/S0040-4039(01)96023-X.
- Hogeveen, Hepke; Kwant, Peter W.; Postma, J.; van Duynen, P. Th. . Tetrahedron Lett. 1974, 15 (49–50): 4351–4354. doi:10.1016/S0040-4039(01)92161-6.
- Hogeveen, Hepke; Kwant, Peter W. . J. Am. Chem. Soc. 1974, 96 (7): 2208–2214. doi:10.1021/ja00814a034.
- Haynes, William M. (编). 93rd. CRC Press. 2016. p. 3-296 [2021-08-29]. ISBN 9781439880500. (原始内容存档于2022-04-27).
- Liebig, Justus. . The Lancet. 1844, 2 (1106): 190–192 [2021-08-29]. doi:10.1016/s0140-6736(02)64759-2. (原始内容存档于2021-08-29).
- Lonsdale, Kathleen. . Nature. 1928, 122 (810): 810. S2CID 4105837. doi:10.1038/122810c0.
- Lonsdale, Kathleen. . George Bell & Sons. 1948.
- Le Bel, Joseph Achille; Greene, William H. . American Chemical Journal. 1880, 2: 20–26.
- Chang, Clarence D. . Catal. Rev. - Sci. Eng. 1983, 25 (1): 1–118. doi:10.1080/01614948308078874.
- Olah, George A.; Doggweiler, Hans; Felberg, Jeff D.; Frohlich, Stephan; Grdina, Mary Jo; Karpeles, Richard; Keumi, Takashi; Inaba, Shin-ichi; Ip, Wai M.; Lammertsma, Koop; Salem, George; Tabor, Derrick. . J. Am. Chem. Soc. 1984, 106 (7): 2143–2149. doi:10.1021/ja00319a039.
- Smith (1930). "Durene". Org. Synth. 10: 32; Coll. Vol. 2: 248.
- Reckleben, Hans; Scheiber, Johannes. [A simple representation of hexamethylbenzene]. Ber. Dtsch. Chem. Ges. 1913, 46 (2): 2363–2365 [2021-08-29]. doi:10.1002/cber.191304602168. (原始内容存档于2021-08-29) (德语).
- Ipatiew, W. N.; Petrow, A. D. [On the catalytic condensation of acetone at high temperatures and pressures (II. Communication)]. Ber. Dtsch. Chem. Ges. A/B. 1927, 60 (3): 753–755. doi:10.1002/cber.19270600328 (德语).
- Kotanigawa, Takeshi; Shimokawa, Katsuyoshi. . Bull. Chem. Soc. Jpn. 1974, 47 (6): 1535–1536. doi:10.1246/bcsj.47.1535
 .
. - Kotanigawa, Takeshi. . Bull. Chem. Soc. Jpn. 1974, 47 (10): 2466–2468. doi:10.1246/bcsj.47.2466
 .
. - Saunders, Martin; Jiménez-Vázquez, Hugo A.; Khong, Anthony. . J. Phys. Chem. 1996, 100 (39): 15968–15971. doi:10.1021/jp9617783.
- Ross, Sidney D.; Bassin, Morton; Finkelstein, Manuel; Leach, William A. . J. Am. Chem. Soc. 1954, 76 (1): 69–74. doi:10.1021/ja01630a018.
- (1968) "2,3,4,5,6,6-Hexamethyl-2,4-cyclohexadien-1-one". Org. Synth. 48; Coll. Vol. 5: 598.
- Earhart, H. W.; Komin, Andrew P., , , New York: John Wiley, 2000, ISBN 9780471238966, doi:10.1002/0471238961.1615122505011808.a01
- Fischer, Ernst Otto; Lindner, Hans Hasso. [About Aromatic Complexes of Metals. LXXVI. Di-hexamethylbenzene metal-π-complexes of mono- and bivalent cobalt and rhodium]. J. Organomet. Chem. 1964, 1 (4): 307–317. doi:10.1016/S0022-328X(00)80056-X (德语).
- Fischer, Ernst Otto; Schmidt, Manfred W. . Chem. Ber. 1966, 99 (7): 2206–2212. doi:10.1002/cber.19660990719.
- Bennett, Martin A.; Huang, T.-N.; Matheson, T. W.; Smith, A. K. 21. 1982: 74–78. ISBN 9780470132524. doi:10.1002/9780470132524.ch16.
|journal=被忽略 (帮助) - Schäfer, W.; Hellmann, H. . Angew. Chem. Int. Ed. Engl. 1967, 6 (6): 518–525. doi:10.1002/anie.196705181.
- Paquette, Leo A.; Krow, Grant R.; Bollinger, J. Martin; Olah, George A. . J. Am. Chem. Soc. 1968, 90 (25): 7147–7149. doi:10.1021/ja01027a060.
- Laube, Thomas; Lohse, Christian. . J. Am. Chem. Soc. 1994, 116 (20): 9001–9008. doi:10.1021/ja00099a018.
- Jašík, Juraj; Gerlich, Dieter; Roithová, Jana. . J. Am. Chem. Soc. 2014, 136 (8): 2960–2962. PMID 24528384. doi:10.1021/ja412109h.
- Puiu, Tibi. . zmescience.com. ZME Science. 5 January 2017 [14 January 2017]. (原始内容存档于2017-01-16).
- Haaland, Arne; Samdal, Svein; Seip, Ragnhild. . J. Organomet. Chem. 1978, 153 (2): 187–192. doi:10.1016/S0022-328X(00)85041-X.
- Elschenbroich, Christoph. . 3rd. John Wiley & Sons. 2006: 59–85 [2021-08-29]. ISBN 9783527805143. (原始内容存档于2022-04-26).

Zn(Me).png.webp)