咖啡酸
咖啡酸(英語:)是一种归属于羟基肉桂酸的有机化合物,同时具有酚羟基和丙烯酸两种官能团结构。因为咖啡酸是生物合成植物生物质及其残留物的主要组分之一木质素的关键中间体,所以它广泛存在于各种植物中[2]。它可以在热水和乙醇中溶解,冷水中微溶。常温下为黄白色结晶体。
| 咖啡酸 | |
|---|---|
 | |
 | |
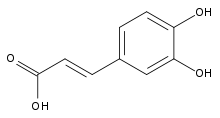
| IUPAC名 3-(3,4-Dihydroxyphenyl 2-propenoic acid 3,4-Dihydroxy-cinnamic acid trans-Caffeate 3,4-Dihydroxy-trans-cinnamate) (E)-3-(3,4-dihydroxyphenyl)-2-propenoic acid | |
| 识别 | |
| CAS号 | 331-39-5 ? |
| PubChem | 689043 |
| ChemSpider | 600426 |
| SMILES |
|
| InChI |
|
| InChIKey | QAIPRVGONGVQAS-DUXPYHPUBE |
| 性质 | |
| 化学式 | C9H8O4 |
| 180.16 g·mol⁻¹ | |
| 密度 | 1.478 g/cm³ |
| 熔点 | 223-225 °C |
| λmax | 327[1] nm |
| 危险性 | |
GHS危险性符号  | |
| GHS提示词 | Warning |
| H-术语 | H315, H319, H335, H351, H361 |
| P-术语 | P201, P202, P261, P264, P271, P280, P281, P302+352, P304+340, P305+351+338, P308+313, P312, P321, P332+313 |
| NFPA 704 |
 1
1
0
|
| 相关物质 | |
| 相关化学品 | 绿原酸 奎尼酸 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
自然中的含量
代谢途径
药理作用
在体外研究和动物模型中发现咖啡酸具有多种潜在的药理作用,通过氧化机制咖啡酸对人HT-1080纤维肉瘤细胞系中的对癌细胞增殖的抑制作用。[12] 咖啡酸在体外和活体内都是一种抗氧化剂[10]。咖啡酸还显示出免疫调节和抗炎活性,咖啡酸能使黄曲霉毒素产量降低超过95%,优于其他抗氧化剂。研究表明否则触发黄曲霉产生黃麴毒素的应激氧化可被咖啡酸阻碍。 对咖啡酸致癌性的研究具有混合的结果[13]。 一部分研究结果表明它抑制致癌作用,另一部分结果显示咖啡酸有致癌作用[13]。对大鼠进行高剂量咖啡酸的口服给药会引起胃乳头状瘤[13]。在相同的研究中,高剂量包含咖啡酸的组合抗氧化剂则能显著减少相同种类大鼠结肠肿瘤的生长[13]。在一些危险物数据表中咖啡酸被列为潜在致癌物,它已被国际癌症研究机构列为2B类致癌物(“可能对人类致癌”)[14]。一些研究数据显示,大鼠肠道中的细菌可能改变咖啡酸代谢产物的形成[15][16]。
化学性质
咖啡酸易于自动氧化。谷胱甘肽以及硫醇类化合物(例如半胱氨酸,巯基乙酸或甲琉酚)或抗坏血酸对咖啡酸的褐变和消失具有抑制作用[17],咖啡酸的褐变是由邻二酚被氧化为邻二醌造成的。在酸性条件下用高碘酸钠对咖啡酸进行化学氧化会生成具有呋喃结构的二聚体(2,5-(3',4'-二羟基苯基)四氢呋喃3,4-二羧酸的异构体)[18]。使用辣根过氧化物酶/过氧化氢的氧化系统能使咖啡酸聚合[19]。
其他用途
咖啡酸也用于蛋白质的基质辅助激光解吸/电离质谱分析的辅助基质[20]。
参考文献
- Gould, Kevin S.; Markham, Kenneth R.; Smith, Richard H.; Goris, Jessica J. . Journal of Experimental Botany. 2000, 51 (347): 1107–1115 [2017-02-05]. PMID 10948238. doi:10.1093/jexbot/51.347.1107. (原始内容存档于2009-06-03).
- Boerjan, Wout; Ralph, John; Baucher, Marie. . Annual Review of Plant Biology. 2003, 54: 519–546 [2017-02-05]. PMID 14503002. doi:10.1146/annurev.arplant.54.031902.134938. (原始内容存档于2021-12-04).
- Santos, Sónia A. O.; Freire, Carmen S. R.; Domingues, M. Rosário M.; Silvestre, Armando J. D.; Pascoal Neto, Carlos Pascoal. . Journal of Agricultural and Food Chemistry. 2011, 59 (17): 9386–93. PMID 21761864. doi:10.1021/jf201801q.
- Choudhary, M. Iqbal; Naheed, Nadra; Abbaskhan, Ahmed; Musharraf, Syed Ghulam; Siddiqui, Hina; Atta-Ur-Rahman. . Phytochemistry. 2008, 69 (4): 1018–23. PMID 18177906. doi:10.1016/j.phytochem.2007.10.028.
- Lee, Y.-S.; Kang, Y.-H.; Jung, J.-Y.; Lee, Sanghyun; Ohuchi, Kazuo; Shin, Kuk Hyun; Kang, Il-Jun; Park, Jung Han Yoon; Shin, Hyun-Kyung; Soon, Sung. . Biological & Pharmaceutical Bulletin. October 2008, 31 (10): 1968–1972 [2017-02-04]. PMID 18827365. doi:10.1248/bpb.31.1968. (原始内容存档于2012-12-19).
- ., Z. Charrouf; ., D. Guillaume. . American Journal of Food Technology. 2007, 2 (7): 679 [2017-02-04]. doi:10.3923/ajft.2007.679.683. (原始内容存档于2020-10-20).
- . [2017-02-04]. doi:10.1155/2013/658596. (原始内容存档于2019-08-23).
- . Journal of Analytical Methods in Chemistry. [2017-02-04]. doi:10.1021/jf2008343. (原始内容存档于2019-12-02).
- Quinde-Axtell, Zory; Baik, Byung-Kee. . J. Agric. Food Chem. 2006, 54 (26): 9978–9984 [2017-02-04]. PMID 17177530. doi:10.1021/jf060974w. (原始内容存档于2021-05-06).
- Olthof, M. R.; Hollman, P. C.; Katan, M. B. . J. Nutr. January 2001, 131 (1): 66–71 [2017-02-05]. PMID 11208940. (原始内容存档于2020-06-26).
- Pierpoint, W. S. . Biochem. J. 1969, 112: 609–616. doi:10.1042/bj1120609.
- Rajendra Prasad, N.; Karthikeyan, A.; Karthikeyan, S.; Reddy, B. V. . Mol Cell Biochem. Mar 2011, 349 (1–2): 11–19. doi:10.1007/s11010-010-0655-7.
- Hirose, M.; Takesada, Y.; Tanaka, H.; Tamano, S.; Kato, T.; Shirai, T. (PDF). Carcinogenesis. 1998, 19 (1): 207–212. PMID 9472713. doi:10.1093/carcin/19.1.207.
- Agents Classified by the IARC Monographs (页面存档备份,存于), International Agency for Research on Cancer
- Peppercorn, M. A.; Goldman, P. . Proceedings of the National Academy of Sciences. 1972, 69 (6): 1413–1415 [2017-02-05]. PMC 426714
 . PMID 4504351. doi:10.1073/pnas.69.6.1413. (原始内容存档于2008-08-08).
. PMID 4504351. doi:10.1073/pnas.69.6.1413. (原始内容存档于2008-08-08). - Gonthier, M.-P.; Verny, M.-A.; Besson, C.; Rémésy, C.; Scalbert, A. . Journal of Nutrition. 1 June 2003, 133 (6): 1853–1859 [2017-02-05]. PMID 12771329. (原始内容存档于2009-04-08).
- Cilliers, Johannes J. L.; Singleton, Vernon L. . J. Agric. Food Chem. 1990, 38 (9): 1789–1796 [2017-02-05]. doi:10.1021/jf00099a002. (原始内容存档于2019-12-02).
- Fulcrand, Hélène; Cheminat, Annie; Brouillard, Raymond; Cheynier, Véronique. . Phytochemistry. 1994, 35 (2): 499–505. doi:10.1016/S0031-9422(00)94790-3.
- Xu, Peng; Uyama, Hiroshi; Whitten, James E.; Kobayashi, Shiro; Kaplan, David L. . J. Am. Chem. Soc. 2005, 127 (33): 11745–11753 [2017-02-05]. doi:10.1021/ja051637r. (原始内容存档于2019-11-30).
- Beavis, R. C.; Chait, B. T. . Rapid Commun. Mass Spectrom. Dec 1989, 3 (12): 432–435 [2017-02-05]. PMID 2520223. doi:10.1002/rcm.1290031207. (原始内容存档于2017-08-27).
