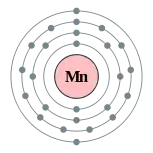
锰
歷史上,錳的名稱來自生產軟錳礦以及其他黑色礦物的希臘馬格尼西亞地區,這個地區的名稱來自其生產鎂以及磁鐵礦。到了大約18世紀中葉時,瑞典裔德國科學家卡爾·威廉·舍勒已經可以利用軟錳礦製造氯氣。這時,舍勒和其他人已經知道軟錳礦(這時還不知道此為二氧化錳)含有其他未被發現的元素,但是他們沒辦法分離出這個新元素。直到1774年,約翰·戈特利布·甘恩是第一個可以從具有不純的金屬樣品分離出錳元素的人,他成功的利用碳還原此氧化物(含二氧化錳的礦物)得到了錳。
錳磷酸化可以用來防止鋼鐵生鏽或者腐蝕。錳離子可以用於各種顏色的工業染劑,離子的顏色決定於其不同的其氧化數。鹼金屬過錳酸鹽或者鹼土族過錳酸鹽是很強的氧化劑。二氧化錳可以用在碳鋅電池或者鹼金屬電池中的陰極材料(電子接受者)。
生物上,錳二價離子為具有很多種功能的多樣性酶的輔因子,具有錳元素的酶特別為必須處理氧元素的生物體內去除造成毒性的過氧化自由基的要素。錳同樣作用於光合作用植物中氧元素進化錯合物。雖然錳是生物體內的必須稀有礦物質,然而,當生物體內的錳濃度過高時也可能造成神經毒性。特別是經過呼吸作用,將造成錳中毒,這是一種在哺乳動物中可能會發生的不可逆神經傷害的情況。
性质
化合物
锰的氧化数有-3至+7,其中以氧化数+2、+4和+7的化合物最重要。
Mn2+
最稳定,呈粉红色,不容易被氧化,也不容易被还原。硫酸锰(MnSO
4)、氯化锰(MnCl
2)等属于这氧化数。MnO−
4和MnO
2有强氧化性。
氧化数+7的高锰酸盐(MnO−
4)呈紫色,多数是强氧化剂,如高锰酸钾、高锰酸钠、高锰酸钡等。
在酸性溶液中,Mn3+
和MnO2−
4均易发生歧化反应:
- 2 Mn3+
+ 2 H
2O → Mn2+
+ MnO
2↓ + 4 H+ - 3 MnO2−
4 + 4 H+
→ 2 MnO−
4 + MnO
2↓ + 2 H
2O
- 2 Mn3+
在碱性溶液中,Mn(OH)
2不稳定,易被空气中的氧气氧化为MnO
2;MnO2−
4也能发生歧化反应,但反应不如在酸性溶液中进行得完全。
锰的氧化物及其水合物酸碱性的递变规律,是过渡金属中最典型的:随锰的氧化数的升高,酸性逐渐增强。[3]
| 锰的氧化物 | 锰的氢氧化物 | 酸碱性 |
|---|---|---|
| MnO(绿) | Mn(OH) 2(白) | 碱性 |
| Mn 2O 3(棕) | Mn(OH) 3(棕) | 弱碱性 |
| MnO 2(黑) | Mn(OH) 4(棕黑) | 两性 |
| — | 不存在(绿) | 酸性 |
| Mn 2O 7(绿) | HMnO 4(紫红) | 强酸性 |
| 锰的氧化数[4] | |
|---|---|
| 0 | Mn 2(CO) 10 |
| +1 | MnC 5H 4CH 3(CO) 3 |
| +2 | MnCl 2, MnCO 3, MnO |
| +3 | MnF 3, Mn(OAc) 3, Mn 2O 3 |
| +4 | MnO 2 |
| +5 | K 3MnO 4 |
| +6 | K 2MnO 4 |
| +7 | KMnO 4, Mn 2O 7 |
同位素
錳在正常狀況下只存在一個穩定同位素——55Mn,此外有二十四個放射性同位素依照原子量從44到69。而具放射性中最穩定的包含半衰期分別為370萬年、312.3天、5.591天的53Mn、54Mn和52Mn,剩餘的半衰期皆少於三小時,而其中大部分都少於一分鐘。在最大量且穩定的錳同位素55Mn,主要的衰變方式為電子捕獲,而在其後者主要為β衰變。
鐵系元素被認為是超新星爆炸前不久合成巨大恆星的物質,而錳正是其一。鐵被宇宙射線衝擊會產生53Mn,而53Mn經過半衰期370萬年會衰變成53Cr,因為其相對較短的半衰期,所以53Mn較為稀有。錳同位素的含量與鉻同位素的含量有關,因此已經在同位素地質學及放射性估年法上有所應用。錳和鉻的同位素比強化了26Al和107Pd對太陽系早期歷史的證明。許多隕石中53Cr/52Cr和Mn/Cr間比例的差異顯示出最初53Mn/55Mn的比例,因此指出相異行星中錳和鉻同位素的組成,必定源自於不同的53Cr衰變過程。所以53Mn提供了太陽系合併前核合成過程近一步的證明。
发现
在歷史上,錳的名字源自於軟錳礦及其他來自希臘馬格尼西亞州的黑色礦物。
18世紀後半瑞典化學家卡爾·威廉·舍勒用軟錳礦來生成氯氣時,尚未知道是二氧化锰,只認為它是一種未知金屬的氧化物,但舍勒並沒能成功分離此金屬。约翰·戈特利布·甘恩在1774年才利用碳把兩個氧還原,成功的分離出錳。並將之命名為Manganese(錳),其拉丁语為magnes,即「具磁性的」(但只有經過特殊處理的錳才會具有磁性),及元素符號Mn亦從之而來。人們早在1913年就已知錳是組成動物的重要元素之一,但直到1931年才經由動物實驗得知和錳有關的症狀。
用途
冶金工业中用以制造特种钢,在钢铁生产上用锰铁合金作为去硫剂和去氧剂。
此外锰也用作合金,电池等。二氧化锰(MnO
2)用作催化剂和棕色颜料,高锰酸钾(KMnO
4)用作氧化剂及消毒剂。
在不鏽鋼上用磷酸錳處理可以防鏽及防蝕。工業上會使用不同氧化態的錳離子當作不同顏色的染料。含有鹼金屬或鹼土族離子的過錳酸鹽類是強氧化劑。在碳鋅電池及鹼性電池中,二氧化錳會被當作陰極使用。 在生物學中,錳離子可在多種的酵素中擔任輔因子的角色。錳酵素對組織中超氧自由基的解毒,清除元素態氧原子非常重要。錳也會在光合植物的氧釋放複合體中作用。雖然目前已知所有的有機生命體皆需要微量的錳,但其過量卻會變成神經毒素。尤其過度吸入可以導致錳中毒,有時會造成不可逆的神經危害。
對人體的影響
| 锰 | |
|---|---|
| 危险性 | |
| GHS危险性符号 none | |
| GHS提示词 | none |
| H-术语 | H401 |
| P-术语 | P273, P501[5] |
| NFPA 704 |
 0
0
0
|
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
和其他较普遍的金属相比,锰的毒性较低。[6]
錳是身體所必需的微量元素之一,可構成生物體中具重要生理功能之酶或輔酶,每日攝取約3-9mg。 具有以下之功能:
- 促進骨骼之發育以及生長
- 維持腦功能之正常運作
- 維持糖以及脂肪之正常代謝
- 維持細胞粒線體之完整
- 構成輔酶
穀類、豆類、蔬菜和甲殼類等食物為錳的主要來源。
由於粒線體需要錳,所以錳在粒線體多之組織含量較高,常見於骨骼、肝臟、腎臟、胰臟。然而過量錳之攝取依然會對生物有所影響(),常見於職業中,其發生原因為吸入含錳濃度高之錳煙及錳塵。
参考文献
- Prohaska, Thomas; Irrgeher, Johanna; Benefield, Jacqueline; Böhlke, John K.; Chesson, Lesley A.; Coplen, Tyler B.; Ding, Tiping; Dunn, Philip J. H.; Gröning, Manfred; Holden, Norman E.; Meijer, Harro A. J. . Pure and Applied Chemistry. 2022-05-04. ISSN 1365-3075. doi:10.1515/pac-2019-0603 (英语).
- Weast, Robert. . Boca Raton, Florida: Chemical Rubber Company Publishing. 1984: E110. ISBN 0-8493-0464-4.
- 《无机化学》第四版.高等教育出版社.P392. 13.4.2 锰的重要化合物
- Schmidt, Max. . . Wissenschaftsverlag. 1968: 100–109 (德语).
- https://www.sigmaaldrich.com/MSDS/MSDS/DisplayMSDSPage.do?country=US&language=en&productNumber=266167&brand=ALDRICH&PageToGoToURL=https%3A%2F%2Fwww.sigmaaldrich.com%2Fcatalog%2Fproduct%2Faldrich%2F266167%3Flang%3Den
- Hasan, Heather. . The Rosen Publishing Group. 2008: 31. ISBN 978-1-4042-1408-8.
外部連結
- 元素锰在洛斯阿拉莫斯国家实验室的介紹(英文)
- —— 锰(英文)
- 元素锰在The Periodic Table of Videos(諾丁漢大學)的介紹(英文)
- 元素锰在Peter van der Krogt elements site的介紹(英文)
- WebElements.com – 锰(英文)